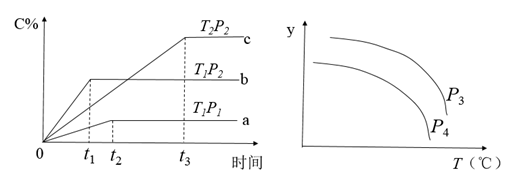
1 . 在一定体积的密闭容器中,可逆反应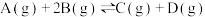 ,有如图所示的反应曲线,下列说法中错误的是
,有如图所示的反应曲线,下列说法中错误的是
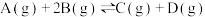 ,有如图所示的反应曲线,下列说法中错误的是
,有如图所示的反应曲线,下列说法中错误的是
| A.正反应是放热反应 | B. |
C.若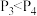 ,y轴可表示A的转化率 ,y轴可表示A的转化率 | D.若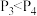 ,y轴可表示D的体积分数 ,y轴可表示D的体积分数 |
您最近一年使用:0次
2 . 已知N2(g)+3H2(g) 2NH3(g) △H<0。在温度、容积相同的甲、乙、丙三个密闭容器中,分别同时充入1molN2、3molH2,甲保持恒温、恒容;乙保持绝热、恒容;丙保持恒温、恒压,测得反应达到平衡时的有关数据如表所示,则下列说法错误的是
2NH3(g) △H<0。在温度、容积相同的甲、乙、丙三个密闭容器中,分别同时充入1molN2、3molH2,甲保持恒温、恒容;乙保持绝热、恒容;丙保持恒温、恒压,测得反应达到平衡时的有关数据如表所示,则下列说法错误的是
 2NH3(g) △H<0。在温度、容积相同的甲、乙、丙三个密闭容器中,分别同时充入1molN2、3molH2,甲保持恒温、恒容;乙保持绝热、恒容;丙保持恒温、恒压,测得反应达到平衡时的有关数据如表所示,则下列说法错误的是
2NH3(g) △H<0。在温度、容积相同的甲、乙、丙三个密闭容器中,分别同时充入1molN2、3molH2,甲保持恒温、恒容;乙保持绝热、恒容;丙保持恒温、恒压,测得反应达到平衡时的有关数据如表所示,则下列说法错误的是| 容器 | 甲(恒温、恒容) | 乙(绝热、恒容) | 丙(恒温、恒压) |
| 反应物投入量 | 1molN2、3molH2 | 1molN2、3molH2 | 1molN2、3molH2 |
| NH3的浓度/mol•L-1 | c1 | c2 | c3 |
| 反应物的转化率 | α1 | α2 | α3 |
| 化学平衡常数 | K1 | K2 | K3 |
| 混合气体的平均相对分子质量 | M1 | M2 | M3 |
| A.c2<c1<c3 | B.α2<α3<α1 |
| C.K2<K1=K3 | D.M2<M1<M3 |
您最近一年使用:0次
名校
3 . 700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O(g),发生如下反应:CO(g)+H2O(g) CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
 CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是
CO2+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法不正确的是| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.80 | 0.90 |
| t1 | 1.20 | |
| t2 | 0.30 |
| A.t2后若压缩容器体积至原来一半,再次平衡则c(H2O)=0.30mol/L |
| B.若初始量CO:3.6mol,H2O:1.8mol,则平衡时n(H2O)=0.60mol |
| C.t2后若增加0.9 mol H2O,则再次平衡时,H2的体积分数为25% |
| D.若为绝热容器(容器初始温度仍为700℃),其他条件不变,则平衡时n(H2)>0.60mol |
您最近一年使用:0次
2021-11-15更新
|
201次组卷
|
4卷引用:安徽省A10联盟2021-2022学年高二上学期期中联考化学试题
名校
4 . 某温度下,在恒容密闭容器中SO2、O2、SO3三种气态物质建立化学平衡:2SO2(g)+O2(g) 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
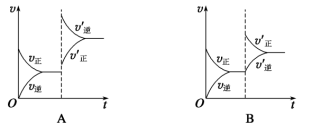
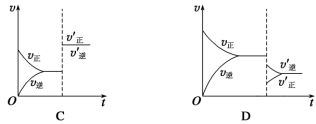
 2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是
2SO3(g) ΔH<0,改变条件对反应正、逆反应速率的影响如图所示,关于改变的条件下列说法不正确的是

| A.压缩容器体积 | B.通入O2 |
| C.通入稀有气体He | D.减低温度 |
您最近一年使用:0次
2021-11-15更新
|
202次组卷
|
2卷引用:安徽省A10联盟2021-2022学年高二上学期期中联考化学试题
5 . 一定条件下,发生反应: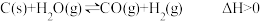 达到平衡后,下列说法错误的是
达到平衡后,下列说法错误的是
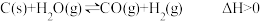 达到平衡后,下列说法错误的是
达到平衡后,下列说法错误的是| A.其它条件不变,升高温度,v(正)增大的程度比v(逆)增大的程度大,平衡向右移动 |
| B.恒温恒容条件下,充入稀有气体,v(正)、v(逆)不变,平衡不移动 |
| C.其它条件不变,增大压强,v(正)、v(逆)同倍数增大,平衡不移动 |
| D.恒温恒容条件下,加入碳粉,v(正)不变,v(逆)不变,平衡不移动 |
您最近一年使用:0次
2021-11-13更新
|
360次组卷
|
6卷引用:河南省中原名校2021-2022学年高二上学期第一次联考化学试题
河南省中原名校2021-2022学年高二上学期第一次联考化学试题河南省实验中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)黑龙江省绥化市第一中学2021-2022学年高二上学期期中考试化学试卷新疆乌鲁木齐市第八中学2021-2022学年高二上学期第二次月考化学试题云南省昆明市官渡区第一中学2021-2022学年高二上学期期中考试化学试题
6 . 已知甲为恒压容器、乙为恒容容器。发生反应:2NO2(g)⇌N2O4(g) △H<0。一段时间后相继达到平衡状态。下列说法中正确的是

| A.达到平衡所需时间,甲与乙相等 |
| B.平衡时NO2体积分数:甲<乙 |
| C.该反应的平衡常数表达式K=c(N2O4)/c(NO2) |
| D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态 |
您最近一年使用:0次
名校
7 . 25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.方程式为X+3Y⇌2Z,平衡常数为1600 |
| C.增大压强使平衡正向方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
2021-12-29更新
|
223次组卷
|
11卷引用:河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题
河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题(已下线)第二章 第三节化学平衡(第3课时 化学平衡常数)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期12月月考化学试题河南省范县第一中学等学校2021-2022学年高二上学期联考检测化学试题 广西玉林市市直六所普通高中2021-2022学年高二上学期期中考试理科综合化学试题河南省安阳市滑县实验学校2020-2021学年高二上学期期中考试化学试题(普通班)内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题
名校
8 . 可逆反应A(g)+B C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
 C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是| A.增大压强,平衡不移动说明B、D一定是气体 |
| B.若A为有色气体,增大A的浓度,平衡体系气体颜色加深 |
| C.若B是气体,增大B的浓度会使A的转化率增大 |
| D.升高温度C的质量分数减小,说明正反应为放热反应 |
您最近一年使用:0次
2021-10-23更新
|
244次组卷
|
2卷引用:山西省长治市第二中学校2021-2022学年高二上学期第一次月考化学试题
9 . 甲醇水蒸气重整制氢具有能耗低、产物组成简单、副产物易分离等优点,是未来制氢技术的重要发展方向。该重整反应体系主要涉及以下反应:
I.CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H1
CO2(g)+3H2(g) △H1
II.CH3OH(g) CO(g)+2H2(g) △H2=+90kJ•mol-1
CO(g)+2H2(g) △H2=+90kJ•mol-1
(1)已知CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1
反应I的△H1=___ kJ•mol-1。
(2)将组成(物质的量分数)为25%CH3OH(g)、35%H2O(g)和40%N2(g)(N2不参与反应)的气体通入恒容容器中反应相同时间,测得CH3OH转化率和产物的物质的量分数随温度变化关系如图所示。
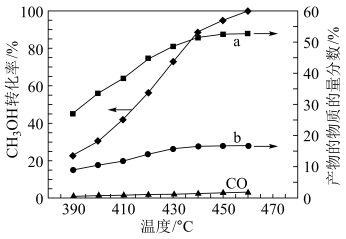
①曲线a和b分别代表产物___ 和___ 。
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有___ 。
A.增大N2的浓度,反应I、II的正反应速率都增加
B.移除CO2能提高CH3OH的平衡转化率
C.升高温度,N2的物质的量分数保持不变
D.440℃~460℃时,升高温度,H2的产率增大
③反应I活化能小于反应II,结合图中信息解释判断依据___ 。
(3)一定条件下,向2L的恒容密闭容器中通入1molCH3OH(g)和1molH2O(g)发生上述反应,达到平衡时,容器中CO2为0.8mol,CO为0.1mol,此时H2的浓度为___ mol•L-1,反应I的平衡常数K=___ (写出计算式)。
(4)研究发现以铜作催化剂时,反应I经历三步:
①CH3OH→HCHO+H2,
②HCHO+H2O→HCOOH+H2,
③___ 。
I.CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H1
CO2(g)+3H2(g) △H1II.CH3OH(g)
 CO(g)+2H2(g) △H2=+90kJ•mol-1
CO(g)+2H2(g) △H2=+90kJ•mol-1(1)已知CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1反应I的△H1=
(2)将组成(物质的量分数)为25%CH3OH(g)、35%H2O(g)和40%N2(g)(N2不参与反应)的气体通入恒容容器中反应相同时间,测得CH3OH转化率和产物的物质的量分数随温度变化关系如图所示。

①曲线a和b分别代表产物
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有
A.增大N2的浓度,反应I、II的正反应速率都增加
B.移除CO2能提高CH3OH的平衡转化率
C.升高温度,N2的物质的量分数保持不变
D.440℃~460℃时,升高温度,H2的产率增大
③反应I活化能小于反应II,结合图中信息解释判断依据
(3)一定条件下,向2L的恒容密闭容器中通入1molCH3OH(g)和1molH2O(g)发生上述反应,达到平衡时,容器中CO2为0.8mol,CO为0.1mol,此时H2的浓度为
(4)研究发现以铜作催化剂时,反应I经历三步:
①CH3OH→HCHO+H2,
②HCHO+H2O→HCOOH+H2,
③
您最近一年使用:0次
2021-12-22更新
|
430次组卷
|
3卷引用:广东省广州市2021-2022学年高三上学期12月调研考试化学试题
广东省广州市2021-2022学年高三上学期12月调研考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省茂名高州市2021-2022学年高二上学期期末考试化学试题
10 . 科学家提出利用CO2与CH4制备“合成气”(CO、H2),发生反应 ,在200℃时,向5L带气压计的恒容密闭容器中通入
,在200℃时,向5L带气压计的恒容密闭容器中通入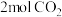 和
和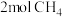 ,测得初始压强为
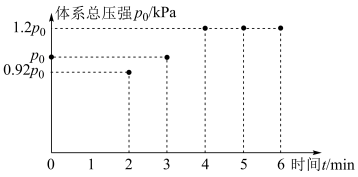
,测得初始压强为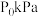 ,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。下列说法不正确的是
,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。下列说法不正确的是
 ,在200℃时,向5L带气压计的恒容密闭容器中通入
,在200℃时,向5L带气压计的恒容密闭容器中通入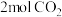 和
和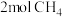 ,测得初始压强为
,测得初始压强为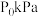 ,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。下列说法不正确的是
,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。下列说法不正确的是
| A.容器内总压强与初始相比增加了20%说明该反应已达平衡状态 |
B.图中0min到2min压强变化可知该反应 |
C.用平衡分压代替平衡浓度衣示的化学平衡常数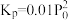 [气体分压(P分)气体总压(P总)×气体体积分数] [气体分压(P分)气体总压(P总)×气体体积分数] |
D.平衡后若继续往容器内通入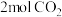 和 和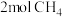 ,再次达到平衡后各组分的物质的量分数保持不变 ,再次达到平衡后各组分的物质的量分数保持不变 |
您最近一年使用:0次
2021-10-19更新
|
302次组卷
|
2卷引用:重庆市巴蜀中学校2021-2022学年高二上学期(10月)第一次月考化学试题



