1 . 煤的液化是获得清洁燃料的一种方式,有人设想先用煤与水蒸气反应生成CO,再通过反应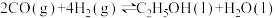
 实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
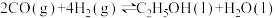
 实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是| A.其他条件不变,增大反应体系的压强,既有利于提高CO和H2的平衡转化率,又有利于加快化学反应速率 |
| B.其他条件不变,升高反应体系的温度,能够加快反应逃率,但CO和H2的平衡转化率降低 |
| C.其他条件不变,增大CO的浓度,CO和H2的平衡转化率均升高 |
| D.其他条件不变,使用高效催化剂,能够加快反应速率。但不能提高CO和H2的平衡转化率 |
您最近一年使用:0次
2021-11-17更新
|
135次组卷
|
2卷引用:江苏省省级联测2021-2022学年高二上学期第二次联考化学试题
2 . 在密闭容器中发生反应: ,下列有关说法正确的是
,下列有关说法正确的是
 ,下列有关说法正确的是
,下列有关说法正确的是| A.CO2、H2的消耗反应速率之比为3∶1 |
| B.该反应在高温下能自发进行 |
C.达到平衡后,向容器中加入少量 固体,CO2的平衡转化率增大 固体,CO2的平衡转化率增大 |
| D.达到平衡后,缩小体积,正反应速率增大程度小于逆反应的 |
您最近一年使用:0次
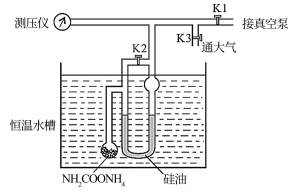
3 . 氨基甲酸铵发生分解的化学方程式为NH2COONH4(s) 2NH3(g)+CO2(g)。利用如图装置测定不同温度下该反应以分压表示的化学平衡常数Kp,实验步骤如下:
2NH3(g)+CO2(g)。利用如图装置测定不同温度下该反应以分压表示的化学平衡常数Kp,实验步骤如下:
(Ⅰ)关闭K3,打开K1和K2,开启真空泵抽气至测压仪数值稳定后关闭K1
(Ⅱ)关闭K2,缓慢开启K3至U形管两边液面相平并保持不变,读取压强数值。记录25℃、30℃下压强分别为12.0kPa、17.1kPa。下列说法错误的是
 2NH3(g)+CO2(g)。利用如图装置测定不同温度下该反应以分压表示的化学平衡常数Kp,实验步骤如下:
2NH3(g)+CO2(g)。利用如图装置测定不同温度下该反应以分压表示的化学平衡常数Kp,实验步骤如下:(Ⅰ)关闭K3,打开K1和K2,开启真空泵抽气至测压仪数值稳定后关闭K1
(Ⅱ)关闭K2,缓慢开启K3至U形管两边液面相平并保持不变,读取压强数值。记录25℃、30℃下压强分别为12.0kPa、17.1kPa。下列说法错误的是

| A.若保持温度和容器体积不变,平衡后再充入n(NH3):n(CO2)=2:1,再次达到平衡时c(NH3)不变 |
| B.气体平均分子量不变不能作为判断反应达到平衡状态的依据 |
| C.该反应25℃时的化学平衡常数Kp=2.56×1011Pa3 |
| D.步骤Ⅱ中读数时U形管左侧液面偏低,Kp测量值偏大 |
您最近一年使用:0次
名校
4 . 砷(As)是第四周期VA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途,回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。化学反应化学方程式为:2As2S3+5O2+6H2O=4H3AsO4+6S。该反应需要在加压下进行,原因是:___________
(2)298K时,将20mL3xmol/L Na3AsO3、20mL3xmol/LI2和20mL NaOH溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-=AsO
(aq)+I2(aq)+2OH-=AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
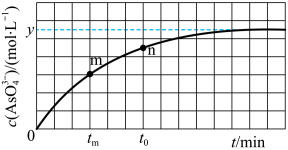
①下列可判断反应达到平衡状态的是___________ (填标号)
a.溶液的pH不再变化 b.v(I-)=2v(AsO )
)
c.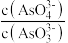 不再变化 d.c(I-)=ymol⋅L-1
不再变化 d.c(I-)=ymol⋅L-1
②tm时,v正___________ v逆(填“大于”“小于”成“等于”)
③若平衡时溶液的pH=14,则该反应的平衡常数K=___________ (用x、y代数式表示)
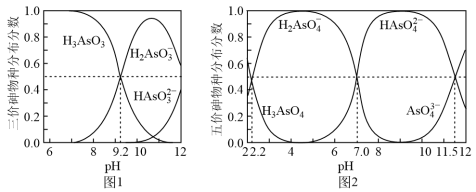
(3)常温下,H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图−1和图−2所示。下列说法错误的是___________
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。化学反应化学方程式为:2As2S3+5O2+6H2O=4H3AsO4+6S。该反应需要在加压下进行,原因是:
(2)298K时,将20mL3xmol/L Na3AsO3、20mL3xmol/LI2和20mL NaOH溶液混合,发生反应:AsO
 (aq)+I2(aq)+2OH-=AsO
(aq)+I2(aq)+2OH-=AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡状态的是
a.溶液的pH不再变化 b.v(I-)=2v(AsO
 )
)c.
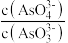 不再变化 d.c(I-)=ymol⋅L-1
不再变化 d.c(I-)=ymol⋅L-1②tm时,v正
③若平衡时溶液的pH=14,则该反应的平衡常数K=
(3)常温下,H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图−1和图−2所示。下列说法错误的是___________

A.以酚酞为指示剂,将氢氧化钠溶液逐滴加入到亚砷酸H3AsO3溶液中,当溶液由无色变为浅红色时,主要反应的离子方程式为:OH-+H3AsO3=H2AsO +H2O +H2O |
| B.常温下,H3AsO4清液中Ka1:Ka2:Ka3=109.3:105.5:1 |
C.H3AsO4水溶液中存在:c(H+)=c(OH-)+c(H2AsO )+2c(HAsO )+2c(HAsO )+3c(AsO )+3c(AsO ) ) |
| D.H3AsO3和Na2HAsO4水溶液可发生复分解反应 |
您最近一年使用:0次
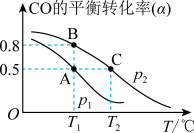
5 . CO可用于合成甲醇,其反应的化学方程式为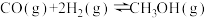 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法不正确 的是
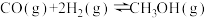 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
| A.合成甲醇的反应为放热反应 |
| B.压强为P1<P2 |
| C.A、B、C三点的平衡常数为KA=KB>KC |
| D.A点的v正和C点的v逆相等 |
您最近一年使用:0次
2021-11-12更新
|
163次组卷
|
3卷引用: 浙江省金华十校2021-2022学年高三上学期11月模拟考试化学试题
浙江省金华十校2021-2022学年高三上学期11月模拟考试化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
6 . 下列关于2SO2(g)+O2(g)⇌2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
| A.该反应的∆S>0 |
| B.该反应中,反应物的总能量小于生成物的总能量 |
| C.生产过程中将SO3分离出去,逆反应速率减慢 |
| D.其他条件不变,增大压强,平衡右移,平衡常数增大 |
您最近一年使用:0次
2021-12-14更新
|
532次组卷
|
5卷引用:江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题
江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题(已下线)第22讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期末考试化学试题 江苏省苏州市重点中学2022-2023学年高三上学期10月月考化学试题江苏省灌南高级中学2023-2024学年高三上学期第一次月考化学试题
名校
7 . 某密闭容器中充入等物质的量的A和B,一定温度下发生反应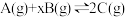 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
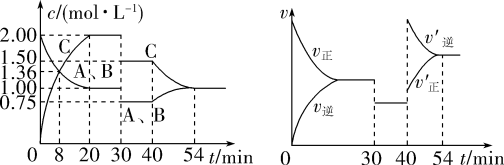
下列说法中不正确 的是
 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
下列说法中
| A.30min~40min间该反应使用了催化剂 |
| B.反应方程式中的x=1 |
| C.正反应为放热反应 |
| D.前8minA的平均反应速率为0.08mol·L-1·min-1 |
您最近一年使用:0次
名校
解题方法
8 . 如图,关闭活塞K,向A中充入1molX、1molY,向B中充入2molX、2molY,此时A的容积是aL,B的容积是2aL。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g) +Y(g)⇌2Z(g)+W(g) ΔH<0 。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
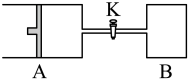

| A.反应速率v(B) > v(A) |
| B.A中X的转化率为80% |
| C.平衡时Y的体积分数:A<B |
| D.若打开K,则A的体积变为2.4aL |
您最近一年使用:0次
2021-11-06更新
|
197次组卷
|
2卷引用:湖北省沙市中学2021-2022学年高二上学期期中考试化学试题
9 . 在体积可变的密闭容器中投入0.5molE和1molF,在一定条件下发生反应: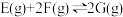
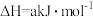 (a<0)。实验测得平衡时F的转化率随温度、压强的变化如图所示。下列说法错误的是
(a<0)。实验测得平衡时F的转化率随温度、压强的变化如图所示。下列说法错误的是

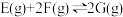
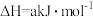 (a<0)。实验测得平衡时F的转化率随温度、压强的变化如图所示。下列说法错误的是
(a<0)。实验测得平衡时F的转化率随温度、压强的变化如图所示。下列说法错误的是
A.Y代表压强,且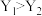 |
B.M、M两点对应的平衡常数: |
C.M、N两点对应的 |
| D.保持温度和压强不变,向平衡体系中再充入物质的量之比为1:2的E(g)和F(g),平衡时反应物的转化率增大 |
您最近一年使用:0次
10 . 利用合成气(主要成分为CO、CO2和H2)制备甲醇的主要反应有
①CO(g) +2H2(g) CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol
②CO2(g)+ H2(g) CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
①CO(g) +2H2(g)
 CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol②CO2(g)+ H2(g)
 CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
| A.增大CO2的浓度,有利于提高甲醇的产量 |
| B.升高温度,①和②反应速率都加快 |
| C.压缩体积,反应②平衡不移动 |
| D.平衡时c(CH3OH)为0.07 mol/L |
您最近一年使用:0次
2021-12-03更新
|
175次组卷
|
2卷引用:河北省百师联盟2022届高三上学期一轮复习联考(三)化学试题



