1 . 煤的液化是获得清洁燃料的一种方式,有人设想先用煤与水蒸气反应生成CO,再通过反应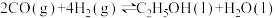
 实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
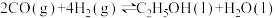
 实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是
实现煤的液化,若要利用这个反应进行乙醇的工业化生产,下列说法错误的是| A.其他条件不变,增大反应体系的压强,既有利于提高CO和H2的平衡转化率,又有利于加快化学反应速率 |
| B.其他条件不变,升高反应体系的温度,能够加快反应逃率,但CO和H2的平衡转化率降低 |
| C.其他条件不变,增大CO的浓度,CO和H2的平衡转化率均升高 |
| D.其他条件不变,使用高效催化剂,能够加快反应速率。但不能提高CO和H2的平衡转化率 |
您最近一年使用:0次
2021-11-17更新
|
135次组卷
|
2卷引用:江苏省省级联测2021-2022学年高二上学期第二次联考化学试题
2 . 在密闭容器中发生反应: ,下列有关说法正确的是
,下列有关说法正确的是
 ,下列有关说法正确的是
,下列有关说法正确的是| A.CO2、H2的消耗反应速率之比为3∶1 |
| B.该反应在高温下能自发进行 |
C.达到平衡后,向容器中加入少量 固体,CO2的平衡转化率增大 固体,CO2的平衡转化率增大 |
| D.达到平衡后,缩小体积,正反应速率增大程度小于逆反应的 |
您最近一年使用:0次
3 . 二氧化碳到淀粉的人工合成第一步为用无机催化剂将二氧化碳还原为甲醇,反应方程式为3H2(g)+CO2(g) CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比
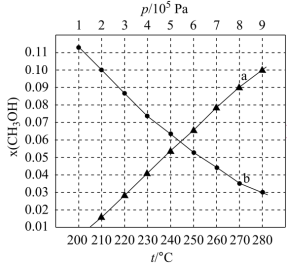
CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比 =3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
=3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
 CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比
CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比 =3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
=3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
| A.当体系中c(CH3OH)与c(H2)比值不变,可说明此时该反应达到平衡状态 |
| B.曲线b表示的是压强相同时,温度升高该反应逆向移动,说明正反应放热 |
| C.在原p=5×105Pa,210℃的条件下,向该恒容密闭容器中继续通入3molH2与1molCO2,达到新的平衡后,x(CH3OH)<0.10 |
| D.当x(CH3OH)=0.10时,反应条件可能为p=5×105Pa,210℃或p=9×105Pa,250℃ |
您最近一年使用:0次
2021-12-15更新
|
439次组卷
|
3卷引用:浙江省普通高中强基联盟2022届高三上学期12月统测化学试题
浙江省普通高中强基联盟2022届高三上学期12月统测化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)北京市海淀区教师进修学校2022-2023学年高三下学期开学检测化学试题
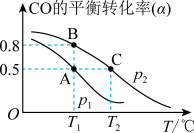
4 . CO可用于合成甲醇,其反应的化学方程式为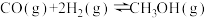 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法不正确 的是
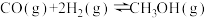 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
| A.合成甲醇的反应为放热反应 |
| B.压强为P1<P2 |
| C.A、B、C三点的平衡常数为KA=KB>KC |
| D.A点的v正和C点的v逆相等 |
您最近一年使用:0次
2021-11-12更新
|
163次组卷
|
3卷引用: 浙江省金华十校2021-2022学年高三上学期11月模拟考试化学试题
浙江省金华十校2021-2022学年高三上学期11月模拟考试化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
5 . 某温度下,在恒容密闭容器中加入一定量X,发生反应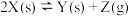 ,一段时间后达到平衡。下列说法错误的是
,一段时间后达到平衡。下列说法错误的是
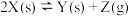 ,一段时间后达到平衡。下列说法错误的是
,一段时间后达到平衡。下列说法错误的是A.升高温度,若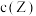 增大,则 增大,则 |
B.加入一定量Z,达新平衡后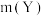 减小 减小 |
C.加入等物质的量的Y和Z,达新平衡后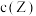 增大 增大 |
| D.加入一定量氩气,平衡不移动 |
您最近一年使用:0次
2021-09-13更新
|
11037次组卷
|
44卷引用:2021年新高考辽宁化学高考真题
2021年新高考辽宁化学高考真题江西省南昌市南昌大学附属中学 2021-2022学年高二上学期第一次月考化学试卷(已下线)专题23 化学平衡的移动和化学反应进行的方向(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练天津市西青区张家窝中学2022届高三上学期第一次月考化学试题湖南省临澧县第一中学2021-2022学年高二上学期第一次阶段性考试化学试题黑龙江省佳木斯市第一中学2021-2022 学年高二上学期期中考试化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)辽宁省实验中学2021-2022学年高二上学期11月期中阶段测化学试题辽宁省实验中学2021-2022学年高二上学期期中考试化学试题2021年北京高考化学试题变式题1-102021年辽宁高考化学试题变式题11-19浙江省吴兴高级中学2021-2022学年高二上学期12月月考化学试题广东省珠海市第一中学2021-2022学年高二上学期期中考试化学试题内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)安徽省皖南地区2021-2022学年高二下学期开学调研考试化学试题天津市河东区2021-2022学年高三上学期期末质量检测化学试题辽宁省沈阳市第五中学2021-2022学年高三下学期3月月考化学试题(已下线)押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题河北省行唐启明中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题5-8)广东华侨中学2022-2023学年高二上学期期中考试化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡章末检测卷(二) 化学反应速率与化学平衡(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题江西省永修县第一中学2023-2024学年高二上学期10月月考化学试题(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题天津市耀华中学2023-2024学年高三上学期第二次月考化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期第一次质量检测化学试题 四川省成都市石室中学2023~2024学年高二上学期10月月考化学试题黑龙江省哈尔滨市第三中学校2023-2024学年高二上学期期中考试化学试题山东省淄博市沂源县第一中学2023-2024学年高二上学期期中考试化学试题河北省保定市唐县第一中学2023-2024学年高二上学期12月期中考试化学试题云南省开远市第一中学校2023-2024学年高二下学期开学考试化学试题
名校
解题方法
6 . 通过反应Ⅰ: 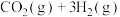

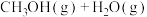
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:
反应Ⅱ:
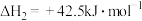
反应Ⅲ:
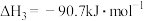
密闭容器中,反应物起始物质的量比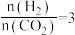 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为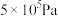 下温度变化)达到平衡时
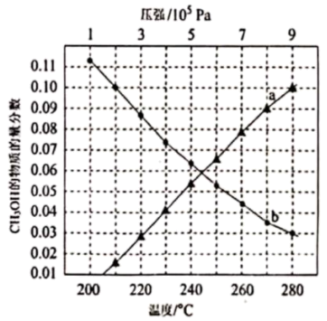
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
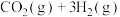

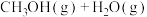
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:反应Ⅱ:

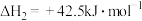
反应Ⅲ:

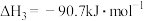
密闭容器中,反应物起始物质的量比
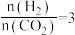 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为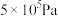 下温度变化)达到平衡时
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
A.反应Ⅰ的平衡常数可表示为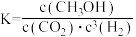 |
B.曲线 表示CH3OH的物质的量分数随温度变化 表示CH3OH的物质的量分数随温度变化 |
| C.提高CO2转化为CH3OH的转化率,需要研发在低温区高效的催化剂 |
D.在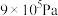 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 |
您最近一年使用:0次
2021-09-11更新
|
390次组卷
|
3卷引用:江苏省苏州市2021-2022学年高三上学期期初调研考试化学试题
名校
7 . 某密闭容器中充入等物质的量的A和B,一定温度下发生反应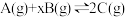 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
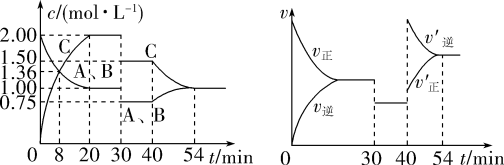
下列说法中不正确 的是
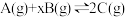 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
下列说法中
| A.30min~40min间该反应使用了催化剂 |
| B.反应方程式中的x=1 |
| C.正反应为放热反应 |
| D.前8minA的平均反应速率为0.08mol·L-1·min-1 |
您最近一年使用:0次
名校
解题方法
8 . 如图,关闭活塞K,向A中充入1molX、1molY,向B中充入2molX、2molY,此时A的容积是aL,B的容积是2aL。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g) +Y(g)⇌2Z(g)+W(g) ΔH<0 。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
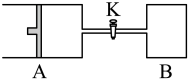

| A.反应速率v(B) > v(A) |
| B.A中X的转化率为80% |
| C.平衡时Y的体积分数:A<B |
| D.若打开K,则A的体积变为2.4aL |
您最近一年使用:0次
2021-11-06更新
|
197次组卷
|
2卷引用:湖北省沙市中学2021-2022学年高二上学期期中考试化学试题
9 . 燃煤电厂锅炉尾气中含有氮氧化物(主要成分NO),可通过主反应4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=-1627.7kJ·mol-1除去。温度高于300℃时会发生副反应:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-904.7kJ·mol-1。在恒压、反应物起始物质的量之比一定的条件下,反应相同时间,NO的转化率在不同催化剂作用下随温度变化的曲线如图所示。下列有关说法一定正确的是
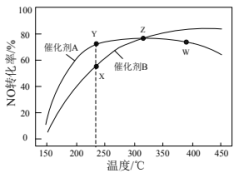

| A.N2(g)+O2(g)=2NO(g) △H=-180.7kJ·mol-1 |
| B.图中X点所示条件下,反应时间足够长,NO的转化率能达到Y点的值 |
| C.关于X、Y、Z三点,KX=KY,Z点反应达到化学平衡状态 |
| D.图中Z点到W点NO的转化率降低的原因是主反应的平衡逆向移动 |
您最近一年使用:0次
2021高三·全国·专题练习
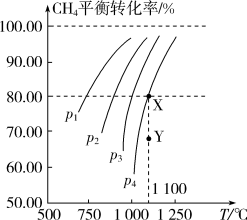
10 . 在一恒容的密闭容器中充入0.1 mol·L-1 CO2、0.1 mol·L-1CH4,在一定条件下发生反应:CH4(g)+CO2(g)  2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图。下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图。下列有关说法不正确的是
 2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图。下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图。下列有关说法不正确的是
| A.上述反应的ΔH<0 |
| B.压强:p4>p3>p2>p1 |
| C.1 100 ℃时该反应的平衡常数为1.64 |
| D.压强为p4时,在Y点:v正<v逆 |
您最近一年使用:0次



