1 . 一定温度下,某气态平衡体系的平衡常数表达式为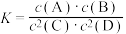 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
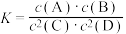 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是A.升高温度,平衡常数 一定增大 一定增大 | B.增大 浓度,平衡向正反应方向移动 浓度,平衡向正反应方向移动 |
C.增大压强, 体积分数增加 体积分数增加 | D.升高温度,若 的百分含量减少,则正反应是放热反应 的百分含量减少,则正反应是放热反应 |
您最近一年使用:0次
2021-10-15更新
|
134次组卷
|
3卷引用:山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题
山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)四川省广安市育才学校2022-2023学年高二上学期11月期中考试化学试题
名校
2 . 在三个相同容器中各充入1molN2和3molH2,在不同条件下反应达到平衡,氨的体积分数随时间变化的曲线如图所示。下列说法中正确的是
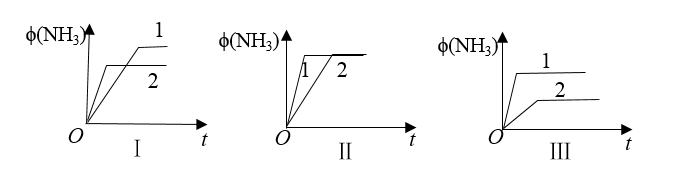

| A.图Ⅰ可能是不同压强对反应的影响,且p2>p1 |
| B.图Ⅱ可能是不同压强对反应的影响,且p1>p2 |
| C.图Ⅲ可能是不同温度对反应的影响,且T1>T2 |
| D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2 |
您最近一年使用:0次
名校
解题方法
3 . 使用石油热裂解的副产物 来制取
来制取 和
和 ,其生产流程如下图:
,其生产流程如下图:
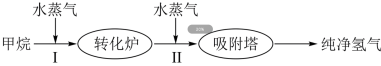
(1)工业上常利用反应Ⅰ产生的 和
和 合成可再生能源甲醇。
合成可再生能源甲醇。
根据图甲写出生成 的热化学方程式
的热化学方程式___________ 。
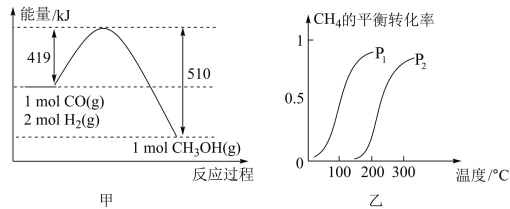
(2)此流程的第Ⅰ步反应为: ,一定条件下
,一定条件下 的平衡转化率与温度、压强的关系如图乙,则P1
的平衡转化率与温度、压强的关系如图乙,则P1___________ P2 (填“小于”、“大于”或“等于”)。 时,将
时,将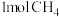 和
和 通入容积为
通入容积为 的恒容密闭容器中,达到平衡时
的恒容密闭容器中,达到平衡时 的转化率为0.8,此时该反应的平衡常数
的转化率为0.8,此时该反应的平衡常数
___________  (保留小数点后两位数字)。
(保留小数点后两位数字)。
(3) 和
和 在一定温度下发生反应:
在一定温度下发生反应:
 。且该温度下,反应的平衡常数
。且该温度下,反应的平衡常数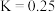 。在容积为
。在容积为 的恒容密闭容器中充入
的恒容密闭容器中充入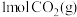 、
、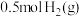 ,
,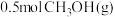 和
和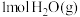 ,比较该时刻,正、逆反应速率大小:
,比较该时刻,正、逆反应速率大小:
___________ 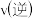 (填“
(填“ ”“
”“ ”或“
”或“ ”)。该反应的平衡常数
”)。该反应的平衡常数 与温度
与温度 的关系如图1所示,
的关系如图1所示, 的转化率如图2所示,下列说法错误的是
的转化率如图2所示,下列说法错误的是___________ 。
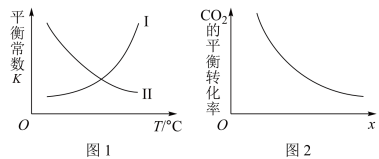
a. 在图1中,曲线Ⅱ表示该反应的平衡常数 与温度
与温度 的关系
的关系
b. 其他条件不变下,图2中 可表示温度或压强或投料比
可表示温度或压强或投料比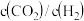
c. 用二氧化碳合成甲醇体现了碳减排理念
 来制取
来制取 和
和 ,其生产流程如下图:
,其生产流程如下图:
(1)工业上常利用反应Ⅰ产生的
 和
和 合成可再生能源甲醇。
合成可再生能源甲醇。根据图甲写出生成
 的热化学方程式
的热化学方程式
(2)此流程的第Ⅰ步反应为:
 ,一定条件下
,一定条件下 的平衡转化率与温度、压强的关系如图乙,则P1
的平衡转化率与温度、压强的关系如图乙,则P1 时,将
时,将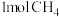 和
和 通入容积为
通入容积为 的恒容密闭容器中,达到平衡时
的恒容密闭容器中,达到平衡时 的转化率为0.8,此时该反应的平衡常数
的转化率为0.8,此时该反应的平衡常数
 (保留小数点后两位数字)。
(保留小数点后两位数字)。(3)
 和
和 在一定温度下发生反应:
在一定温度下发生反应:
 。且该温度下,反应的平衡常数
。且该温度下,反应的平衡常数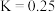 。在容积为
。在容积为 的恒容密闭容器中充入
的恒容密闭容器中充入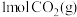 、
、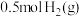 ,
,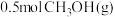 和
和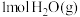 ,比较该时刻,正、逆反应速率大小:
,比较该时刻,正、逆反应速率大小:
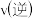 (填“
(填“ ”“
”“ ”或“
”或“ ”)。该反应的平衡常数
”)。该反应的平衡常数 与温度
与温度 的关系如图1所示,
的关系如图1所示, 的转化率如图2所示,下列说法错误的是
的转化率如图2所示,下列说法错误的是
a. 在图1中,曲线Ⅱ表示该反应的平衡常数
 与温度
与温度 的关系
的关系b. 其他条件不变下,图2中
 可表示温度或压强或投料比
可表示温度或压强或投料比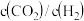
c. 用二氧化碳合成甲醇体现了碳减排理念
您最近一年使用:0次
2021-10-11更新
|
80次组卷
|
2卷引用:山东省2021-2022学年高二10月“山东学情”联考化学试题(B)
名校
4 . 利用 CO2与丙烷反应生成丙烯和水蒸气的反应机理如图所示。下列说法错误的是


| A.C3H8是还原剂 | B.CrO3作催化剂 |
| C.Cr2O3是反应的中间体 | D.增大压强有利于提高 CO2的转化率 |
您最近一年使用:0次
2021-10-11更新
|
491次组卷
|
4卷引用:广东省深圳市第七高级中学2022届高三上学期9月月考化学试题
广东省深圳市第七高级中学2022届高三上学期9月月考化学试题广东省深圳市第七高级中学2022届高三第二次月考化学试题山西省长治市上党区一中2021-2022学年高二上学期10月月考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-讲义
名校
5 . 工业上利用C和H2O(g)来制造水煤气,可以进一步制造重要的工业原料甲醇。现有10molC(s)和5molH2O(g)在一定条件下发生反应:C(s)+H2O(g) CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
 CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是| A.再加入1molH2O(g),平衡时H2O(g)的转化率减小 |
| B.v[C(s)]=0.2mol·L-1·s-1 |
| C.水蒸气的转化率为40% |
| D.反应生成了2molCO |
您最近一年使用:0次
名校
6 . 已知: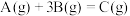
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入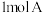 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法错误的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法错误的是
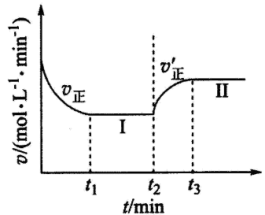
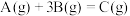
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入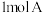 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法错误的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法错误的是
| A.容器内压强不变,表明反应达到平衡 |
B. 时改变的条件:向容器中加入 时改变的条件:向容器中加入 |
C.平衡时 的体积分数 的体积分数 : :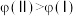 |
D.反应开始后, 与 与 的浓度之比不变 的浓度之比不变 |
您最近一年使用:0次
2021-09-23更新
|
271次组卷
|
4卷引用:山西省长治市2022届高三上学期九月份质量监测化学试题
20-21高三下·浙江·阶段练习
7 . 硫酸在国民经济中占有极其重要的地位,工业上常用黄铁矿为原料接触法制硫酸。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式_______ 。
(2)硫酸的生产中,下列说法不正确的是_______ 。
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应: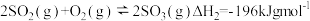 ,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
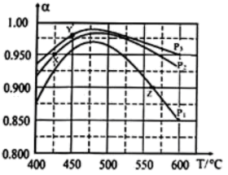
请回答:
①据图判断p1、p2、p3的大小关系_______ 。
②判断X、Y、Z中属于平衡点的是_______ (填“X”、 “Y”、 “Z”),并计算该温度下平衡的Kp=_______ 。(用含p1或p2或p3的式子表示)。
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
①恒容、恒温(T1)条件下,反应体系中c(SO2)随时间t变化的总趋势如图。结合已知信息分析c(SO2)浓度随时间t变化的原因_______ 。
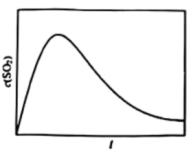
②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图_______ 。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式
(2)硫酸的生产中,下列说法不正确的是
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应:
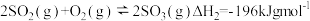 ,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
请回答:
①据图判断p1、p2、p3的大小关系
②判断X、Y、Z中属于平衡点的是
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
| 反应 | 活化能 | 平衡常数 | |
| I | 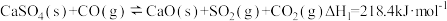 | EaI | KI |
| II | 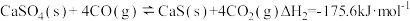 | EaII(EaII>EaI) | KII(KI>KII) |

②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图
您最近一年使用:0次
名校
解题方法
8 . 对于反应2SO2(g)+O2(g) 2SO3(g),下列有关说法不正确的是
2SO3(g),下列有关说法不正确的是
 2SO3(g),下列有关说法不正确的是
2SO3(g),下列有关说法不正确的是| A.使用催化剂能缩短该反应到达平衡的时间 |
| B.升高温度有利于提高SO2的平衡转化率 |
C.提高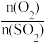 的值可增大SO2的转化率 的值可增大SO2的转化率 |
| D.增大体系的压强能提高SO2的反应速率和转化率 |
您最近一年使用:0次
2021-06-23更新
|
482次组卷
|
6卷引用:江苏省盐城市东台创新高级中学2020-2021学年高二4月份月检测化学试题
江苏省盐城市东台创新高级中学2020-2021学年高二4月份月检测化学试题(已下线)2.3.2 影响化学平衡状态的因素-2021-2022学年高二化学课后培优练(人教版选修4)江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期第一次阶段性诊断测试化学试题(已下线)2.4 化学反应的调控(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)江苏省常州市第一中学2022-2023学年高二上学期期末考试化学试题江苏省常州市第一中学2023-2024学年高二上学期10月月考化学试题
名校
9 . 在密闭容器中进行某可逆反应 , 在 t1 时刻降低温度或减小压强, 速率的变化均符合下图中的情况 ,则有关该反应的说法中不正确的是
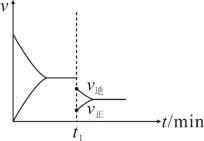

| A.由图判断△S小于0 |
| B.由图判断△H <0 |
| C.降低温时,达到新平衡时平衡常数增大 |
| D.降温或减压,平衡向逆反应方向移动 |
您最近一年使用:0次
名校
10 . NO2与N2O4能相互转化,热化学方程式为N2O4(g)⇌2NO2(g)ΔH=57kJ·mol-1,下列有关说法正确的是
| A.升高体系温度正反应速率增大,逆反应速率也增大 |
| B.若容器体积不变,气体密度不变时说明该反应建立化学平衡 |
C.其它条件不变,向平衡后的容器中再加入少量N2O4, 的值变大 的值变大 |
| D.增大体系的压强能提高N2O4的反应速率和转化率 |
您最近一年使用:0次



