利用合成气(主要成分为CO、CO2和H2)制备甲醇的主要反应有
①CO(g) +2H2(g) CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol
②CO2(g)+ H2(g) CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
①CO(g) +2H2(g)
 CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol②CO2(g)+ H2(g)
 CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
| A.增大CO2的浓度,有利于提高甲醇的产量 |
| B.升高温度,①和②反应速率都加快 |
| C.压缩体积,反应②平衡不移动 |
| D.平衡时c(CH3OH)为0.07 mol/L |
更新时间:2021-12-03 10:31:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中不能用勒夏特列原理解释是
| A.由H2、I2(g)、HI(g)气体组成的平衡体系压缩体积后颜色变深 |
| B.实验室常用排饱和食盐水法收集氯气 |
| C.红棕色的NO2,加压后颜色先变深后变浅 |
D.工业制取金属钾[Na(l)+KCl(l) NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来 NaCl(l)+ K(g)]时,使K变成蒸气从混合体系中分离出来 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列能用勒夏特列原理解释的有几个
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②棕红色NO2加压后颜色先变深后变浅
③氯水宜保存在低温、避光条件下
④实验室用排饱和食盐水的方法收集氯气
⑤由H2(g)、I2(g)、HI(g)组成的平衡体系加压(缩小体积)后颜色变深
⑥合成氨时将氨液化分离,可提高原料的利用率
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②棕红色NO2加压后颜色先变深后变浅
③氯水宜保存在低温、避光条件下
④实验室用排饱和食盐水的方法收集氯气
⑤由H2(g)、I2(g)、HI(g)组成的平衡体系加压(缩小体积)后颜色变深
⑥合成氨时将氨液化分离,可提高原料的利用率
| A.6 | B.5 | C.4 | D.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】2SO2(g)+O2(g) 2SO3(g)ΔH<0是硫酸制造工业的基本反应。将2.0L密闭反应器置于常压下某恒温环境中,反应的部分数据如下表所示。下列说法正确的是
2SO3(g)ΔH<0是硫酸制造工业的基本反应。将2.0L密闭反应器置于常压下某恒温环境中,反应的部分数据如下表所示。下列说法正确的是
 2SO3(g)ΔH<0是硫酸制造工业的基本反应。将2.0L密闭反应器置于常压下某恒温环境中,反应的部分数据如下表所示。下列说法正确的是
2SO3(g)ΔH<0是硫酸制造工业的基本反应。将2.0L密闭反应器置于常压下某恒温环境中,反应的部分数据如下表所示。下列说法正确的是n/mol t/min | n(SO2) | n(O2) | n(SO3) |
0 | 0.100 | 0.060 | 0 |
4 | 0.056 | ||
8 | 0.016 | ||
10 | 0.088 |
A.该反应的平衡常数K=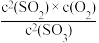 |
| B.工业上应选择高温高压条件进行生产 |
| C.平衡状态时,c(SO2)=0.006mol·L-1 |
| D.0~4min用O2表示的平均反应速率为5.5×10-3mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用尿素水解生成的 催化还原NO,是柴油机车辆尾气净化的主要方法。反应为
催化还原NO,是柴油机车辆尾气净化的主要方法。反应为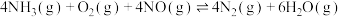 ,下列说法不正确的是
,下列说法不正确的是
 催化还原NO,是柴油机车辆尾气净化的主要方法。反应为
催化还原NO,是柴油机车辆尾气净化的主要方法。反应为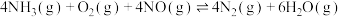 ,下列说法不正确的是
,下列说法不正确的是| A.恒温恒容,压强不变说明上述反应达到平衡 |
B.上述反应平衡常数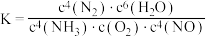 |
C.上述反应中消耗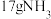 ,转移电子的数目为 ,转移电子的数目为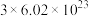 |
| D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气产生的污染越小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定量混合气体在密封容器中发生如下反应:xA(g)+yB(g) nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是
nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是
 nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是
nC(g)。达到平衡后测得A气体的浓度为0.5mol/L;保持恒温下将密闭容器的容积扩大1倍,再达到平衡时,测得A的浓度为0.3 mol/L。则下列叙述正确的是| A.x+y<n | B.该化学平衡向右移动 |
| C.B的转化率增大 | D.A的物质的量增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定温度下,向容积固定不变的密闭容器里充入a mol NO2,发生如下反应:2NO2(g) N2O4(g),达到平衡后,再向该容器内充入a mol NO2,达平衡后与原平衡比较错误的是
N2O4(g),达到平衡后,再向该容器内充入a mol NO2,达平衡后与原平衡比较错误的是
 N2O4(g),达到平衡后,再向该容器内充入a mol NO2,达平衡后与原平衡比较错误的是
N2O4(g),达到平衡后,再向该容器内充入a mol NO2,达平衡后与原平衡比较错误的是| A.平均相对分子质量增大 | B.NO2的转化率提高 |
| C.压强为原来的2倍 | D.颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列方案设计、现象和结论均正确且具有因果关系的是
| 选项 | 方案设计 | 现象和结论 |
| A | 室温下,用pH计测定0.1mol/L的 、 、 两种溶液的pH 两种溶液的pH |  溶液的pH较大,则电负性:F>Cl 溶液的pH较大,则电负性:F>Cl |
| B | 向盛有0.2mol/L 溶液的试管中加入0.1mol/L的 溶液的试管中加入0.1mol/L的 溶液 溶液 | 试管口出现红棕色气体,则 被 被 还原为 还原为 |
| C | 将注射器充满 气体,再往里推活塞压缩体积 气体,再往里推活塞压缩体积 | 气体颜色加深,则加压平衡向生成 气体的方向移动 气体的方向移动 |
| D | 2mL0.1mol·L⁻¹的 溶液中滴加2滴同浓度NaOH的溶液,再滴加4滴同浓度的 溶液中滴加2滴同浓度NaOH的溶液,再滴加4滴同浓度的 | 白色沉淀转化为红褐色沉淀,则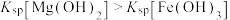 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下,反应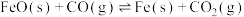 的平衡常数为1,在体积为2L的容器中充入1 mol CO、0.2 mol
的平衡常数为1,在体积为2L的容器中充入1 mol CO、0.2 mol 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是
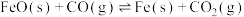 的平衡常数为1,在体积为2L的容器中充入1 mol CO、0.2 mol
的平衡常数为1,在体积为2L的容器中充入1 mol CO、0.2 mol 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是A.该反应的平衡常数的表达式为: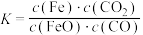 |
| B.CO的平衡转化率为20% |
C.达到平衡时再充入CO和 各0.2 mol,平衡不移动 各0.2 mol,平衡不移动 |
| D.升高温度,可以提高反应的活化能,正、逆反应速率均加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 时,
时,
 ,
,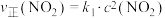 ,
,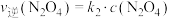 ,其中
,其中 、
、 只与温度有关,将一定量的
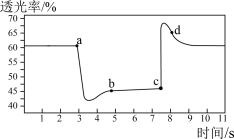
只与温度有关,将一定量的 充入注射器中,改变活塞位置,气体透光率随时间的变化如图所示(气体颜色越深,透光率越低),下列说法错误的是
充入注射器中,改变活塞位置,气体透光率随时间的变化如图所示(气体颜色越深,透光率越低),下列说法错误的是
 时,
时,
 ,
,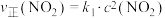 ,
,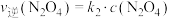 ,其中
,其中 、
、 只与温度有关,将一定量的
只与温度有关,将一定量的 充入注射器中,改变活塞位置,气体透光率随时间的变化如图所示(气体颜色越深,透光率越低),下列说法错误的是
充入注射器中,改变活塞位置,气体透光率随时间的变化如图所示(气体颜色越深,透光率越低),下列说法错误的是
A. 时, 时, |
B. 时, 时, ,则 ,则 |
C. 点 点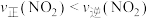 |
D.保持容积不变,再充入一定量 气体, 气体, 的平衡转化率变大 的平衡转化率变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某学习小组在容积固定为2 L的密闭容器内充入1 mol N2和3 mol H2合成NH3。恒温下开始反应,并用压力传感器测定压强如下表所示:
下列说法不正确 的是
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
| A.不断地将NH3液化并移走,有利于反应正向进行 |
| B.其它条件不变,在30 min时,若压缩容器的体积,N2的平衡转化率增大 |
| C.从反应开始到10 min时,v(NH3)=0.035 mol·L−1·min−1 |
| D.在30 min时,再加入0.5 mol N2、1.5 mol H2和2 mol NH3,平衡向逆反应方向移动 |
您最近一年使用:0次

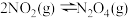 。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知:
。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知: 为无色气体)
为无色气体)

