名校
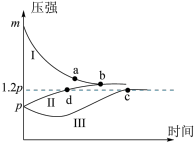
1 . 一定条件下,分别向体积为1L的密闭容器中充入表中所示的①、②、③三组反应气,发生反应:2X(g)+Y(g) Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
 Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2molX+1molY | 恒温 |
| ② | 1molZ | 恒温 |
| ③ | 1molZ | 绝热 |

| A.曲线I对应实验① | B.正反应为放热反应 |
| C.气体的总物质的量:nc=nd | D.b点平衡常数比c点平衡常数小 |
您最近一年使用:0次
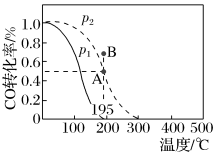
2 . 在20L的密闭容器中按物质的量之比为1:2充入CO和H2,发生反应 △H。测得CO的转化率随温度及压强的变化如图所示,p2和195℃时n(H2)随时间的变化如下表所示。下列说法不正确的是
△H。测得CO的转化率随温度及压强的变化如图所示,p2和195℃时n(H2)随时间的变化如下表所示。下列说法不正确的是
 △H。测得CO的转化率随温度及压强的变化如图所示,p2和195℃时n(H2)随时间的变化如下表所示。下列说法不正确的是
△H。测得CO的转化率随温度及压强的变化如图所示,p2和195℃时n(H2)随时间的变化如下表所示。下列说法不正确的是
| P2和195℃时n(H2) | ||||
 | 0 | 1 | 3 | 5 |
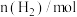 | 8 | 5 | 4 | 4 |
A. 和195℃时, 和195℃时,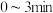 ,反应速率 ,反应速率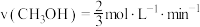 |
| B.p1<p2,△H<0 |
C.在 和195℃时,该反应的平衡常数为25 和195℃时,该反应的平衡常数为25 |
D.195℃、 时,在B点:v正>v逆 时,在B点:v正>v逆 |
您最近一年使用:0次
解题方法
3 . 下列图中的实验装置或操作表述合理的是
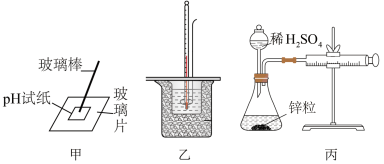



A.图甲:测定 溶液的 溶液的 |
B.图乙:测定稀盐酸和 溶液反应的中和热 溶液反应的中和热 |
C.图丙:测定锌粒与稀 反应的速率 反应的速率 |
| D.图丁:注射器活塞由Ⅱ推至Ⅰ处管内气体颜色变浅 |
您最近一年使用:0次
名校
解题方法
4 . 已知:反应反应2NH3(g) N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是

 N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
A.若保持容器体积不变,0~t1min内,N2的平均反应速率为 mol•L﹣1•min﹣1 mol•L﹣1•min﹣1 |
| B.若保持容器体积不变,该温度下,当N2和H2的分压比保持不变时,表明反应已达平衡 |
| C.若保持容器体积不变,t1min时,反应放出0.2akJ的热量 |
| D.t2min时,将容器体积迅速缩小一半并保持不变,N2的分压变化如图中曲线b所示 |
您最近一年使用:0次
名校
5 . 向 容器中充入
容器中充入 和
和 ,发生反应
,发生反应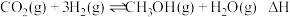 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中
体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中 关系如图Ⅱ所示。下列说法正确的是
关系如图Ⅱ所示。下列说法正确的是
 容器中充入
容器中充入 和
和 ,发生反应
,发生反应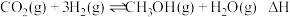 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中
体积分数如图Ⅰ所示,测得反应时逆反应速率与容器中 关系如图Ⅱ所示。下列说法正确的是
关系如图Ⅱ所示。下列说法正确的是
A. |
B.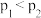 |
C.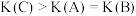 |
| D.图Ⅱ中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是d |
您最近一年使用:0次
2023-02-11更新
|
970次组卷
|
5卷引用:湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题
名校
6 . 反应
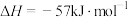 ,在温度为
,在温度为 、
、 时,平衡体系中
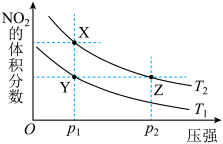
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是

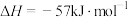 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
A. | B.X、Y两点的反应速率:X>Y |
| C.X、Z两点气体的颜色:X比Z浅 | D.X、Z两点气体的平均相对分子质量:X>Z |
您最近一年使用:0次
2023-02-10更新
|
506次组卷
|
6卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
7 . 我国政府承诺二氧化碳排放在2030年前达到峰值,2060年前实现碳中和,彰显作为大国的担当和责任。 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为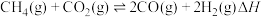 。回答下列问题:
。回答下列问题:
(1)已知:①
②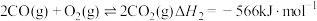
③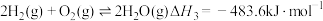
则
___________  。
。
(2)恒容密闭容器中可逆反应 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。
(3)容器容积为1L,控制 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
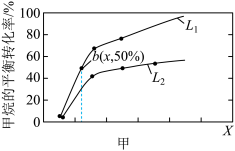
则 代表
代表___________ (填“温度”或“压强”):
___________  (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由:___________ ;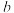 点反应的平衡常数为
点反应的平衡常数为___________ 。
(4)500℃下,将 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
由图乙可知,75min后 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为___________ ,原因是___________ 。
(5)①温度为 时,
时,
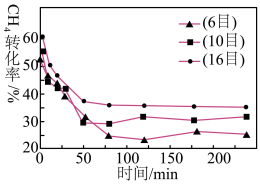
实验测得: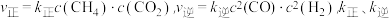 为速率常数。
为速率常数。 时,
时, =
=___________ (以 表示)。
表示)。
②当温度改变为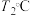 时,
时,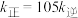 ,则
,则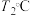 时平衡压强
时平衡压强___________  时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是___________ 。
 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为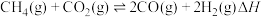 。回答下列问题:
。回答下列问题:(1)已知:①

②
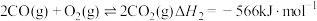
③
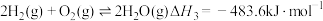
则

 。
。(2)恒容密闭容器中可逆反应
 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。A.单位时间内生成1mol 的同时消耗2molCO 的同时消耗2molCO |
| B.混合气体的密度不再改变 |
C.反应速率 |
| D.混合气体的平均相对分子质量不再改变 |
 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
则
 代表
代表
 (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由: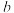 点反应的平衡常数为
点反应的平衡常数为(4)500℃下,将
 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
由图乙可知,75min后
 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为(5)①温度为
 时,
时,
实验测得:
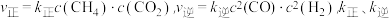 为速率常数。
为速率常数。 时,
时, =
= 表示)。
表示)。②当温度改变为
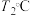 时,
时,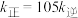 ,则
,则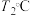 时平衡压强
时平衡压强 时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是
您最近一年使用:0次
2023-02-07更新
|
351次组卷
|
3卷引用:湖南省醴陵市第一中学2023届高三第六次月考化学试题
名校
解题方法
8 . 随着我国“碳达峰”、“碳中和”目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.以 和
和 为原料合成尿素:
为原料合成尿素: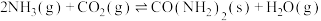
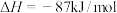 。
。
(1)有利于提高 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如图甲所示。
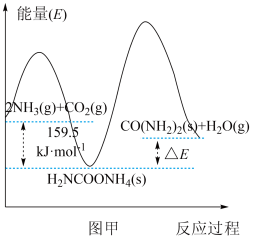
第一步: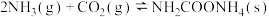

第二步: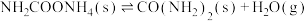

反应速率较快的是反应_______ (填“第一步”或“第二步”)。
Ⅱ.以和催化重整制备合成气: 。
。
(3)在密闭容器中通入物质的量均为0.2mol的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应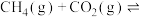
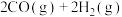 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
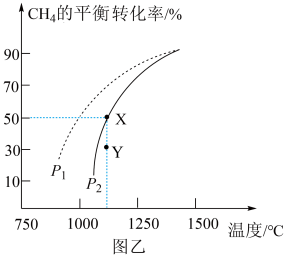
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是_______ (填标号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: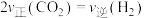 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H
②由图乙可知,压强
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则X点对应温度下的
,则X点对应温度下的
_______ (用含 的代数式表示)。
的代数式表示)。
Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为_______ ;该装置中使用的是_______ (填“阳”或“阴”)离子交换膜。
Ⅰ.以
 和
和 为原料合成尿素:
为原料合成尿素: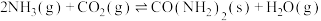
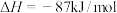 。
。(1)有利于提高
 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |

第一步:
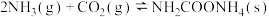

第二步:
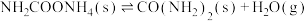

反应速率较快的是反应
Ⅱ.以和催化重整制备合成气:
 。
。(3)在密闭容器中通入物质的量均为0.2mol的
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应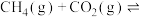
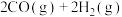 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
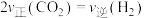 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H②由图乙可知,压强

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则X点对应温度下的
,则X点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为
您最近一年使用:0次
2023-02-06更新
|
342次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高三下学期月考卷(六)化学试题
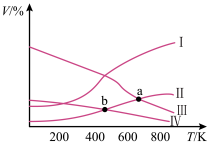
9 . 在密闭容器中:按CO2与H2的物质的量之比为1∶3进行投料,发生反应2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H<0,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(V%)如图所示,下列说法中正确的是
CH3CH2OH(g)+3H2O(g) △H<0,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(V%)如图所示,下列说法中正确的是
 CH3CH2OH(g)+3H2O(g) △H<0,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(V%)如图所示,下列说法中正确的是
CH3CH2OH(g)+3H2O(g) △H<0,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(V%)如图所示,下列说法中正确的是
| A.表示CH3CH2OH组分的曲线是Ⅳ |
| B.图中曲线交点a、b对应的上述反应平衡常数Ka>Kb |
| C.图中曲线交点a对应的CO2转化率为60% |
| D.若甲、乙两个密闭容器起始时的容积、温度及投料方式均相同,甲:恒温恒压,乙;恒温恒容,反应达平衡时CH3CH2OH产率:甲<乙 |
您最近一年使用:0次
2023-02-01更新
|
450次组卷
|
4卷引用:湖南省长沙市长郡梅溪湖中学2022-2023学年高二下学期期中考试化学试题
湖南省长沙市长郡梅溪湖中学2022-2023学年高二下学期期中考试化学试题湖南省张家界市慈利县第一中学2023-2024学年高二上学期第二次月考化学试题(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题15 化学平衡图像-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
10 . 一定温度和压强下,在两个容积均为1L的密闭容器中,充入一定量的A和B,发生反应: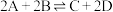 。相关反应数据如下表所示(已知在
。相关反应数据如下表所示(已知在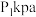 、
、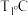 下,A、B、C、D都是气态)
下,A、B、C、D都是气态)
下列说法正确的是
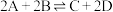 。相关反应数据如下表所示(已知在
。相关反应数据如下表所示(已知在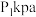 、
、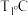 下,A、B、C、D都是气态)
下,A、B、C、D都是气态)| 容器编号 | 压强 | 温度 | 起始物质的量/mol | 10s时物质的量/mol | |
| A | B | C | |||
| Ⅰ | 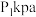 | 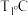 | 0.2 | 0.2 | 0.05 |
| Ⅱ | 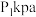 | 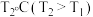 | 0.2 | 0.2 | 0.05 |
| Ⅲ |  | 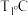 | 0.2 | 0.2 | 0.05 |
A.该反应的 |
| B.在容器Ⅲ中,A、B中至少有一种呈非气态 |
| C.10s时,容器Ⅱ中的反应一定处于平衡状态 |
D.若起始时,向容器II中充入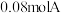 、 、 、 、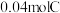 和 和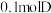 ,反应将向正反应方向进行 ,反应将向正反应方向进行 |
您最近一年使用:0次



