真题
解题方法
1 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH4(g)+CO2(g) 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1
b)CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
c)CH4(g) C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3
d)2CO(g) CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4
e)CO(g)+H2(g) H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=_______ (写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______ 。
A. 增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加
B. 移去部分C(s),反应c、d、e的平衡均向右移动
C. 加入反应a的催化剂,可提高CH4的平衡转化率
D. 降低反应温度,反应a~e的正、逆反应速率都减小
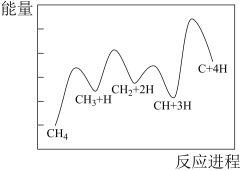
(3)一定条件下,CH4分解形成碳的反应历程如图所示。该历程分_______ 步进行,其中,第_______ 步的正反应活化能最大。
(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
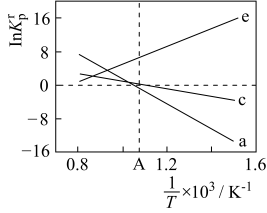
①反应a、c、e中,属于吸热反应的有_______ (填字母)。
②反应c的相对压力平衡常数表达式为K =
=_______ 。
③在图中A点对应温度下、原料组成为n(CO2):n(CH4)=1:1、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40kPa。计算CH4的平衡转化率,写出计算过程_______ 。
(5)CO2用途广泛,写出基于其物理性质的一种用途:_______ 。
a)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1b)CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2c)CH4(g)
 C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3d)2CO(g)
 CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4e)CO(g)+H2(g)
 H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5(1)根据盖斯定律,反应a的∆H1=
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有
A. 增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加
B. 移去部分C(s),反应c、d、e的平衡均向右移动
C. 加入反应a的催化剂,可提高CH4的平衡转化率
D. 降低反应温度,反应a~e的正、逆反应速率都减小
(3)一定条件下,CH4分解形成碳的反应历程如图所示。该历程分

(4)设K
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
①反应a、c、e中,属于吸热反应的有
②反应c的相对压力平衡常数表达式为K
 =
=③在图中A点对应温度下、原料组成为n(CO2):n(CH4)=1:1、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40kPa。计算CH4的平衡转化率,写出计算过程
(5)CO2用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
2021-06-11更新
|
13561次组卷
|
11卷引用:考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)2021年新高考广东化学高考真题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考向18 化学反应与能量变化-备战2022年高考化学一轮复习考点微专题2021年广东省高考化学试卷变式题11-21(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点23 化学平衡常数-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题
20-21高二下·浙江·期中
解题方法
2 . 尿素(NH2CONH2)又称碳酰胺,是含氮量最高的氮肥。工业上利用二氧化碳和氨气在一定条件下合成尿素,涉及的反应如下:
反应I:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵)△H1=-272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵)△H1=-272kJ·mol-1
反应II:H2NCOONH4(s) NH2CONH2(s)+H2O(g)△H2=+138kJ·mol-1
NH2CONH2(s)+H2O(g)△H2=+138kJ·mol-1
请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式___ 。该反应自发进行的条件是___ (填“低温”、“高温”或“任意条件”)。
(2)为提高反应I中NH3的反应速率和平衡转化率,可采取的措施是___ (填标号)。
A.升高温度 B.增大压强
C.增大CO2的浓度 D.使用催化剂
(3)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式___ 。
(4)写出反应I的平衡常数表达式K=___ 。
(5)工业上含尿素的废水需经处理后才能排放,一种利用电化学方式降解尿素装置示意图如图,写出尿素被降解的电极反应式___ 。

反应I:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵)△H1=-272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵)△H1=-272kJ·mol-1反应II:H2NCOONH4(s)
 NH2CONH2(s)+H2O(g)△H2=+138kJ·mol-1
NH2CONH2(s)+H2O(g)△H2=+138kJ·mol-1请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式
(2)为提高反应I中NH3的反应速率和平衡转化率,可采取的措施是
A.升高温度 B.增大压强
C.增大CO2的浓度 D.使用催化剂
(3)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式
(4)写出反应I的平衡常数表达式K=
(5)工业上含尿素的废水需经处理后才能排放,一种利用电化学方式降解尿素装置示意图如图,写出尿素被降解的电极反应式

您最近一年使用:0次
19-20高二·浙江·期中
3 . 碳单质在工业上有多种用途,用活性炭还原处理氮氧化物,有关反应为:C(s)+ 2NO(g) N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式___________ 。
(2)在恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
①结合表中数据,判断该反应的△H___________ 0 (填“>”或“<”),理由是___________ 。
②判断该反应达到平衡的依据是___________ (填字母)。
a、容器内气体密度恒定 b、容器内气体平均摩尔质量恒定
c、容器内N2和CO2物质的量之比恒定 d、 2v正(NO)=v逆(N2)
(3) 700℃时,若向4 L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+ 2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+ 2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。

①0~10 min内的CO2平均反应速率v=___________ 。
②图中A点v正___________ v逆 (填“>”“<”或“=”)。
③第10 min时,外界改变的条件可能是___________ (填字母) 。
a、加催化剂 b、增大C的物质的量 c、加压 d、升温
 N2(g)+CO2(g)。
N2(g)+CO2(g)。(1)写出上述反应的平衡常数表达式
(2)在恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.40 | 0.10 |
①结合表中数据,判断该反应的△H
②判断该反应达到平衡的依据是
a、容器内气体密度恒定 b、容器内气体平均摩尔质量恒定
c、容器内N2和CO2物质的量之比恒定 d、 2v正(NO)=v逆(N2)
(3) 700℃时,若向4 L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+ 2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+ 2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
①0~10 min内的CO2平均反应速率v=
②图中A点v正
③第10 min时,外界改变的条件可能是
a、加催化剂 b、增大C的物质的量 c、加压 d、升温
您最近一年使用:0次



