2024高三下·全国·专题练习
1 . 二甲醚(DME)在制药、燃料、农药等化学工业中有许多独特的用途。工业上常用合成气制备二甲醚的主要原理如下:①CO(g)+2H2(g)⇌CH3OH(g) ΔH1<0
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2<0
③CO(g)+H2O(g)⇌H2(g)+CO2(g) ΔH3<0
在催化剂作用下,发生上述3个反应,CO的转化率、CH3OH和CO2的产率和随温度变化关系如图1所示。总压分别为100kPa、10kPa时,平衡体系中CO和CH3OCH3(g)的物质的量分数随温度变化关系如图2所示
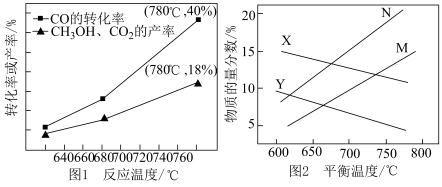
回答下列问题:
(1)图1中CO的转化率随温度升高而上升的原因是_______ 。
(2)图1中780℃时,CH3OCH3的选择性为_______ 。(CH3OCH3选择性= )
)
(3)能提高CH3OCH3选择性的最关键因素是_______ 。
(4)100kPa时,CO和CH3OCH3的物质的量分数随温度变化关系的曲线分别是_______ 、_______ 。
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2<0
③CO(g)+H2O(g)⇌H2(g)+CO2(g) ΔH3<0
在催化剂作用下,发生上述3个反应,CO的转化率、CH3OH和CO2的产率和随温度变化关系如图1所示。总压分别为100kPa、10kPa时,平衡体系中CO和CH3OCH3(g)的物质的量分数随温度变化关系如图2所示

回答下列问题:
(1)图1中CO的转化率随温度升高而上升的原因是
(2)图1中780℃时,CH3OCH3的选择性为
 )
)(3)能提高CH3OCH3选择性的最关键因素是
(4)100kPa时,CO和CH3OCH3的物质的量分数随温度变化关系的曲线分别是
您最近一年使用:0次
解题方法
2 . 对于反应N2(g)+3H2(g) 2NH3(g) ΔH<0,如何根据下列图像比较T1、T2的大小?
2NH3(g) ΔH<0,如何根据下列图像比较T1、T2的大小?_____
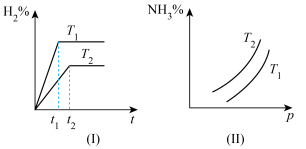
 2NH3(g) ΔH<0,如何根据下列图像比较T1、T2的大小?
2NH3(g) ΔH<0,如何根据下列图像比较T1、T2的大小?
您最近一年使用:0次
3 . “先拐先平”原则
在化学平衡图像中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高(如图1)或表示的压强较大(如图2)[仍以aA(g)+bB(g) cC(g)为例]。
cC(g)为例]。
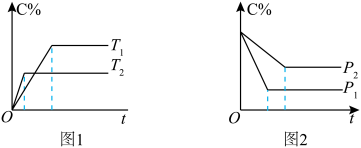
根据图像回答下列问题:
(1)图1中,温度T1、T2的大小关系是___________ ,温度升高,C%(C的含量)的变化是___________ ,化学平衡___________ 移动,正反应是___________ 反应。
(2)图2中,压强p1、p2的大小关系是___________ ,压强增大,C%(C的含量)的变化是___________ ,化学平衡___________ 移动,a+b___________ c。
在化学平衡图像中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高(如图1)或表示的压强较大(如图2)[仍以aA(g)+bB(g)
 cC(g)为例]。
cC(g)为例]。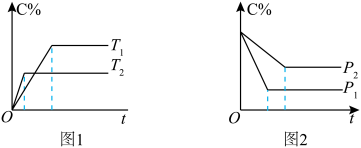
根据图像回答下列问题:
(1)图1中,温度T1、T2的大小关系是
(2)图2中,压强p1、p2的大小关系是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)⇌xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。
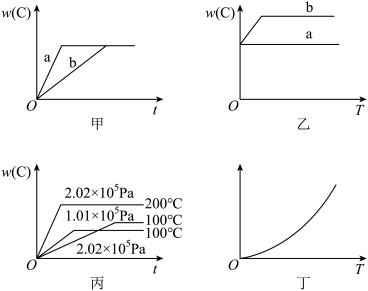
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则曲线___________ 表示无催化剂时的情况,原因是___________ 。
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下充入氦气后的情况,则曲线___________ 表示恒温恒容时的情况,原因是___________ 。
(3)根据丙图可以判断该可逆反应的正反应是___________ (填“放”或“吸”)热反应,化学计量数x的值___________ (填“大于”或“小于”)2。
(4)丁图表示在某固定容积的密闭容器中上述可逆反应达到平衡后某物理量随温度(T)的变化情况,根据你的理解,丁图的纵坐标可能是___________ ,原因为___________ 。

(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则曲线
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下充入氦气后的情况,则曲线
(3)根据丙图可以判断该可逆反应的正反应是
(4)丁图表示在某固定容积的密闭容器中上述可逆反应达到平衡后某物理量随温度(T)的变化情况,根据你的理解,丁图的纵坐标可能是
您最近一年使用:0次
2023高三·全国·专题练习
5 . 回答下列问题
(1)已知合成氨反应: N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ=
NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ= ,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=
,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=___________ (用含w的最简式表示)。
(2)某科研小组向一恒容密闭容器中通入2 mol CH4、2 mol CO2,控制适当条件使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示

①X___________ (填“能”或“不能”)表示平衡体系中CH4的体积分数;p1、p2的大小关系为___________ ,b点浓度商Qc与对应温度下的平衡常数K相比,较大的是___________
②若容器容积为2 L,a点时c(CH4)=0.4 mol·L-1,则相应温度下的平衡常数K=___________
(1)已知合成氨反应:
 N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ=
NH3(g) ΔH=-46.2 kJ·mol-1,标准平衡常数Kθ= ,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=
,其中pθ为标准压强,p(NH3)、p(N2)、p(H2)为各组分的平衡分压,如p(NH3)=x(NH3)p,p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。若往一密闭容器中加入的N2、H2起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则Kθ=(2)某科研小组向一恒容密闭容器中通入2 mol CH4、2 mol CO2,控制适当条件使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
2CO(g)+2H2(g) ΔH=+247 kJ·mol-1,测出CH4的某个平衡物理量X随着温度、压强的变化如图所示
①X
②若容器容积为2 L,a点时c(CH4)=0.4 mol·L-1,则相应温度下的平衡常数K=
您最近一年使用:0次
22-23高二上·新疆哈密·期末
解题方法
6 . 工业上合成氨是在一定条件下进行反应:N2(g)+3H2(g)  2NH3(g),ΔH=-92.4kJ·mol-1,其部分工艺流程如图所示。
2NH3(g),ΔH=-92.4kJ·mol-1,其部分工艺流程如图所示。
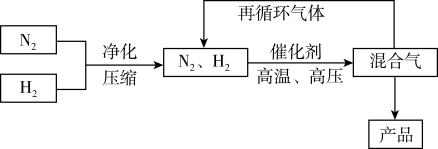
反应体系中各组分的部分性质如下表所示:
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=___________ 。温度升高,K值___________ (填“增大”“减小”或“不变”)。
(2)K值越大,表明___________(填序号)。
(3)对于合成氨反应而言,如图有关图像一定正确的是___________ (填字母)。
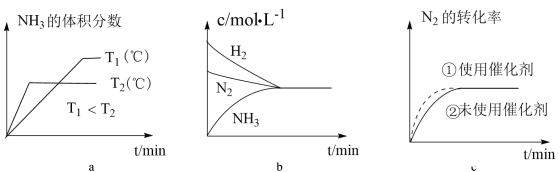
 2NH3(g),ΔH=-92.4kJ·mol-1,其部分工艺流程如图所示。
2NH3(g),ΔH=-92.4kJ·mol-1,其部分工艺流程如图所示。
反应体系中各组分的部分性质如下表所示:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点/℃ | -210.01 | -259.23 | -77.74 |
| 沸点/℃ | -195.79 | -252.77 | -33.42 |
(1)写出该反应的化学平衡常数表达式:K=
(2)K值越大,表明___________(填序号)。
| A.其他条件相同时N2的转化率越高 |
| B.其他条件相同时NH3的产率越高 |
| C.原料中N2的含量越高 |
| D.化学反应速率越快 |

您最近一年使用:0次
2023高三·全国·专题练习
7 . 二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1) CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=_______ 。当反应达到平衡时,若增大压强,则n(C2H4)_______ (填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2):n(H2O)=1:3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
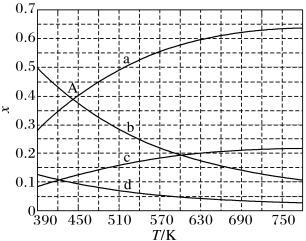
图中,表示C2H4、CO2变化的曲线分别是_______ 、_______ 。CO2催化加氢合成C2H4反应的△H_______ 0(填“大于”或“小于”)。
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数Kp=_______ (MPa)-3 (列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H4、C3H5、C4H3等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当_______ 。
(1) CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=
(2)理论计算表明,原料初始组成n(CO2):n(H2O)=1:3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示C2H4、CO2变化的曲线分别是
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数Kp=
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H4、C3H5、C4H3等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
您最近一年使用:0次
8 . 回答下列问题:
Ⅰ.一定条件下,在容积为 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
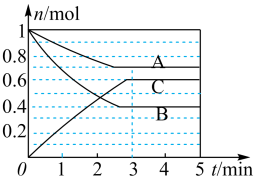
(1)达到平衡后加压,C的含量_______ (填写“变大”“变小”或“不变”)。
(2)该反应的反应速率v随时间t的关系如图所示。
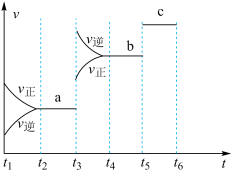
①根据图判断,在 时刻改变的外界条件是
时刻改变的外界条件是_______ 。
②a、b、c对应的平衡状态中,A的转化率最大的是状态_______ 。
Ⅱ.在密闭容器中充入一定量的 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。

(3)该反应的逆反应是_______ (填“吸热反应”或“放热反应”)。
(4)N点 的体积分数是
的体积分数是_______ 。
(5)M点对应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅰ.一定条件下,在容积为
 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
(1)达到平衡后加压,C的含量
(2)该反应的反应速率v随时间t的关系如图所示。

①根据图判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②a、b、c对应的平衡状态中,A的转化率最大的是状态
Ⅱ.在密闭容器中充入一定量的
 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)该反应的逆反应是
(4)N点
 的体积分数是
的体积分数是(5)M点对应的平衡常数

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
20-21高二上·云南曲靖·阶段练习
9 . 利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)⇌5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5 固体的2L恒容密闭容器中通入2mol CO,测得CO的体积分数 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
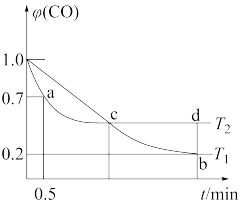
(1)此反应的平衡常数表达式____________ 。
(2)到a点时表示的化学反应速率v(CO)=____________ 。
(3)b点时CO的转化率____________ 。
(4)Kb_______ Kd(填“大于”“小于”或“等于”),原因是_______________ 。
(5)此反应的ΔH________ 0(填“大于”“小于”或“等于”)。
 (CO)随时间t变化曲线如图。
(CO)随时间t变化曲线如图。
(1)此反应的平衡常数表达式
(2)到a点时表示的化学反应速率v(CO)=
(3)b点时CO的转化率
(4)Kb
(5)此反应的ΔH
您最近一年使用:0次
名校
10 . I.可逆反应∶mA(g)+nB(g)⇌pC(g)+qD(s) ∆H,试根据图回答∶
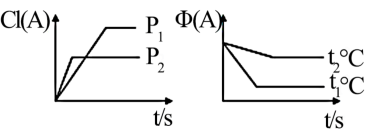
[A的转化率(%)表示为α(A)、A的含量(%)表示为φ(A)]
(1)压强P1_______ P2(填“>”,“<”或“=”下同)
(2)计量数(m+n)_______ (p)
(3)温度t1℃_______ t2℃
(4)ΔH_______ 0
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
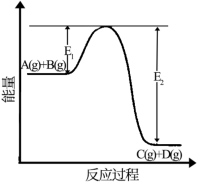
(5)该反应是_______ 反应(填“吸热”,“放热”);
(6)当反应达到平衡时,只升高温度,化学平衡向_______ (填“正反应方向”或“逆反应方向”)移动。
(7)反应体系中加入催化剂该反应的反应热_______ (填增大”“减小”“不变”);

[A的转化率(%)表示为α(A)、A的含量(%)表示为φ(A)]
(1)压强P1
(2)计量数(m+n)
(3)温度t1℃
(4)ΔH
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(5)该反应是
(6)当反应达到平衡时,只升高温度,化学平衡向
(7)反应体系中加入催化剂该反应的反应热
您最近一年使用:0次
2021-09-15更新
|
567次组卷
|
4卷引用:新疆乌鲁木齐市第二十中学2019-2020学年高二上学期期中考试化学试题
新疆乌鲁木齐市第二十中学2019-2020学年高二上学期期中考试化学试题安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)



