1 . 在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如表,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是

 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是| 容器 | n(CO2)/mol | n(C)/mol | n(CO)/mol |
| 甲 | 0.1 | 0.3 | 0 |
| 乙 | 0 | 0 | 0.4 |

| A.曲线Ⅰ对应的是甲容器 |
| B.a、b两点所处状态的压强大小关系:9pa>14pb |
C.c点:CO的体积分数>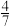 |
| D.900K时,若起始向容器乙中加入CO、CO2、C各1mol,则v(正)>v(逆) |
您最近一年使用:0次
2021-12-27更新
|
2466次组卷
|
15卷引用:上海市金山区2022届高三一模化学试题
上海市金山区2022届高三一模化学试题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)江西省宜春市奉新县第一中学2021-2022学年高二下学期第一次月考化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题山东省青岛第二中学2022-2023学年高二上学期期中考试化学试题辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题湖南省攸县第二中学2022-2023学年高三第六次月考化学试题湖南省攸县第三中学2022-2023学年高三第六次月考化学试题湖南省常德市第一中学2023届高三第五次月考化学试题山东省滕州市第一中学2023-2024学年高二上学期10月月考化学试题河南省周口恒大中学2023-2024学年高二上学期9月月考化学试题安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
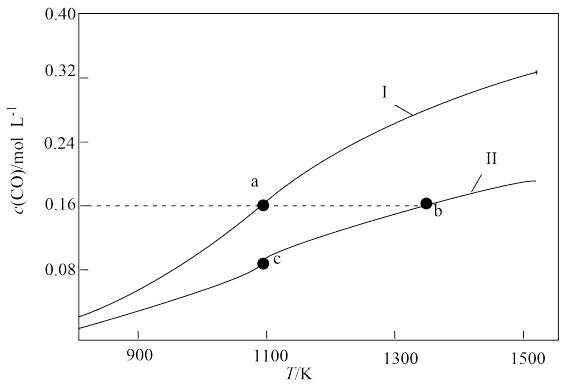
2 . 体积均为1.0L的甲、乙两个恒容密闭容器,向甲中加入0.1molCO2和0.3mol碳粉,向乙中加入0.4molCO,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
| A.曲线II对应的是乙容器 |
| B.a、b两点对应平衡体系中的压强之比:pa:pb<14:9 |
C.b点对应的平衡体系中,CO的体积分数小于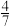 |
| D.900K时,起始时向容器乙中加入CO、CO2、碳粉各1mol,此时v正﹥v逆 |
您最近一年使用:0次
2020-12-23更新
|
1864次组卷
|
3卷引用:安徽省舒城中学2020-2021学年高二上学期第三次月考化学试题
解题方法
3 . 丙烯是一种重要的化工原料,可以在催化剂作用下由丙烷脱氢制备。反应原理为:
热解反应:
副反应:
请回答:
(1)已知相关键能的数据如下表所示,则:
①热解反应的
_______  。
。
②裂解气中存在浓度不低的 ,从结构角度解释度原因
,从结构角度解释度原因_______ 。
③裂解反应的选择性随温度变化如图所示,则丙烷裂解应控制温度在_______ 。
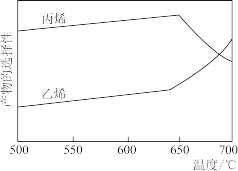
(2)恒定不同压强( 、
、 ),热解气中丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
),热解气中丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
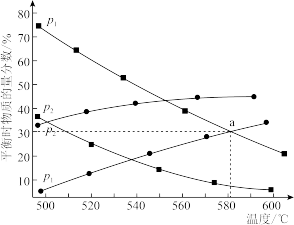
①压强:
_______  (填“>”或“<”)。
(填“>”或“<”)。
②若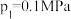 ,则
,则 点对应温度下,热解反应的平衡常数
点对应温度下,热解反应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)向容器中通入一定量 进行丙烷氧化脱氢,可提高产物丙烯的选择性。
进行丙烷氧化脱氢,可提高产物丙烯的选择性。
①通 的好处是
的好处是_______ 。
②反应体系中会有 检出,是烃燃烧产物
检出,是烃燃烧产物 与原料气中残留的
与原料气中残留的 反应而成。研究表明在
反应而成。研究表明在 催化下,
催化下, 转化为
转化为 经两步完成,用方程式表示该转变过程
经两步完成,用方程式表示该转变过程_______ 、_______ 。
热解反应:

副反应:

请回答:
(1)已知相关键能的数据如下表所示,则:
| 化学键 |  |  |  |  |
键能/ | 348 | 615 | 413 | 436 |
①热解反应的

 。
。②裂解气中存在浓度不低的
 ,从结构角度解释度原因
,从结构角度解释度原因③裂解反应的选择性随温度变化如图所示,则丙烷裂解应控制温度在

(2)恒定不同压强(
 、
、 ),热解气中丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
),热解气中丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
①压强:

 (填“>”或“<”)。
(填“>”或“<”)。②若
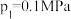 ,则
,则 点对应温度下,热解反应的平衡常数
点对应温度下,热解反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(3)向容器中通入一定量
 进行丙烷氧化脱氢,可提高产物丙烯的选择性。
进行丙烷氧化脱氢,可提高产物丙烯的选择性。①通
 的好处是
的好处是②反应体系中会有
 检出,是烃燃烧产物
检出,是烃燃烧产物 与原料气中残留的
与原料气中残留的 反应而成。研究表明在
反应而成。研究表明在 催化下,
催化下, 转化为
转化为 经两步完成,用方程式表示该转变过程
经两步完成,用方程式表示该转变过程
您最近一年使用:0次
名校
解题方法
4 . 萘类物质的加成反应,可以合成多种环状结构的异构体,并在工业中有重要应用,利用1-甲基萘(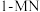 )制备四氢萘类物质(
)制备四氢萘类物质( ,包括
,包括 和
和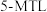 )。反应过程中伴有生成十氢萘(
)。反应过程中伴有生成十氢萘(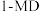 )的副反应,涉及反应如图:
)的副反应,涉及反应如图:
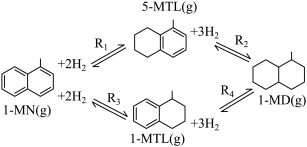
请回答下列问题:
(1)已知一定条件下反应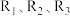 的焓变分别为
的焓变分别为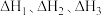 ,则反应
,则反应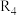 的焓变
的焓变
______ (用含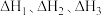 的代数式表示)。
的代数式表示)。
(2)根据 和
和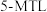 的结构及命名方式,
的结构及命名方式, 和
和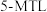 的一种同分异构体
的一种同分异构体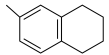 的名称为
的名称为______  。
。
(3)四个平衡体系的平衡常数与温度的关系如图所示。
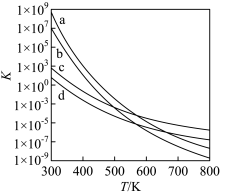
①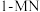 ,
, ,
,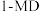 中最稳定的是
中最稳定的是______ 。
②不考虑生成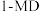 ,从反应进行程度上考虑,利于生成
,从反应进行程度上考虑,利于生成 的条件是
的条件是______ 。
③若曲线c、d分别代表反应 、
、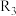 的平衡常数随温度的变化,则表示反应
的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的曲线为
的平衡常数随温度变化的曲线为______ 。
(4)某温度下,将一定量的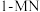 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
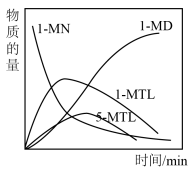
在此温度下,如何更多的得到
______ 。
a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多 时,及时分离出
时,及时分离出
(5) 时,在体积恒定的密闭容器中投入一定量的
时,在体积恒定的密闭容器中投入一定量的 ,假定只发生
,假定只发生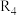 过程,
过程, 足量,且反应过程中氢气的浓度恒定为
足量,且反应过程中氢气的浓度恒定为 ,当
,当 的转化率为a时,反应的平衡常数为
的转化率为a时,反应的平衡常数为______ 。
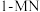 )制备四氢萘类物质(
)制备四氢萘类物质( ,包括
,包括 和
和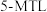 )。反应过程中伴有生成十氢萘(
)。反应过程中伴有生成十氢萘(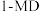 )的副反应,涉及反应如图:
)的副反应,涉及反应如图:
请回答下列问题:
(1)已知一定条件下反应
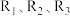 的焓变分别为
的焓变分别为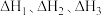 ,则反应
,则反应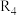 的焓变
的焓变
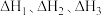 的代数式表示)。
的代数式表示)。(2)根据
 和
和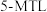 的结构及命名方式,
的结构及命名方式, 和
和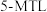 的一种同分异构体
的一种同分异构体 的名称为
的名称为 。
。(3)四个平衡体系的平衡常数与温度的关系如图所示。

①
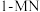 ,
, ,
,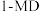 中最稳定的是
中最稳定的是②不考虑生成
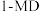 ,从反应进行程度上考虑,利于生成
,从反应进行程度上考虑,利于生成 的条件是
的条件是③若曲线c、d分别代表反应
 、
、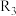 的平衡常数随温度的变化,则表示反应
的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的曲线为
的平衡常数随温度变化的曲线为(4)某温度下,将一定量的
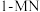 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如图乙所示。
在此温度下,如何更多的得到

a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多
 时,及时分离出
时,及时分离出
(5)
 时,在体积恒定的密闭容器中投入一定量的
时,在体积恒定的密闭容器中投入一定量的 ,假定只发生
,假定只发生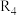 过程,
过程, 足量,且反应过程中氢气的浓度恒定为
足量,且反应过程中氢气的浓度恒定为 ,当
,当 的转化率为a时,反应的平衡常数为
的转化率为a时,反应的平衡常数为
您最近一年使用:0次
2023-12-08更新
|
401次组卷
|
2卷引用:湖北省十一校2023-2024学年高三上学期第一次联考化学试题
解题方法
5 . 二氧化碳加氢制甲烷过程中的主要反应为
Ⅰ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1<0
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2>0
Ⅲ.2CO(g)+2H2(g)=CO2(g)+CH4(g) △H3
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,在催化剂作用下反应相同时间所测得的CO2平衡转化率、CO2实际转化率随温度的变化如图2所示。CH4的选择性可表示为 ×100%。
×100%。
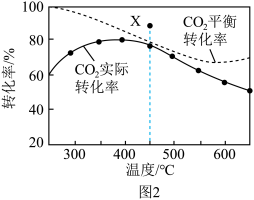
(1)各物质的相对能量如图1所示,△H3=______ kJ•mol-1,平衡时CH4的选择性随着温度的升高______ ,用该催化剂催化二氧化碳反应的最佳温度为______ ,450℃时,使CO2平衡转化率达到X点的值,可以采用的措施为_______ (写出一条)。
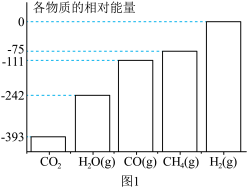
(2)在密闭容器中,1.01×105Pa,CO2和H2的起始物质的量分别为1mol和4mol,平衡后反应体系中各物质的物质的量随温度的变化如图3所示,图中表示CH4的物质的量的曲线为______ 。在505℃,反应Ⅱ的平衡常数K=______ 。(保留两位有效数字)
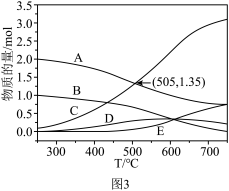
(3)CeO2催化CO2与H2转化为CH4的机理如图4所示。反应体系中Ce呈现______ 种价态,催化剂中掺入少量CaO,用Ca2+替代CeO2结构中部分Ce4+形成CaxCe1-xOy,可提高催化效率的原因是_______ 。

Ⅰ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1<0
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2>0
Ⅲ.2CO(g)+2H2(g)=CO2(g)+CH4(g) △H3
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,在催化剂作用下反应相同时间所测得的CO2平衡转化率、CO2实际转化率随温度的变化如图2所示。CH4的选择性可表示为
 ×100%。
×100%。
(1)各物质的相对能量如图1所示,△H3=

(2)在密闭容器中,1.01×105Pa,CO2和H2的起始物质的量分别为1mol和4mol,平衡后反应体系中各物质的物质的量随温度的变化如图3所示,图中表示CH4的物质的量的曲线为

(3)CeO2催化CO2与H2转化为CH4的机理如图4所示。反应体系中Ce呈现

您最近一年使用:0次
名校
6 . 恒容条件下,1 mol SiHCl3发生如下反应:2SiHCl3(g) SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是

 SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
| A.该反应为放热反应,v正,a<v逆,b |
| B.T1 K时平衡体系中可通过移走SiCl4提高SiHCl3的转化率 |
| C.当反应进行到a处时,v正/v逆=16/9 |
| D.T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大 |
您最近一年使用:0次
2019-02-20更新
|
1845次组卷
|
2卷引用:【市级联考】江苏省泰州市2019届高三上学期期末考试化学试题
名校
7 . 在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s) 2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

 2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
| A.该反应的ΔH>0、ΔS<0 |
| B.体系的总压强p:p(Ⅰ)>p(Ⅲ) |
| C.平衡常数:K(Ⅰ)>K(Ⅱ) |
| D.T1K时,Ⅳ点所处的状态中v(正)<v(逆) |
您最近一年使用:0次
2016-11-15更新
|
1393次组卷
|
8卷引用:2016-2017学年山西省太原五中高二上10月月考化学卷



