名校
1 . 运用相关化学知识进行判断,下列结论错误的是
| A.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ·mol-11能自发进行,是因为体系有自发地向混乱度增大的方向转变的倾向。 |
| B.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应可以加快反应速率。 |
| C.NH4F水溶液中含有HF,因此NH4F溶液不能存放在玻璃试剂瓶中。 |
| D.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=a kJ·mol-1,HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)ΔH=b kJ·mol-1,因醋酸电离吸热,所以a>b |
您最近一年使用:0次
2020-02-11更新
|
312次组卷
|
5卷引用:本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
(已下线)本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)江西省南昌市第二中学2019-2020学年高二上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——影响化学反应速率的因素(强化练习)江西省南昌市南昌县莲塘第三中学2020-2021学年高二上学期第二次月考化学试题江西省赣州市南康中学、平川中学、信丰中学2019—2020学年高二上学期12月月考试题化学
11-12高二上·江西新余·期中
名校
2 . 下列变化过程中,ΔS <0的是
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl |
| C.干冰的升华 | D.CaCO3(s)分解为CaO(s)和CO2(g) |
您最近一年使用:0次
2019-12-12更新
|
553次组卷
|
29卷引用:2018-2019学年鲁科版高中化学选修四:第2章检测题
2018-2019学年鲁科版高中化学选修四:第2章检测题(已下线)2011-2012学年浙江临海市白云高级中学高二下学期期中考试化学卷(已下线)2012-2013学年福建福清东张中学高二上学期期中考试理科化学试卷(已下线)2013-2014学年福建省长乐二中等五校高二上学期期中考试化学试卷2015-2016学年广西南宁市上林中学高二上学期期末化学试卷天津市红桥区2017-2018学年高二上学期期中考试化学试题山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题河北省承德一中2017-2018学年高二第二次月考化学试卷天津市静海区独流中学等四校2019-2020学年高二10月联考化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第三节 化学反应的方向 教材帮苏教2020版选择性必修1专题2第二单元 化学反应的方向与限度课后习题(已下线)2011-2012学年江西省新余九中高二上学期期中考试化学试卷(已下线)2011-2012学年浙江省嘉兴八校高二下学期期中联考化学试卷(已下线)2011-2012学年浙江省温州四中高二下学期期中考试化学试卷(已下线)2012-2013学年浙江省桐乡一中高二下学期期中考试化学试卷(已下线)2013-2014学年江苏省常州市四校高二期中考试化学试卷2016-2017学年浙江省慈溪市高二上学期期中化学试卷浙江省金华十校2017-2018学年高二上学期期末调研考试化学试题吉林省延边朝鲜族自治州汪清县第四中学2019-2020学年高二上学期第二次阶段考试化学试题浙江省金华市方格外国语学校2019-2020学年高二上学期12月月考化学试题黑龙江省大庆市东风中学2020-2021学年高二上学期10月月考化学试题新疆伊犁奎屯市第一高级中学2020-2021学年高二上学期期末考试化学试题云南省弥勒市第二中学2020-2021学年高二下学期期中考试化学试题江苏省淮安市涟水县第一中学2021-2022学年高二下学期第一次阶段检测化学试题湖南师范大学附属中学2019-2020学年高二上学期第一次月考化学试题江苏省无锡市太湖高级中学2022-2023学年高二下学期期中考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题广东省佛山市顺德区罗定邦中学2023-2024学年高二上学期期中考试化学试题
9-10高二下·浙江台州·阶段练习
名校
3 . 碳铵(NH4HCO3)在室温下就能自发地分解产生氨气,下列有关说法中正确的是:
| A.碳铵分解是因为生成了易挥发的气体,使体系的熵增大 | B.碳铵分解是因为外界给予了能量 |
| C.碳铵分解是吸热反应,根据焓判据,不能自发分解 | D.碳酸盐都不稳定,都能自发分解 |
您最近一年使用:0次
2019-09-30更新
|
204次组卷
|
15卷引用:第02章 化学反应速率和化学平衡(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
(已下线)第02章 化学反应速率和化学平衡(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)浙江省临海市白云中学2009—2010学年度高二下学期第一次月考化学试题(已下线)2012年人教版高中化学选修4 2.4化学反应进行的方向练习卷(已下线)同步君 选修4 第2章 第4节 化学反应进行的方向2016-2017学年河南省漯河中学高二上第一次月考化学卷河南省安阳市第三十六中学2017-2018学年高二上学期第二次月考化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第四节 化学反应进行的方向 化学反应进行的方向(已下线)2018年9月25日 《每日一题》人教选修4-自发过程与自发反应湖南怀化中方县一中2019-2020学年高二9月月考化学试卷内蒙古自治区通辽市开鲁县第一中学2019-2020学年高一下学期期末考试化学试题(已下线)2.2.1 化学反应的方向(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)作业(九) 化学反应的方向贵州省黔东南苗族侗族自治州天柱县第二中学2019-2020学年高二上学期期末考试化学试题西藏自治区日喀则市第三高级中学2019-2020学年高二上学期期末考试化学(理)试题福建省建瓯市芝华中学2020-2021学年高二上学期期中考试化学(选考班)试题
名校
4 . 自由能的变化(ΔG)是反应方向判断的复合判据:ΔG=ΔH-TΔS,ΔG<0时,反应正向自发进行。已知某化学反应其ΔH=-122 kJ·mol-1,ΔS=231 J·mol-1·K-1,则此反应在下列哪种情况下可自发进行 ( )。
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |
您最近一年使用:0次
2019-08-13更新
|
443次组卷
|
10卷引用:2020年春季人教版高中化学选修4第二章《化学反应速率和化学平衡》测试卷
2020年春季人教版高中化学选修4第二章《化学反应速率和化学平衡》测试卷陕西省渭南三贤中学2019-2020学年高二上学期期中考试化学试题(已下线)2.4+化学反应进行的方向-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)广东省清远市四校联盟2022-2023学年高二上学期期中考试化学试题甘肃省兰州第一中学2022-2023学年高二上学期期末考试化学试题新疆自治区生产建设兵团第一师高级中学2018-2019学年高二上学期第二次月考化学试题贵州省施秉县一中2019-2020学年高二上学期期末考试化学试题福建省永安市第一中学2020-2021学年高二上学期第一次月考化学试题江苏省淮安市涟水县第一中学2022届高三第一次阶段检测化学试卷黑龙江省鹤岗市第三中学2023-2024学年高二上学期10月月考化学试题
名校
5 . 下列叙述中正确的是
| A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B.常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023 |
| C.工业制粗硅2C(s)+SiO2(s)===Si(s)+2CO(g),室温下不能自发进行,则△H>0 |
| D.稀盐酸和稀氢氧化钠反应的中和热为-57.3 kJ•mol-1,则稀醋酸和稀氨水反应的中和热也为-57.3kJ·mol-1 |
您最近一年使用:0次
2019-07-01更新
|
937次组卷
|
7卷引用:本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
名校
6 . 下列关于化学反应方向及其判据的说法错误的是( )
| A.1mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] |
| B.放热反应都可以自发进行,而吸热反应不能自发进行 |
| C.2KClO3(s)=2KCl(s)+3O2(g)△H>0能否自发进行与温度有关 |
| D.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
您最近一年使用:0次
2019-03-26更新
|
1678次组卷
|
24卷引用:第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)
(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)河北省邯郸市第二中学2017-2018学年高二上学期期中考试化学试题【校级联考】安徽省滁州市民办高中2018-2019学年高二上学期第三次月考化学试题【市级联考】陕西省咸阳市2019届高三下学期第一次模拟考试化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)河北省新乐市第一中学2020届高三上学期11月月考化学试题河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第1节 化学反应的方向高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第三节 化学反应的方向江西省南昌市第二中学2020-2021学年高二上学期期中考试化学试题四川省成都市简阳市阳安中学2020-2021学年高二上学期期中考试化学试题内蒙古自治区乌兰察布市四子王旗第一中学2020-2021学年高二上学期期中考试化学试题(已下线)【南昌新东方】3. 2020 高二上 南昌二中 期中考试 吴丹(已下线)2.3 化学反应的方向(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)吉林省长春市第二中学2021-2022学年高二上学期期末考试化学试题广东省潮州湘桥区南春中学2021-2022学年高二上学期期中考试化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题大庆市肇州县肇州中学2021-2022学年高二上学期第二次月考化学试题广东省江门广雅中学2022-2023学年高二上学期期中考试化学试题安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷甘肃省白银市靖远县第一中学2023-2024学年高二上学期12月期末考试化学试题湖南省张家界市民族中学2023-2024学年高二上学期第四次月考化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第三次月考化学试题
7 . 已知:
又已知不同温度下, 、
、 的值如下:
的值如下:
(1)若 时进行反应①,
时进行反应①, 的起始浓度为
的起始浓度为 ,
, 后建立平衡,则
后建立平衡,则 的转化率为
的转化率为__________ ,用 表示的反应速率为
表示的反应速率为__________ 。
(2) 进行反应③,其平衡常数为
进行反应③,其平衡常数为 为
为__________ (求具体数值),焓变
__________ (填“>”“=”或“<”)0,若已知该反应仅在高温时正反应自发,则
__________ (填“>”“=”或“<”)0。
(3)下列图象符合反应②的是__________ (填序号)。(图中v是速率, 为混合物中
为混合物中 的体积分数)
的体积分数)
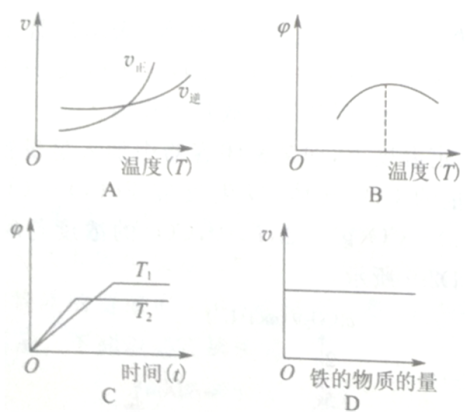
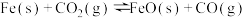 |  | ① |
 |  | ② |
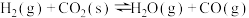 |  | ③ |
 、
、 的值如下:
的值如下:| 温度/℃ |  |  |
| 500 |  |  |
| 700 | 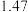 | 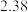 |
| 900 | 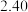 | 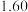 |
 时进行反应①,
时进行反应①, 的起始浓度为
的起始浓度为 ,
, 后建立平衡,则
后建立平衡,则 的转化率为
的转化率为 表示的反应速率为
表示的反应速率为(2)
 进行反应③,其平衡常数为
进行反应③,其平衡常数为 为
为

(3)下列图象符合反应②的是
 为混合物中
为混合物中 的体积分数)
的体积分数)
您最近一年使用:0次
名校
8 . 煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)下列有关说法正确的是
| A.反应I在较低的温度下可自发进行 |
| B.反应II在较低的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应I和反应II可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
| A.5.6 g铁粉与硝酸反应失去电子数一定为0.3×6.02×1023 |
| B.反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH<0、ΔS>0 |
| C.电解精炼铜过程中,电路中每通过1 mol电子,阳极溶解铜32 g |
D.0.1mol·L-1 Na2SO3溶液中:c(OH-)-c(H+)=2c(H2SO3)+c(HSO ) ) |
您最近一年使用:0次
2018-09-04更新
|
504次组卷
|
2卷引用:2018-2019学年人教版高中化学选修四模块综合测评题
名校
解题方法
10 . 以下对影响反应方向因素的判断不正确的是
| A.有时焓变对反应的方向起决定性作用 |
| B.有时熵变对反应的方向起决定性作用 |
| C.焓变和熵变是判断反应方向的两个主要因素 |
| D.任何情况下,温度都不可能对反应的方向起决定性作用 |
您最近一年使用:0次
2017-07-25更新
|
709次组卷
|
16卷引用:2018-2019学年鲁科版高中化学选修四:第2章检测题
2018-2019学年鲁科版高中化学选修四:第2章检测题陕西省黄陵中学2016-2017学年高一(重点班)下学期期末考试化学试题河南省南阳市第一中学2017-2018学年高二上学期第二次月考化学试题重庆市北碚区2019-2020学年高二11月联合性测试化学试题陕西省宝鸡市渭滨区2019—2020学年高二上学期期末考试化学试题河南省洛阳市孟津县第二高级中学2020-2021学年高二上学期9月月考化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第三节 化学反应的方向 作业帮湖北省黄冈麻城市第二中学2021届高三上学期第一次质量检测化学试题(已下线)2.3 化学反应的方向(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.3 化学反应的方向(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)贵州省安顺市平坝第一高级中学2018-2019学年高二上学期期中考试化学试题福建省建瓯市芝华中学2019-2020学年高二上学期期中考试化学(1-2班)试题云南省迪庆州维西县第二中学2019-2020学年上学期高二期末考试化学试题贵州省雷山县第四中学2019-2020学年高二上学期期末考试化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期第二次月考化学试题吉林江城中学2021-2022学年高二上学期期中考试化学试题



