1 . 常温下,将体积均为 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是
 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是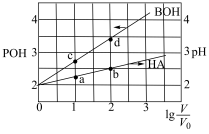
A.电离常数: |
| B.水的电离程度:b>d |
C.升温,a点溶液中 增大 增大 |
| D.等浓度HA和BOH溶液等体积混合,溶液的pH<7 |
您最近一年使用:0次
名校
解题方法
2 . 常温下,下列说法正确的是
| A.pH加和为12的强酸与弱酸混合,pH可能为6 |
| B.pH加和为12的强酸与弱碱等体积混合,溶液一定呈碱性 |
| C.pH加和为12的弱酸与强碱混合,若成中性,则v(酸)>v(碱) |
| D.pH加和为12的强酸与强碱混合,若成中性,则两溶液体积比为100:1 |
您最近一年使用:0次
2018-11-08更新
|
1740次组卷
|
5卷引用:山东省莱州市第一中学2020-2021学年高二上学期10月月考化学试题
10-11高三·山东·阶段练习
3 . 化学实验是研究物质性质的基础。
(1)下列有关实验操作或测量数据合理的是_________ (填序号)。
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8mL的Na2CO3溶液
(2)某废水样品中含有一定的Na+、 、
、 ,甲、乙两研究小组欲测定其中
,甲、乙两研究小组欲测定其中 离子的浓度。
离子的浓度。
甲组方案:
试剂X从下列试剂中选择:
a.0.1mol·L-1KMnO4(H2SO4酸化)溶液
b.0.5mol·L-1NaOH溶液
c.新制氯水d.KI溶液
①加入的试剂X为______ (填字母序号),生成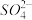 主要的离子方程式为
主要的离子方程式为___________ 。
②甲组方案中,第iii步的“系列操作”包含的操作名称各为_________________ 。
乙组方案:
i.用烧杯盛取废水适量,加少量活性炭,除去废水的杂色;过滤,取滤液;
ii.

(3)某同学制备Fe(OH)3胶体:用洁净烧杯量取适量蒸馏水加热至沸腾,向烧杯中缓慢滴加饱和的FeCl3溶液,并不断用玻璃棒搅拦,结果溶液变浑浊。该同学制备胶体失败的原因是____________ ,你认为成功制得Fe(OH)3胶体的特征现象是_________________ 。
(4)用下图装置进行CO2性质的有关实验。

①试剂瓶B中盛有饱和NaHCO3溶液,其目的是______________ 。
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系______________ 。
(1)下列有关实验操作或测量数据合理的是
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8mL的Na2CO3溶液
(2)某废水样品中含有一定的Na+、
 、
、 ,甲、乙两研究小组欲测定其中
,甲、乙两研究小组欲测定其中 离子的浓度。
离子的浓度。甲组方案:

试剂X从下列试剂中选择:
a.0.1mol·L-1KMnO4(H2SO4酸化)溶液
b.0.5mol·L-1NaOH溶液
c.新制氯水d.KI溶液
①加入的试剂X为
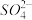 主要的离子方程式为
主要的离子方程式为②甲组方案中,第iii步的“系列操作”包含的操作名称各为
乙组方案:
i.用烧杯盛取废水适量,加少量活性炭,除去废水的杂色;过滤,取滤液;
ii.

(3)某同学制备Fe(OH)3胶体:用洁净烧杯量取适量蒸馏水加热至沸腾,向烧杯中缓慢滴加饱和的FeCl3溶液,并不断用玻璃棒搅拦,结果溶液变浑浊。该同学制备胶体失败的原因是
(4)用下图装置进行CO2性质的有关实验。

①试剂瓶B中盛有饱和NaHCO3溶液,其目的是
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系
您最近一年使用:0次
4 . 部分弱电解质的电离平衡常数如下表:
下列说法不正确的是
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3·H2O |
| 电离平衡常数 (25 ℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
下列说法不正确的是
A.结合H+的能力: >CN-> >CN-> >HCOO- >HCOO- |
B.0.1mol/L的HCOONH4溶液中:c(HCOO-)>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| C.25 ℃时,pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水) |
D.0.1mol/L的NaHCO3溶液中:c(Na+)+ c(H+)=c( )+c(OH-)+c( )+c(OH-)+c( ) ) |
您最近一年使用:0次
2015-05-11更新
|
1082次组卷
|
3卷引用:2015届广东省韶关市高三调研考试理综化学试卷



