名校
解题方法
1 . 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是


| A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、 |
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、 |
D.a点对应的溶液中大量存在: 、Na+、I-、Fe3+ 、Na+、I-、Fe3+ |
您最近一年使用:0次
2 . 回答下列问题:
(1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料。
已知25℃,101kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式为_______ 。
(2)某温度时水的离子积Kw=1.0×10-13,则该温度时纯水的pH_______ 7(填“>”、“<”或“=”)。该温度下,pH=2的CH3COOH溶液中,水电出的c(H+)=_______ 。
(3)25 ℃时,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比11∶9混合,混合液的pH=_______ 。
(4)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池。
①负极材料是_______ (写名称)。
②正极电极反应式为_______ 。
③溶液中SO 向
向_______ 极移动。
(1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料。
已知25℃,101kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式为
(2)某温度时水的离子积Kw=1.0×10-13,则该温度时纯水的pH
(3)25 ℃时,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比11∶9混合,混合液的pH=
(4)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池。
①负极材料是
②正极电极反应式为
③溶液中SO
 向
向
您最近一年使用:0次
名校
3 . 常温下,将pH=3的强酸溶液和pH=12的强碱溶液混合,当混合液的pH等于11时,强酸与强碱溶液的体积比是
| A.9∶2 | B.11∶2 | C.10∶1 | D.9∶1 |
您最近一年使用:0次
2022-09-19更新
|
1191次组卷
|
5卷引用:吉林江城中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
4 . 室温下,柠檬水溶液的pH是3,则其中由水电离出的c(H+)是
| A.1×10-11mol/L | B.1×10-3mol/L | C.1×10-7mol/L | D.0.3mol/L |
您最近一年使用:0次
2022-09-19更新
|
430次组卷
|
3卷引用:吉林江城中学2021-2022学年高二上学期期中考试化学试题
5 . 下列叙述正确的是
| A.室温下,某溶液由水电离出来的H+的浓度为1.0×10-10 mol·L-1,则该溶液的pH=4 |
| B.100 ℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| C.一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1 |
D.25 ℃时,c(H+)=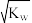 mol·L-1=1.0×10-7 mol·L-1的溶液一定呈中性 mol·L-1=1.0×10-7 mol·L-1的溶液一定呈中性 |
您最近一年使用:0次
名校
6 . 常温下,0.1mol/L某一元酸(HA)溶液中 ,下列叙述不正确的是
,下列叙述不正确的是
 ,下列叙述不正确的是
,下列叙述不正确的是A.该溶液与 NaOH溶液等体积混合后: NaOH溶液等体积混合后: |
B.常温下HA的电离平衡常数约为 |
C.该溶液中水电离出的 |
D.向该溶液中加入一定量水稀释,溶液中 增大 增大 |
您最近一年使用:0次
名校
解题方法
7 . 一定温度下,纯水中存在
 的平衡,下列叙述一定正确的是
的平衡,下列叙述一定正确的是

 的平衡,下列叙述一定正确的是
的平衡,下列叙述一定正确的是A.向水中滴入少量稀盐酸,平衡逆向移动, 减小 减小 |
B.向水中加入少量固体硫酸钠, , , 不变 不变 |
C.向水中加入少量固体 ,平衡逆向移动, ,平衡逆向移动, 降低 降低 |
D.将水加热, 增大,pH减小 增大,pH减小 |
您最近一年使用:0次
名校
8 . 现有浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(1)将③和④按体积比1∶2混合后,混合液中各离子浓度由大到小的顺序是_______ 。
(2)已知t ℃时,Kw=1×10-13,则t ℃_______ (填“>”“<”或“=”)25 ℃。
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ (填“酸”、“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=_______ 。
(1)将③和④按体积比1∶2混合后,混合液中各离子浓度由大到小的顺序是
(2)已知t ℃时,Kw=1×10-13,则t ℃
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显
您最近一年使用:0次
名校
解题方法
9 . 25℃ 时,用0.01mol·L-1 H2SO4溶液滴定0.01 mol·L-1 NaOH溶液,中和后加水至100 mL。若在滴定时终点判断有误差:①多加了1滴H2SO4溶液;②少加了1滴H2SO4溶液(设1滴为0.05 mL),则①和②的溶液中由水电离出的c(H+)的比值是
| A.1 | B.50 | C.2.5×103 | D.104 |
您最近一年使用:0次
名校
解题方法
10 . 一定温度下,用水稀释 的一元弱酸
的一元弱酸 ,随着稀释的进行,下列数值一定增大的是(
,随着稀释的进行,下列数值一定增大的是( 表示水的离子积,
表示水的离子积, 表示
表示 的电离常数)
的电离常数)
 的一元弱酸
的一元弱酸 ,随着稀释的进行,下列数值一定增大的是(
,随着稀释的进行,下列数值一定增大的是( 表示水的离子积,
表示水的离子积, 表示
表示 的电离常数)
的电离常数)A. | B.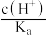 | C. | D.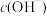 |
您最近一年使用:0次
2021-08-07更新
|
982次组卷
|
12卷引用:吉林省长春市第二实验中学2020-2021学年高二上学期期中考试化学试题
吉林省长春市第二实验中学2020-2021学年高二上学期期中考试化学试题辽宁省六校协作体2020-2021学年高二上学期期中联考化学试题湖南省邵东创新实验学校2021-2022学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时1 水的电离黑龙江省牡丹江市东宁市第一中学2020-2021学年高二上学期第一次月考化学试题选择性必修1(SJ)专题3第一单元课时3 水的电离选择性必修1 专题3 第一单元 弱电解质的电离平衡(已下线)第三章 第二节水的电离和溶液的酸碱性(第1课时 水的电离和溶液的酸碱性)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)3.2.1 水的电离和溶液的酸碱性-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.2.1 水的电离 溶液的酸碱性(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)3.1.1强电解质和弱电解质 弱电解质的电离平衡 课后3.1.2水的电离平衡 课后



