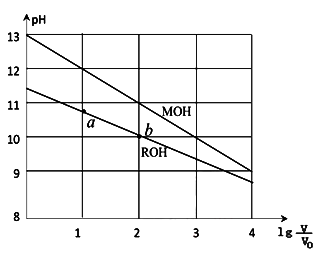
1 . 浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随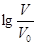 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
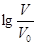 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
| A.MOH的碱性强于ROH的碱性 |
| B.ROH的电离程度:b点大于a点 |
| C.若两溶液无限稀释,则它们的c(OH-)相等 |
D.当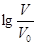 =2时,若两溶液同时升高温度,则 =2时,若两溶液同时升高温度,则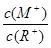 增大 增大 |
您最近一年使用:0次
2016-12-09更新
|
9270次组卷
|
62卷引用:2018-2019学年鲁科版高中化学选修四:模块综合检测题(一)
2018-2019学年鲁科版高中化学选修四:模块综合检测题(一)山东省菏泽市第一中学老校区2018-2019学年高二上学期期末模拟化学试题2015年全国普通高等学校招生统一考试化学(新课标I卷)河北省衡水中学2015-2016学年高二上一调考试化学试卷2015-2016学年河北正定中学高二上学期第一次联考化学试卷2015-2016学年河北省衡水中学高二上学期调考化学试卷2015-2016学年湖北省荆州中学高二上第二次月考化学试卷陕西省西安市第一中学2015-2016学年高二上12月月考化学试卷2015-2016学年湖南师大附属中学高二上二次阶段测化学卷2015-2016学年江西省余江一中高二上期中考试化学试卷2015-2016学年湖南省浏阳一中高二上第三次月考化学试卷2015-2016学年山西省忻州一中高二上学期期末理化学试卷2016届甘肃省武威二中高三下学期开学考试理综化学试卷2016-2017学年湖南省长沙一中高二上第一次月考化学卷2016-2017学年河北省冀州中学高二上期中化学卷2016-2017学年安徽省淮北市第一中学高二下学期第一次月考化学试卷山西省康杰中学2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题八对接高考精练--弱电解质的电离平衡内蒙古赤峰市宁城县2018届高三10月月考化学试题湖北省沙市中学2017-2018学年高二上学期第三次双周考试化学试题江西省临川第二中学2017-2018学年高二上学期期中考试化学试题山西省康杰中学2017-2018学年高二上学期期中考试化学试题(已下线)解密11 弱电解质的电离和溶液的酸碱性——备战2018年高考化学之高频考点解密【全国百强校】湖北省武汉市华中师范大学第一附属中学2018-2019学年高二上学期期中检测化学试题河北省沧州市盐山中学2018-2019学年高二上学期12月月考化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二上学期期末考试化学试题(已下线)2019年3月2日《每日一题》二轮复习- 周末培优【全国百强校】江苏省扬州中学2018-2019学年高二下学期4月月考化学试题云南省腾冲市第八中学2018-2019学年高二下学期期中考试化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高二上学期期中考试化学(理)试题河北省承德第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题8.1 弱电解质的电离平衡(练)-《2020年高考一轮复习讲练测》辽宁省丹东市凤城市第一中学2019-2020学年高二上学期12月月考化学试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题1 弱电解质的电离复习题云南省楚雄永仁一中2020届高三3月线上模拟理综化学试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训四川省遂宁市船山区第二中学校2019-2020学年高二下学期期中考试化学试题江西省赣州市赣州县第三中学2019-2020学年高二下学期入学考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 高考帮黑龙江省鹤岗市第一中学2020-2021学年高二10月月考化学试题(已下线)易错18 电解质溶液图像-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题新疆北屯高级中学2020-2021学年高二上学期10月月考化学试题河南省郑州市第一〇六高级中学2020-2021学年高二上学期11月考试化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第二次月考化学试题青海省湟川中学2019-2020学年高二上学期期中考试化学试题安徽省蚌埠市2020-2021学年高二上学期期末统考化学试题江西省赣州市赣县第三中学2020-2021学年高二下学期2月入学考试化学试题(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)广东省惠州市第一中学2021-2022学年高二上学期第二次考试化学试题河南省南阳市第一中学校2021-2022学年高二上学期第三次月考化学试题广东省惠州市第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题河南省信阳高级中学2021-2022学年高二下学期4月月考化学试题第三章 本章复习提升3(已下线)专题八 水溶液中的离子反应与平衡 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(段考)化学科试题 广西钟山县钟山中学2021-2022学年高二上学期第三次(12月)月考化学(理科)试题(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)四川省凉山州宁南中学2022-2023学年高二上学期期末考试化学试题
13-14高三·全国·课后作业
名校
2 . 0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化正确的是
①电离程度增大 ②c(NH3·H2O)增大 ③ 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥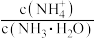 增大
增大
①电离程度增大 ②c(NH3·H2O)增大 ③
 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥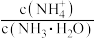 增大
增大| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
您最近一年使用:0次
2021-06-02更新
|
2037次组卷
|
37卷引用:山东省东营市胜利第二中学2020-2021学年高二上学期期中考试化学试题
山东省东营市胜利第二中学2020-2021学年高二上学期期中考试化学试题山东省济南市商河县第一中学2020-2021学年高二10月月考化学试题(已下线)2014年化学高考总复习课时演练 8-1弱电解质的电离练习卷(已下线)2014高考化学专题突破训练 专题7电解质溶液练习卷黑龙江省大庆中学2018届高三上学期开学考试化学试题湖北省长阳县第一高级中学2017-2018学年高二9月月考化学试题陕西省黄陵中学高新部2019-2020学年高二上学期期中考试化学试题云南省曲靖市宣威市第九中学2019-2020学年高二上学期第二次段考化学试题云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题沪科版化学高二拓展性课程3《化学中的平衡》测试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡 课时2 电离平衡常数黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第二次月考化学试题安徽省合肥市第十一中学2020-2021学年高二上学期第二次月考化学试题山东省临沂市兰陵县2021-2022学年高二上学期期中考试化学试题山东省临沂市兰山区、罗庄区2021-2022学年高二上学期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(理)试题广西南宁市第四中学2020-2021学年高二下学期开学考试化学试题云南省丽江市第一中学2020-2021学年高二下学期期中考试化学试题云南省新平县一中2020-2021学年高二下学期期中考试化学试题选择性必修1(SJ)专题3第一单元课时2 电离平衡常数辽宁省沈阳市郊联体2021-2022学年高二上学期期中考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期中考试化学试卷云南省玉溪市第二中学2021-2022学年高二上学期期中考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题(已下线)专题23 强酸(碱)与弱酸(碱)的比较-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)山西省朔州市朔城区第一中学校2021-2022学年高二下学期开学检测化学试题新疆师范大学附属中学2021-2022学年高二12月月考化学试题吉林省长春市第二实验中学2021-2022学年高二上学期10月月考化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题四川省凉山州宁南中学2022-2023学年高二上学期第二次月考化学试题黑龙江省饶河县高级中学2021-2022学年高二上学期期中考试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第二次调研考试化学试题安徽省怀宁县第二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
3 . 常温下,浓度均为1 mol/L的HX溶液、HY溶液,分别加水稀释。稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是
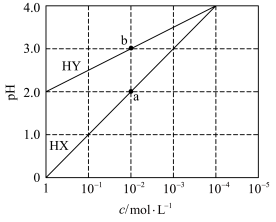

| A.HX是强酸,溶液每稀释至原体积的10倍,pH始终增大1 |
| B.常温下HY的电离常数为1.0×10-4 |
| C.溶液中水的电离程度:a点大于b点 |
| D.消耗同浓度NaOH溶液的体积:a点大于b点 |
您最近一年使用:0次
2020-11-02更新
|
1672次组卷
|
17卷引用:广西钦州市2018届高三上学期第一次质量检测理综化学试题1
广西钦州市2018届高三上学期第一次质量检测理综化学试题1广西钦州市2018届高三上学期第一次质量检测理综化学试题2湖北省沙市中学2019-2020学年高二上学期期末考试化学试题(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时2 溶液的酸碱性与pH河北省衡水市武强中学2020-2021学年高二上学期第一次月考化学试题山东省临沂市平邑县第一中学实验部2021-2022学年高二上学期第二次月考化学试题宁夏银川市长庆高级中学2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题3第二单元课时1 溶液的酸碱性与pH黑龙江省绥化市第一中学2021-2022学年高二上学期期中考试化学试卷第三章水溶液中的离子反应与平衡作业(十五) 溶液 pH的计算吉林省长春市第八中学2022-2023学年高二上学期11月期中考试化学试题河北省衡水市武强中学2023-2024学年高二上学期期中考试化学试题【精品卷】3.2.2 溶液的酸碱性与pH课堂例题-人教版2023-2024学年选择性必修1河北省邯郸市永年区高级中学2023-2024学年高二上学期期中考试化学试题河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷
名校
解题方法
4 . 室温下,向两份浓度均为0.1mol/LHX溶液中分别滴加0.1mol/L盐酸和NaOH溶液,向两份0.1mol/LHY溶液中也进行同样操作,测得x[x=-lg 其中A=X或Y]与溶液pH的关系如图所示。
其中A=X或Y]与溶液pH的关系如图所示。

已知:Ka(HX)>Ka(HY)
下列说法正确的是
 其中A=X或Y]与溶液pH的关系如图所示。
其中A=X或Y]与溶液pH的关系如图所示。
已知:Ka(HX)>Ka(HY)
下列说法正确的是
| A.HY溶液对应的曲线为I,Ka(HY)的数量级为10-4 |
| B.a点溶液中:c(HY)+c(Y-)=0.10mol/L |
| C.溶液中水的电离程度:f>e>d |
| D.e点溶液中:c(Na+)<c(HX),NaX的Kh=1.0×10-10.5 |
您最近一年使用:0次
2021-05-13更新
|
950次组卷
|
5卷引用:2020年山东卷化学高考真题变式题11-15
(已下线)2020年山东卷化学高考真题变式题11-15山东省滨州市2021届高三第二次模拟考试化学试题(已下线)专题10 水溶液中的离子平衡-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期5月月考化学试题
真题
名校
5 . 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。据图判断正确的是


| A.Ⅱ为盐酸稀释时pH值变化曲线 | B.b点溶液的导电性比c点溶液的导电性强 | C.a点Kw的数值比c点Kw的数值大 | D.b点酸的总浓度大于a点酸的总浓度 |
您最近一年使用:0次
2019-01-30更新
|
2989次组卷
|
80卷引用:2009年普通高等学校招生统一考试理综试题化学部分(山东卷)
2009年普通高等学校招生统一考试理综试题化学部分(山东卷)(已下线)2011-2012学年山东省济宁市梁山二中高二上学期期中考试化学试卷(已下线)2014届山东省济南一中高二上学期期末考试化学试卷 2015-2016学年山东寿光现代中学高二上12月月考化学卷2016-2017学年山东省寿光现代中学高二12月月考化学卷2山东省寿光现代中学2017-2018学年高二12月月考化学试题山东省淄博市淄川区般阳中学2019-2020学年高二上学期期中考试化学试题(已下线)2010年湖北省武汉市华中师大一附中高三五月适应性考试理综化学试题(已下线)2010年广西桂林十八中高二上学期期中考试化学卷(已下线)2010—2011学年辽宁省北镇高中高二上学期期末考试化学试卷(已下线)2011-2012年山西省平遥中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年江西省安福中学高二上学期期中考试化学试卷(已下线)2011-2012学年辽宁省沈阳同泽女中高二上学期期中考试化学试卷(已下线)2011-2012学年河南省濮阳市高二上学期期末考试化学试卷(已下线)2011-2012学年山西省“晋商四校”高二下学期联考化学试卷(已下线)2011-2012学年江西省白鹭洲中学高二下学期第三次月考化学试卷(已下线)2013-2014学年广东省佛山市高二上学期普通高中质量检测化学试卷(已下线)2014-2015学年黑龙江大庆铁人中学高二上期中考试化学卷(已下线)2015届黑龙江省牡丹江第一高中高二上学期期中考试化学(理)试卷(已下线)2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷2016届安徽省安庆市第二中学高三上学期第一次质检化学试卷2015-2016学年四川省成都市六校高二上学期期中联考化学试卷2015-2016学年江苏省射阳县第二中学高二上学期期末选修化学试卷2015-2016学年河北省唐山市高二上学期期末考试化学试卷2015-2016学年湖北省孝感市六校教学联盟高二上期末联考化学试卷2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二12月月考化学试题(A卷)甘肃省天水市第一中学2017-2018学年高二下学期入学考试化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】山西省忻州第一中学2018-2019学年高二上学期第一次月考化学试题河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】河北省武邑中学2019届高三上学期期中考试化学试题吉林省长春市九台区师范高级中学2018-2019学年高二上学期期中考试化学试题云南省大理市下关一中2018-2019学年高二上学期期中考试化学试题【全国百强校】山西省忻州市第一中学2018-2019学年高二上学期第一次月考化学试题【校级联考】吉林省辽源市田家炳高级中学(第六十六届友好学校)2018-2019学年高二上学期期末联考化学试题宁夏回族自治区长庆高级中学2018-2019学年高二上学期期末考试化学试题【全国百强校】内蒙古杭锦后旗奋斗中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题江苏省启东中学2019-2020学年高二上学期第一次质量检测化学试题辽宁省大连市旅顺口区2018-2019学年高二上学期期中考试化学试题安徽省阜阳市颍上二中2019-2020学年高二上学期第二次段考化学试题步步为赢高二化学寒假作业:作业八 溶液的酸黑龙江省哈尔滨工业大学附属中学2019-2020学年高二上学期期末考试化学试题(已下线)上海市闸北区2012届高三上学期期末化学试题江苏苏州市第四中学2019-2020学年高二下学期5月自学能力测试化学试题(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 作业帮吉林省长春市第七中学2020-2021学年高二上学期第一次月考化学试题河南省洛阳市豫西名校2020-2021学年高二上学期第一次联考化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 易错疑难集训(一)新疆昌吉州教育共同体2020-2021学年高二上学期期中考试化学试题吉林省油田高级中学2020-2021学年高二上学期期初考试化学试题重庆市育才中学校2020-2021学年高二上学期10月月考化学试题江苏省南京市中华中学2020-2021学年高二上学期9月测试化学试题广东省广州市禺山高级中学2020-2021学年高二下学期第一阶段考试化学试题黑龙江省大庆中学2021-2022学年高二上学期第一次月考化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题吉林省长春市农安县2021-2022学年高二上学期期末考试化学试题(已下线)3.2.2 溶液pH的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)吉林省延边朝鲜族自治州汪清县汪清第四中学2021-2022学年高二上学期第二次阶段考试化学试题福建省莆田市莆田第十五中学2021-2022学年高二下学期第一次月考化学试题湖南省常德市石门县第一中学2021-2022学年高一下学期期中考试化学试题辽宁省阜新市第二高级中学2021-2022学年高二上学期期末考试化学试题湖南省邵东创新实验学校2021-2022学年高二上学期期中考试化学试题福建省莆田第七中学2021-2022学年高二下学期期中考试化学试题天津市西青区杨柳青第一中学2022-2023学年高二上学期第一次适应性测试化学试题浙江省北斗联盟2022-2023学年高二上学期期中联考化学试题湖北省武汉市东湖中学2022-2023学年高二上学期期中考试化学试题(已下线)3.2.2 pH计算和酸碱中和滴定-同步学习必备知识内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题宁夏回族自治区银川市北方民族大学附属中学2020-2021学年高二下学期3月月考化学试题广东省广州市从化区从化中学2022-2023学年高二上学期期中考试化学试题广西河池市罗城仫佬族自治县高级中学等2校2022-2023学年高二上学期12月月考化学试题辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题天津市第五十四中学2023-2024学年高二上学期11月期中考试化学试题江苏省南菁高级中学2023-2024学年高二上学期10月考试化学试题陕西省延安市延川县中学2023-2024学年高二上学期第一次月考化学试题2023-2024学年高二上学期化学期中考试试卷
名校
6 . 25℃时, 溶液加水稀释,混合溶液中
溶液加水稀释,混合溶液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 溶液加水稀释,混合溶液中
溶液加水稀释,混合溶液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A. |
B.P、Q点对应溶液中 的值: 的值: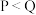 |
C.若将溶液无限稀释,溶液中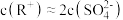 |
D.相同条件下,若改为 ,P点移至W点 ,P点移至W点 |
您最近一年使用:0次
2020-12-18更新
|
1126次组卷
|
4卷引用:山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)
山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题(已下线)2021年1月浙江高考化学试题变式题21-25全书综合测评2
7 . 某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是


| A.曲线Ⅰ代表HNO2溶液 |
| B.溶液中水的电离程度:b点>c点 |
| C.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同 |
D.从c点到d点,溶液中 减小(其中HA、A-分别代表相应的酸和酸根离子) 减小(其中HA、A-分别代表相应的酸和酸根离子) |
您最近一年使用:0次
2020-12-13更新
|
1027次组卷
|
7卷引用:山东省莱西市第一中学2020-2021学年高二上学期12月月考化学试题
山东省莱西市第一中学2020-2021学年高二上学期12月月考化学试题河北省邯郸市大名一中、磁县一中,邯山区一中,永年一中等六校2020-2021学年高二上学期期中考试化学试题 (已下线)第三章 水溶液中的离子反应与平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)辽宁省葫芦岛市兴城市高级中学2021-2022学年高二上学期10月月考化学试题黑龙江省大庆铁人中学2021-2022学年高二上学期期中考试化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题广东省广州市第八十六中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
8 . 下列图示或根据图示所得出的结论正确的是
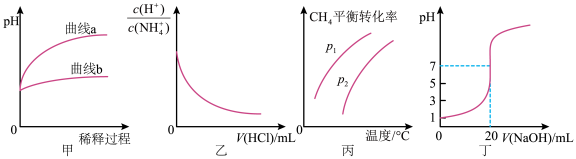

| A.图甲表示相同pH的盐酸和醋酸加水稀释过程中pH的变化,则曲线a代表醋酸 |
B.图乙表示温度不变,向0.1mol·L-1NH4Cl溶液中滴加0.1mol·L-1盐酸时,溶液中 随盐酸体积的变化关系 随盐酸体积的变化关系 |
| C.图丙表示密闭容器中CH4(g)+ H2O(g)⇌CO(g)+3H2(g)到达平衡时,CH4的平衡转化率与压强、温度的变化关系曲线,说明P1<P2 |
| D.图丁表示0.1000mol·L-1NaOH溶液滴定20.00 mL 0.1000mol·L-1醋酸溶液滴定曲线 |
您最近一年使用:0次
2020-07-21更新
|
986次组卷
|
10卷引用:山东省实验中学2021届高三上学期第一次诊断考试化学试题
山东省实验中学2021届高三上学期第一次诊断考试化学试题江苏省苏州市2019-2020学年高二下学期学业质量阳光指标调研化学试题江苏省苏州市2019-2020学年高二下学期期末考试化学试题江苏省扬州市扬州中学2021届高三开学检测化学试题河北省邢台市第二中学2021届高三上学期第四次月考化学试题安徽省黄山市2020-2021学年高二下学期期末考试化学试题上海市卢湾高级中学2022届高三下学期在线评估综合练习一(4月线上模拟考)化学试题(已下线)微专题38 新情景下的综合图象与突破-备战2023年高考化学一轮复习考点微专题吉林省大安市第一中学校2021-2022学年高二上学期第三次月考化学试题18 2024年苏州高新区吴县高级中学高二3月月考
名校
9 . 根据下列图示所得出的结论正确的是( )
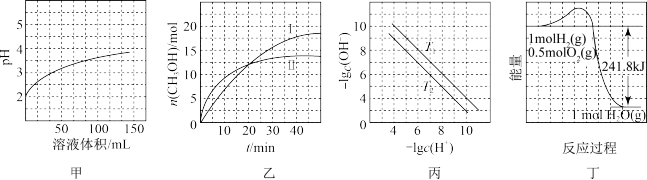

| A.图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸 |
B.图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ |
| C.图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2 |
| D.图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1 |
您最近一年使用:0次
2019-03-04更新
|
1120次组卷
|
6卷引用:山东省济南市历城区第一中学2020届高三12月检测化学试题
名校
10 . 常温下,浓度均为0.1mol·L-1、体积为V0的HX、HY溶液,分别加水稀释至体积V,pH随lg  的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是
| A.HX、HY都是弱酸,且HX的酸性比HY的弱 |
| B.常温下,由水电离出的c(H+)·c(OH-):a<b |
| C.相同温度下,电离常数K(HX):a>b |
D.lg  =3,若同时微热两种溶液,则 =3,若同时微热两种溶液,则 减小 减小 |
您最近一年使用:0次
2019-12-01更新
|
847次组卷
|
25卷引用:山东省章丘市第四中学2019届高三上学期第二次质量检测理综化学试题
山东省章丘市第四中学2019届高三上学期第二次质量检测理综化学试题2016届湖北省武汉市高三下学期2月调研理综化学试卷四川省成都市第七中学2017届高三6月高考热身考试理综化学试题山西省朔州市应县第一中学2017-2018学年高二上学期月考(四)化学试题四川省广安市2017-2018学年高二上学期期末考试化学试题【全国市级联考】安徽省合肥市2019届高三上学期调研性检测化学试题【全国校级联考】全国大联考2019届高三入学调研考试卷(四)化学试题河南省鹤壁市淇县第一中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第三单元 水溶液中的离子平衡单元测试A卷(已下线)《2018-2019学年同步单元双基双测AB卷》第三单元 水溶液中的离子平衡单元测试B卷重庆市万州第三中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高二上学期期中考试化学试题【全国百强校】河北省辛集中学2019届高三上学期期中考试化学试题【全国百强校】福建省厦门外国语学校2018-2019学年高二下学期第一次月考化学试题福建省厦门市湖滨中学2018-2019学年高二下学期期中考试化学试题【全国百强校】广东省深圳外国语学校2017-2018学年高二上学期期中化学试题河南省许昌市许昌高级中学2019-2020学年高二上学期开学考试化学试题(尖子生)重庆市黔江新华中学校2019-2020学年高二10月月考化学试题江西省赣州市第三中学2019—2020学年高二上学期12月月考化学试题湖北省黄冈市浠水县实验高级中学2019-2020学年高二上学期期中复习检测化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——水的电离及影响因素(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)第一部分 二轮专题突破 专题14 溶液中的三大平衡及应用(已下线)题型128 一元酸(碱)溶液加水稀释后溶液的判断图像



