19-20高二·浙江·期中
1 . Ⅰ.(1)请写出Al(OH)3酸式电离方程式
(2)混盐指的是一种盐中有一种阳离子,还有两种或以上的酸根阴离子,混盐CaOCl2中各离子均满足8电子结构,请写出CaOCl2的电子式:
(3)氧化性比较F2
Ⅱ.(1)已知室温下Kw=1.0×10-14,计算室温条件下0.1 mol/L HCl溶液中由水电离的氢离子浓度为
(2)室温下弱酸HA的电离平衡常数Ka=1.6×10-5 mol/L,计算0.01mol/L溶液的pH为
您最近半年使用:0次
名校
解题方法
2 . 室温下,用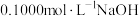 滴定
滴定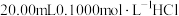 溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
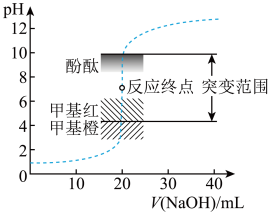
(1)酸碱式滴定管在加溶液滴定前,需要的操作是___________ 和_________ 。
(2)当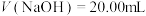 时,溶液中所有离子的浓度存在的关系是
时,溶液中所有离子的浓度存在的关系是___________ 。
(3)已知 ,当加入的
,当加入的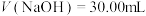 时,溶液中pH=
时,溶液中pH=___________ 。
(4)下列说法不正确 的是_________ 。
A.NaOH与盐酸恰好完全反应时,
B.选择甲基红指示反应终点,误差比甲基橙的大
C.当接近滴定终点时,极少量的碱就会引起溶液的pH突变
D.选择变色范围在pH突变范围内的指示剂,可减小实验误差
E.当用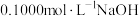 滴定
滴定 溶液时,其突变范围比滴定
溶液时,其突变范围比滴定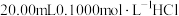 溶液的突变范围大
溶液的突变范围大
(5)在化学分析中,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 和
和 反应生成砖红色沉淀表示滴定终点。当溶液中的
反应生成砖红色沉淀表示滴定终点。当溶液中的 恰好完全沉淀时,溶液中的
恰好完全沉淀时,溶液中的
___________  。
。
已知:①25℃时, ,
,
②当溶液中某种离子的浓度等于或小于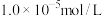 时,可认为已完全沉淀。
时,可认为已完全沉淀。
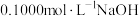 滴定
滴定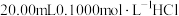 溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
(1)酸碱式滴定管在加溶液滴定前,需要的操作是
(2)当
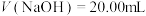 时,溶液中所有离子的浓度存在的关系是
时,溶液中所有离子的浓度存在的关系是(3)已知
 ,当加入的
,当加入的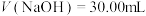 时,溶液中pH=
时,溶液中pH=(4)下列说法
A.NaOH与盐酸恰好完全反应时,

B.选择甲基红指示反应终点,误差比甲基橙的大
C.当接近滴定终点时,极少量的碱就会引起溶液的pH突变
D.选择变色范围在pH突变范围内的指示剂,可减小实验误差
E.当用
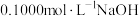 滴定
滴定 溶液时,其突变范围比滴定
溶液时,其突变范围比滴定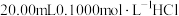 溶液的突变范围大
溶液的突变范围大(5)在化学分析中,以
 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 和
和 反应生成砖红色沉淀表示滴定终点。当溶液中的
反应生成砖红色沉淀表示滴定终点。当溶液中的 恰好完全沉淀时,溶液中的
恰好完全沉淀时,溶液中的
 。
。已知:①25℃时,
 ,
,
②当溶液中某种离子的浓度等于或小于
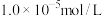 时,可认为已完全沉淀。
时,可认为已完全沉淀。
您最近半年使用:0次
名校
解题方法
3 . 常温下,关于溶液稀释的说法正确的是
| A.将1L0.1mol•L-1的Ba(OH)2溶液加水到体积为2L,pH=13 |
B.pH=3的醋酸溶液加水稀释到原浓度的 ,pH=5 ,pH=5 |
C.pH=4的H2SO4溶液加水稀释到原浓度的 ,溶液中由水电离产生的c(H+)=1×10-6mol•L-1 ,溶液中由水电离产生的c(H+)=1×10-6mol•L-1 |
D.pH=8的NaOH溶液加水稀释到原浓度的 ,其pH=6 ,其pH=6 |
您最近半年使用:0次
2022-09-28更新
|
975次组卷
|
5卷引用:浙江省金华市东阳市外国语学校2023-2024学年高二上学期10月月考化学试题
浙江省金华市东阳市外国语学校2023-2024学年高二上学期10月月考化学试题(已下线)第22讲 水的电离与溶液的pH(练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期第三次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期11月期中考试化学试题(已下线)第2讲 溶液的酸碱性和pH计算
解题方法
4 . 用 表示阿伏加德罗常数的数值,下列说法
表示阿伏加德罗常数的数值,下列说法不正确 的是
 表示阿伏加德罗常数的数值,下列说法
表示阿伏加德罗常数的数值,下列说法A.惰性电极电解 溶液,转移的电子数最多为 溶液,转移的电子数最多为 |
B.在含 的 的 溶液中, 溶液中, 数目可能大于 数目可能大于 |
C.常温下,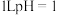 的硫酸溶液中,氢离子的数目为 的硫酸溶液中,氢离子的数目为 |
D. 与足量 与足量 溶液反应后,所得溶液中 溶液反应后,所得溶液中 数目小于 数目小于 |
您最近半年使用:0次
5 . 某同学模拟工业废水变废为宝,设计了用沉淀法回收各金属阳离子的实验方案:

已知:
①溶液中某离子浓度小于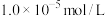 ,可认为该离子不存在;
,可认为该离子不存在;
②实验过程中,假设溶液体积、温度不变;
③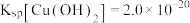 ;
;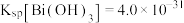 ;
;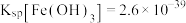 ;
; 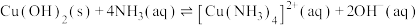

下列说法不正确的是

| 模拟工业废水的离子浓度(mol/l) |  |  |  |  |  |
| 0.10 | 0.010 | 0.0040 | 0.0010 | 0.141 |
①溶液中某离子浓度小于
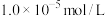 ,可认为该离子不存在;
,可认为该离子不存在;②实验过程中,假设溶液体积、温度不变;
③
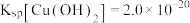 ;
;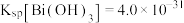 ;
;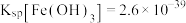 ;
; 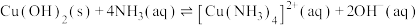

下列说法不正确的是
A.步骤I中加入的 |
B.步骤II得到的滤液N中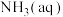 的浓度 的浓度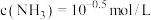 |
C.步骤III得到的沉淀Z为 |
D.反应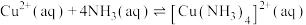 的平衡常数 的平衡常数 |
您最近半年使用:0次
2023-05-31更新
|
447次组卷
|
3卷引用:浙江省重点中学拔尖学生培养联盟2023届高三下学期6月适应性考试化学试题
浙江省重点中学拔尖学生培养联盟2023届高三下学期6月适应性考试化学试题江西省智学联盟体2023-2024学年高三上学期第一次联考化学试题 (已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
6 . 下列说法不正确 的是
| A.25℃时,0.1mol·L−1NaHCO3溶液和CH3COONa溶液,前者的pH较大 |
| B.25℃时,pH相同的HCl溶液和NH4Cl溶液,后者的c(Cl-)较大 |
| C.40℃时,0.01mol·L−1HClO4溶液的pH=2 |
| D.25℃时,pH=2的某酸HA溶液和pH=12的某碱BOH溶液分别加水稀释100倍后,两溶液pH之和小于14,则HA一定是弱酸 |
您最近半年使用:0次
2022-04-23更新
|
176次组卷
|
2卷引用:浙江省稽阳联谊学校2021-2022学年高三下学期4月联考化学试题
7 . 25℃时,由水电离出来的c(H+)=1×10-12,则关于溶液的pH的说法正确的是( )
| A.可能2或12 | B.一定是2 | C.一定是12 | D.一定是7 |
您最近半年使用:0次
名校
解题方法
8 . 下列关于溶液的酸碱性,说法正确的是
| A.pH=7的溶液呈中性 |
| B.中性溶液中一定有:c(H+)=1.0×10-7 mol·L-1 |
| C.在100°C时,纯水的pH<7,因此显酸性 |
| D.在100°C时,c(H+)=c(OH-)的溶液呈中性 |
您最近半年使用:0次
2022-04-08更新
|
291次组卷
|
3卷引用:浙江省宁波市北仑中学2021-2022学年高一下学期期中考试(1班)化学试题
20-21高三上·浙江·期中
解题方法
9 . 下列说法不正确的是
| A.一定温度下,0.01mol/L的盐酸pH一定等于2 |
| B.常温下,KNO3溶液和CH3COONH4溶液pH均为7,但两溶液中水的电离程度不相同 |
| C.常温下,NaHA溶液呈酸性,说明H2A是弱电解质 |
| D.常温下,pH=7的CH3COOH和CH3COONa混合溶液加水稀释,溶液pH不变 |
您最近半年使用:0次
名校
解题方法
10 . 下列说法正确 的是
| A.298K时,pH=10的氨水稀释100倍,所得溶液的pH=8 |
| B.298K时,pH=9的CH3COONa溶液和pH=5的盐酸等体积混合,溶液显中性 |
C.HClO与HF的混合溶液中c(H+)= |
| D.等pH的盐酸和氯化铵两种溶液,导电能力相同 |
您最近半年使用:0次
2020-12-19更新
|
198次组卷
|
6卷引用:浙江省绍兴市2020年稽阳联考高三化学试题
浙江省绍兴市2020年稽阳联考高三化学试题浙江省杭州高级中学2021届高三上学期期中考试化学试题(已下线)【浙江新东方】116浙江省瑞安中学2020--2021学年高二上学期期末考试化学试题(已下线)【浙江新东方】高中化学20210513-042【2021】【高二下】河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题



