1 . 某化学兴趣小组模拟酒驾的检测方法,设计如下实验:
①配制500mLc1mol/LK2Cr2O7标准溶液并加入少许稀硫酸酸化;
②量取VmL酒精溶液置于锥形瓶中;
③加入c1mol/LK2Cr2O7标准溶液V1mL,充分反应后,再加入过量的KI溶液和指示剂;
①用c2mol/LNa2S2O3溶液滴定反应后的溶液,达到滴定终点时,重复三次,平均消耗Na2S2O3溶液的体积为V2mL。
已知有关反应为:16H++2 +3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++
+3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++ +6I-=2Cr3++3I2+7H2O、I2+2
+6I-=2Cr3++3I2+7H2O、I2+2 =2I-+
=2I-+ 。
。
对上述实验,下列说法正确的是
①配制500mLc1mol/LK2Cr2O7标准溶液并加入少许稀硫酸酸化;
②量取VmL酒精溶液置于锥形瓶中;
③加入c1mol/LK2Cr2O7标准溶液V1mL,充分反应后,再加入过量的KI溶液和指示剂;
①用c2mol/LNa2S2O3溶液滴定反应后的溶液,达到滴定终点时,重复三次,平均消耗Na2S2O3溶液的体积为V2mL。
已知有关反应为:16H++2
 +3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++
+3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++ +6I-=2Cr3++3I2+7H2O、I2+2
+6I-=2Cr3++3I2+7H2O、I2+2 =2I-+
=2I-+ 。
。对上述实验,下列说法正确的是
| A.若实验前锥形瓶中存在少量水,将导致测定结果偏小 |
| B.若因酒精挥发造成消耗Na2S2O3溶液的体积偏大,将导致测定结果偏大 |
| C.步骤③中加入K2Cr2O7溶液时,不慎有少量液体外洒,将导致测定结果偏大 |
| D.步骤④中,滴定终点时,若俯视读数,将导致测定结果偏小 |
您最近一年使用:0次
2 . 三氯化硼可用于有机反应催化剂、电子工业等,其熔点为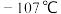 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
Ⅰ.制备
将氯气通入装有mg 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且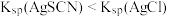 。
。
取反应后 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
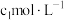
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用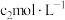 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。
下列说法正确的是)
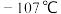 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:Ⅰ.制备
将氯气通入装有mg
 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且
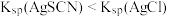 。
。取反应后
 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
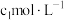
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用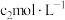 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。下列说法正确的是)
| A.滴入最后半滴标准溶液,溶液由红色变为无色,且半分钟不褪色,说明达到滴定终点 |
B.实验所得产品的产率是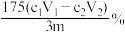 |
| C.若未加硝基苯,则测定结果将偏大 |
D.实验中用碱式滴定管盛放 水解液 水解液 |
您最近一年使用:0次
解题方法
3 . 富马酸亚铁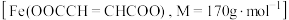 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:
I.制备
步骤1:将 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为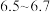 。
。
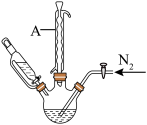
步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加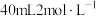 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应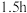 ;
; 。
。
II.纯度测定
取 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 ),平行测定三次,消耗标准溶液的平均体积为
),平行测定三次,消耗标准溶液的平均体积为 。
。
对于上述实验,下列说法不正确的是
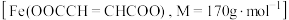 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:I.制备
步骤1:将
 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为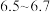 。
。步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通
 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加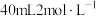 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应 ;
;
 。
。II.纯度测定
取
 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 ),平行测定三次,消耗标准溶液的平均体积为
),平行测定三次,消耗标准溶液的平均体积为 。
。对于上述实验,下列说法不正确的是
A.“步骤2”若不通入 会导致产品纯度降低 会导致产品纯度降低 |
| B.可以用硝酸代替硫酸进行纯度测定 |
C.加入煮沸过的蒸馏水小于 ,对实验结果无影响 ,对实验结果无影响 |
| D.滴定前仰视读数,导致产品纯度测定结果偏低 |
您最近一年使用:0次
4 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
5 . 测定150.0g新鲜菠菜中草酸含量(以 计),实验方案如图。下列说法错误的是
计),实验方案如图。下列说法错误的是
 计),实验方案如图。下列说法错误的是
计),实验方案如图。下列说法错误的是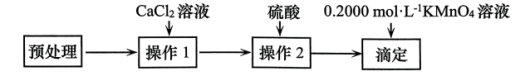
| A.“操作1”需要用到的主要玻璃仪器有3种 |
| B.“操作2”若用盐酸替代硫酸可能会导致测定结果偏高 |
| C.“滴定”至终点后,需再静置滴定管1~2分钟后读数,否则会使测定结果偏高 |
D.若滴定终点消耗30.00mL 溶液,则测得菠菜中草酸含量为9.000% 溶液,则测得菠菜中草酸含量为9.000% |
您最近一年使用:0次
6 . 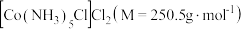 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。
(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入 研细的
研细的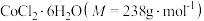 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到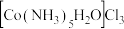 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到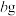 产品。
产品。
(2)钴的测定:取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入 ,用
,用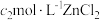 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。
根据上述原理,下列说法错误的是
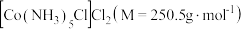 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入
 研细的
研细的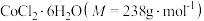 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到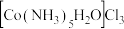 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到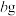 产品。
产品。(2)钴的测定:取
 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入 ,用
,用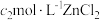 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。根据上述原理,下列说法错误的是
A.若用热水洗涤紫红色晶体,将导致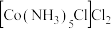 的产率偏小 的产率偏小 |
| B.还原为钴(Ⅱ)后,锥形瓶内壁残留少量沉淀,将导致钴的质量分数测量结果偏小 |
C.配制 时,定容时若仰视刻度线,将导致钴的质量分数测量结果偏小 时,定容时若仰视刻度线,将导致钴的质量分数测量结果偏小 |
| D.滴定结束后滴定管中有气泡产生,将导致钴的质量分数测量结果偏大 |
您最近一年使用:0次
7 . 利用工业废液生产 CuSCN具有经济价值和社会效益。SCN⁻的测定方法如下:
①准确称取 CuSCN 样品 m g 置于 100 mL 烧杯中,加入 30 mL 水,再加入 20.00 mL 溶液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中速滤纸过滤于100 mL 容量瓶中,用蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无SCN⁻,用去离子水稀释滤液到刻度,混匀,作为含SCN⁻的待测试液。
溶液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中速滤纸过滤于100 mL 容量瓶中,用蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无SCN⁻,用去离子水稀释滤液到刻度,混匀,作为含SCN⁻的待测试液。
②准确移取25.00mL SCN⁻待测试液于250mL锥形瓶中,加入8 mL硝酸酸化,摇匀后,加入 标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.050 0
标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.050 0 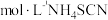 标准溶液滴定至终点,平行滴定3次,记录平均消耗NH4SCN 标准溶液的体积为`V2mL。
标准溶液滴定至终点,平行滴定3次,记录平均消耗NH4SCN 标准溶液的体积为`V2mL。
已知:CuSCN+NaOH =NaSCN+CuOH↓,2CuOH =Cu2O+H2O;Ag⁺ +SCN⁻=AgSCN↓(白色)。
根据上述实验原理,下列说法错误的是
①准确称取 CuSCN 样品 m g 置于 100 mL 烧杯中,加入 30 mL 水,再加入 20.00 mL
 溶液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中速滤纸过滤于100 mL 容量瓶中,用蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无SCN⁻,用去离子水稀释滤液到刻度,混匀,作为含SCN⁻的待测试液。
溶液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中速滤纸过滤于100 mL 容量瓶中,用蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无SCN⁻,用去离子水稀释滤液到刻度,混匀,作为含SCN⁻的待测试液。②准确移取25.00mL SCN⁻待测试液于250mL锥形瓶中,加入8 mL硝酸酸化,摇匀后,加入
 标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.050 0
标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.050 0 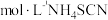 标准溶液滴定至终点,平行滴定3次,记录平均消耗NH4SCN 标准溶液的体积为`V2mL。
标准溶液滴定至终点,平行滴定3次,记录平均消耗NH4SCN 标准溶液的体积为`V2mL。已知:CuSCN+NaOH =NaSCN+CuOH↓,2CuOH =Cu2O+H2O;Ag⁺ +SCN⁻=AgSCN↓(白色)。
根据上述实验原理,下列说法错误的是
| A.用去离子水稀释滤液超过刻度线,立即吸出多余部分,将导致测定结果偏小 |
| B.用滴定管量取含SCN⁻的待测液时,没有润洗滴定管,将导致测量结果偏小 |
| C.使用 NH4SCN标准溶液滴定至终点时俯视读数,将导致测定结果偏小 |
| D.滴定过程中发现溶液出现淡粉色,立即读数,将导致测定结果偏大 |
您最近一年使用:0次
8 . 醋酸钙片常用于补钙、缓解磷过多症等。某小组为了测定醋酸钙片纯度,进行如下实验:
①称取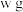 醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入
醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入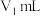
 溶液。
溶液。
②完全反应后,加水稀释吸收液并配制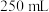 溶液。
溶液。
③准确量取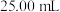 配制溶液于锥形瓶中,滴加指示剂R,用
配制溶液于锥形瓶中,滴加指示剂R,用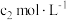 盐酸滴定过量的
盐酸滴定过量的 至终点,消耗滴定液
至终点,消耗滴定液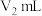 。
。
下列叙述正确的是
①称取
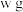 醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入
醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入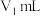
 溶液。
溶液。②完全反应后,加水稀释吸收液并配制
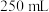 溶液。
溶液。③准确量取
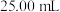 配制溶液于锥形瓶中,滴加指示剂R,用
配制溶液于锥形瓶中,滴加指示剂R,用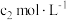 盐酸滴定过量的
盐酸滴定过量的 至终点,消耗滴定液
至终点,消耗滴定液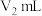 。
。下列叙述正确的是
| A.指示剂R可以选择酚酞溶液或甲基橙溶液 |
| B.步骤②配制溶液定容时仰视读数,配制溶液的浓度偏高 |
| C.步骤③中,若没有润洗酸式滴定管会使测定结果偏高 |
D.上述实验测得醋酸钙样品纯度为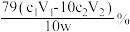 |
您最近一年使用:0次
名校
9 . 化学需氧量(Chemial Oxygen Demand)是在一定条件下,用强氧化剂氧化一定体积水中的还原性物质时所消耗氧化剂的量,折算成氧气的量(单位为mg/L)来表示。我国地表水可采用标准 法测定水中化学需氧量(COD),即水体中还原性物质每消耗
法测定水中化学需氧量(COD),即水体中还原性物质每消耗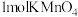 折算为
折算为 的消耗量。其操作步骤如下:
的消耗量。其操作步骤如下:
①取水样 ,先加入足量稀硫酸酸化,再加入
,先加入足量稀硫酸酸化,再加入 的
的 标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
②向①中溶液中加入 的
的 标准液(过量)。
标准液(过量)。
③用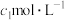 的
的 标准液滴定②中溶液至滴定终点,消耗
标准液滴定②中溶液至滴定终点,消耗 标准液
标准液 。
。
根据上述实验原理,下列说法错误的是
 法测定水中化学需氧量(COD),即水体中还原性物质每消耗
法测定水中化学需氧量(COD),即水体中还原性物质每消耗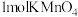 折算为
折算为 的消耗量。其操作步骤如下:
的消耗量。其操作步骤如下:①取水样
 ,先加入足量稀硫酸酸化,再加入
,先加入足量稀硫酸酸化,再加入 的
的 标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。②向①中溶液中加入
 的
的 标准液(过量)。
标准液(过量)。③用
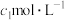 的
的 标准液滴定②中溶液至滴定终点,消耗
标准液滴定②中溶液至滴定终点,消耗 标准液
标准液 。
。根据上述实验原理,下列说法错误的是
A.若水样中 含量偏高,则所测水样中COD偏大 含量偏高,则所测水样中COD偏大 |
| B.步骤③滴定终点俯视读数,则所测水样中COD偏大 |
| C.步骤①中若煮沸时间过短,则所测水样中COD偏小 |
D.步骤①煮沸后,若红色消失说明水样中COD偏大,需补加 标准液 标准液 |
您最近一年使用:0次
解题方法
10 . 下列有关实验操作的描述正确的是
| A.加热液体出现暴沸时,立即停止加热并加入沸石 |
| B.配制Na2SiO3溶液时,加入少量NaOH溶液 |
| C.用热的氢氧化钠溶液清洗试管内壁残留的矿物油 |
| D.滴定实验时,不能向锥形瓶中加入蒸馏水,以免溶液稀释产生误差 |
您最近一年使用:0次



