1 . 25℃时,用 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是

 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
A.25℃时, 的电离平衡常数为 的电离平衡常数为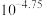 |
B. 所示溶液中: 所示溶液中: |
C. 所示溶液中: 所示溶液中: |
D. 所示溶液中: 所示溶液中: |
您最近一年使用:0次
名校
2 . 常温下,用0.10mol/L的NaOH溶液滴定0.10mol/L的HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列叙述错误的是


| A.Ka(HA)的数量级约为10-5 |
B.N点,c(Na+)-c(A-)=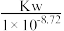 |
| C.P→Q过程中,水的电离程度逐渐减小 |
| D.当滴定至溶液呈中性时,c(A-)>c(HA) |
您最近一年使用:0次
名校
解题方法
3 . ROH是一种一元碱,25℃时,在20.0mL0.1mol·L-1ROH溶液中滴加0.1mol·L-1盐酸VmL,混合溶液的pH与lg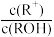 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是

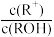 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
| A.a点时,V=10.0 |
| B.b点时,x=3.75 |
| C.b点溶液中,c(ROH)>c(R+) |
| D.c点溶液中,c(Cl-)>c(R+)>c(H+)>c(OH-) |
您最近一年使用:0次
解题方法
4 . 25℃时,0.10 L某二元弱酸H2A用1.00 mol·L-1NaOH溶液调节其pH,溶液中H2A、HA-及A2-的物质的量浓度变化如图所示:

下列说法错误 的是

下列说法
| A.H2A的Ka1=1×10-4 |
| B.溶液在X点和Z点时水的电离程度相同 |
| C.在Y点时,c(Na+)>3c(A2-) |
| D.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-) |
您最近一年使用:0次
2020-11-11更新
|
641次组卷
|
2卷引用:湖南省永州市2021届高三第二次模拟考试理综化学试题



