名校
解题方法
1 . 25℃时,用 溶液滴定20mL
溶液滴定20mL 溶液的滴定曲线如图所示(曲线上的数字为pH)。已知:
溶液的滴定曲线如图所示(曲线上的数字为pH)。已知: 二元弱酸;25℃时,
二元弱酸;25℃时,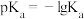 ,
, 的
的 ,
, 。下列说法正确的是
。下列说法正确的是

 溶液滴定20mL
溶液滴定20mL 溶液的滴定曲线如图所示(曲线上的数字为pH)。已知:
溶液的滴定曲线如图所示(曲线上的数字为pH)。已知: 二元弱酸;25℃时,
二元弱酸;25℃时, ,
, 的
的 ,
, 。下列说法正确的是
。下列说法正确的是
| A.a点消耗NaOH溶液体积小于10.00mL |
B.滴定过程中,某时刻溶液中 ,则此时溶液的pH=4.34 ,则此时溶液的pH=4.34 |
| C.溶液中水的电离程度:b>d |
D.向d点溶液中滴入盐酸至中性,离子浓度大小关系为 |
您最近一年使用:0次
解题方法
2 . 实验室使用 传感器来测定某
传感器来测定某 和
和 混合溶液中
混合溶液中 的含量,用
的含量,用 盐酸滴定该混合溶液,得到如图曲线。滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。以下说法错误的是
盐酸滴定该混合溶液,得到如图曲线。滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。以下说法错误的是

 传感器来测定某
传感器来测定某 和
和 混合溶液中
混合溶液中 的含量,用
的含量,用 盐酸滴定该混合溶液,得到如图曲线。滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。以下说法错误的是
盐酸滴定该混合溶液,得到如图曲线。滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。以下说法错误的是
A.未滴定时该混合溶液中: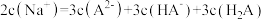 |
B.滴定过程中, 恒成立 恒成立 |
C.滴加 盐酸时,溶液中: 盐酸时,溶液中: |
D.滴加 盐酸时,溶液中: 盐酸时,溶液中: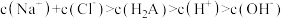 |
您最近一年使用:0次
3 . 25℃时,用 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是

 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
A.25℃时, 的电离平衡常数为 的电离平衡常数为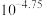 |
B. 所示溶液中: 所示溶液中: |
C. 所示溶液中: 所示溶液中: |
D. 所示溶液中: 所示溶液中: |
您最近一年使用:0次
名校
4 . 常温下,用0.10mol/L的NaOH溶液滴定0.10mol/L的HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列叙述错误的是


| A.Ka(HA)的数量级约为10-5 |
B.N点,c(Na+)-c(A-)=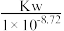 |
| C.P→Q过程中,水的电离程度逐渐减小 |
| D.当滴定至溶液呈中性时,c(A-)>c(HA) |
您最近一年使用:0次
5 . 25℃时,向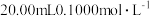 的两种酸HX、HY中分别滴加
的两种酸HX、HY中分别滴加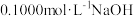 溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法错误的是
溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法错误的是

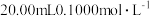 的两种酸HX、HY中分别滴加
的两种酸HX、HY中分别滴加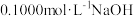 溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法错误的是
溶液,测得两溶液pH随NaOH溶液体积变化的曲线如图所示。下列说法错误的是
A.酸性: |
B.a点溶液中微粒浓度: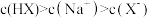 |
C.滴加NaOH溶液至 时,两溶液中 时,两溶液中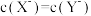 |
D.从开始滴加至 溶液时,两溶液中 溶液时,两溶液中 的电离程度均逐渐增大 的电离程度均逐渐增大 |
您最近一年使用:0次
名校
解题方法
6 . ROH是一种一元碱,25℃时,在20.0mL0.1mol·L-1ROH溶液中滴加0.1mol·L-1盐酸VmL,混合溶液的pH与lg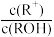 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是

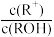 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
| A.a点时,V=10.0 |
| B.b点时,x=3.75 |
| C.b点溶液中,c(ROH)>c(R+) |
| D.c点溶液中,c(Cl-)>c(R+)>c(H+)>c(OH-) |
您最近一年使用:0次
解题方法
7 . 常温下,向10.00mL 0.10 mol/L HCl和0.20 mol/L 的混合溶液中逐滴加入0. 10 mol/L NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),且
的混合溶液中逐滴加入0. 10 mol/L NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),且 的电离常数
的电离常数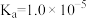 。已知指示剂变色范围为甲基橙 (3. 1〜4. 4),酚酞(8. 2〜10. 0),下列说法不正确的是
。已知指示剂变色范围为甲基橙 (3. 1〜4. 4),酚酞(8. 2〜10. 0),下列说法不正确的是

 的混合溶液中逐滴加入0. 10 mol/L NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),且
的混合溶液中逐滴加入0. 10 mol/L NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),且 的电离常数
的电离常数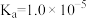 。已知指示剂变色范围为甲基橙 (3. 1〜4. 4),酚酞(8. 2〜10. 0),下列说法不正确的是
。已知指示剂变色范围为甲基橙 (3. 1〜4. 4),酚酞(8. 2〜10. 0),下列说法不正确的是
| A.测定盐酸浓度时,可选用酚酞或甲基橙作为指示剂 |
| B.点b处c(CH3COOH) + c(CH3COO-) = 0.2mol/L |
| C.点b处溶液pH为3 |
D.点c处溶液中粒子浓度大小为 |
您最近一年使用:0次
解题方法
8 . 25℃时,0.10 L某二元弱酸H2A用1.00 mol·L-1NaOH溶液调节其pH,溶液中H2A、HA-及A2-的物质的量浓度变化如图所示:

下列说法错误 的是

下列说法
| A.H2A的Ka1=1×10-4 |
| B.溶液在X点和Z点时水的电离程度相同 |
| C.在Y点时,c(Na+)>3c(A2-) |
| D.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-) |
您最近一年使用:0次
2020-11-11更新
|
641次组卷
|
2卷引用:湖南省永州市2021届高三第二次模拟考试理综化学试题
解题方法
9 . 298K时,向20 mL 0.1000 mol·L-1 CH3COOH溶液中滴入0.1000 mol·L-1NaOH溶液,滴定曲线如图所示(忽略温度变化)。下列说法正确的是


| A.该滴定过程应该选择石蕊溶液做指示剂 |
| B.由c点数值可求醋酸的电离平衡常数为1.66×10-5 mol·L-1 |
| C.b点溶液中各微粒浓度关系为2c(H+)+c(CH3COOH) =c(CH3COO-)+2c(OH-) |
| D.中和同体积同pH的醋酸和盐酸所用氢氧化钠的物质的量,后者多 |
您最近一年使用:0次
2020-05-09更新
|
408次组卷
|
2卷引用:湖南省邵阳市新邵县2019-2020学年高二下学期期末考试化学试题



