名校
1 . 下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近一年使用:0次
名校
2 . 已知:亚硝酸( )是一种弱酸,亚硝酸钠(
)是一种弱酸,亚硝酸钠( )是一种常用的食品防腐剂。常温下,将0.1mol⋅L-1
)是一种常用的食品防腐剂。常温下,将0.1mol⋅L-1 溶液加水稀释或加入少量
溶液加水稀释或加入少量 晶体时,下列观点正确的是
晶体时,下列观点正确的是
 )是一种弱酸,亚硝酸钠(
)是一种弱酸,亚硝酸钠( )是一种常用的食品防腐剂。常温下,将0.1mol⋅L-1
)是一种常用的食品防腐剂。常温下,将0.1mol⋅L-1 溶液加水稀释或加入少量
溶液加水稀释或加入少量 晶体时,下列观点正确的是
晶体时,下列观点正确的是A.加水稀释时,电离平衡正向移动,溶液中 增大 增大 |
B.加 晶体时,电离平衡逆向移动,溶液导电能力增强 晶体时,电离平衡逆向移动,溶液导电能力增强 |
C.加水稀释时, 的电离程度增大,电离常数也增大 的电离程度增大,电离常数也增大 |
D.加 晶体时,溶液的pH增大,与 晶体时,溶液的pH增大,与 增大有关 增大有关 |
您最近一年使用:0次
2023-12-26更新
|
137次组卷
|
2卷引用:安徽省滁州中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 以下措施中,能使 溶液中
溶液中 减小,
减小, 增大的是
增大的是
 溶液中
溶液中 减小,
减小, 增大的是
增大的是| A.升高温度 | B.加入少量 |
C.加入少量 | D.加水稀释 |
您最近一年使用:0次
4 . 稀氨水中存在着平衡:NH3·H2O
 +OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的
+OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤MgSO4固体

 +OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的
+OH-,若要使平衡向逆方向移动,同时使c平(OH-)增大,应加入适量的①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤MgSO4固体
| A.①②③ | B.③⑤ | C.③ | D.③④ |
您最近一年使用:0次
2023-08-26更新
|
1282次组卷
|
4卷引用:第1课时 弱电解质的电离平衡
名校
5 . 弱酸型指示剂( )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: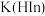 为
为 的电离平衡常数,
的电离平衡常数,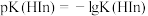 ]
]
 )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: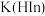 为
为 的电离平衡常数,
的电离平衡常数,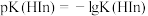 ]
]A.常温下,向 溶液中滴加 溶液中滴加 ,溶液变红 ,溶液变红 |
B.常温下,溶液 减小过程中,上述平衡向右移动 减小过程中,上述平衡向右移动 |
C. 可能是甲基橙指示剂 可能是甲基橙指示剂 |
D.当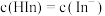 时, 时, 溶液中 溶液中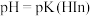 |
您最近一年使用:0次
6 . 已知氨水中存在下列平衡: NH3+H2O  NH3·H2O
NH3·H2O
 +OH-,下列说法正确的是
+OH-,下列说法正确的是
 NH3·H2O
NH3·H2O
 +OH-,下列说法正确的是
+OH-,下列说法正确的是| A.常温下的稀氨水中:c(OH-)·c(H+)>10-14 |
| B.向氨水中加入蒸馏水,溶液的pH增大 |
| C.向浓氨水中加入氢氧化钠固体,会逸出氨气 |
| D.将湿润的蓝色石蕊试纸放在盛有浓氨水的试管口,试纸变红 |
您最近一年使用:0次
7 . 已知K2HPO4溶液中水解程度大于电离程度,对于平衡HPO +H2O
+H2O H3O++PO
H3O++PO ,欲使溶液中c(HPO
,欲使溶液中c(HPO )、c(PO
)、c(PO )、c(H3O+)三种离子浓度均减少,可采用的方法是
)、c(H3O+)三种离子浓度均减少,可采用的方法是
 +H2O
+H2O H3O++PO
H3O++PO ,欲使溶液中c(HPO
,欲使溶液中c(HPO )、c(PO
)、c(PO )、c(H3O+)三种离子浓度均减少,可采用的方法是
)、c(H3O+)三种离子浓度均减少,可采用的方法是| A.加水 | B.加热 |
| C.加消石灰 | D.加AgNO3 |
您最近一年使用:0次
名校
8 . 在CH3COOH CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
 CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是| A.升高温度 | B.增大压强 | C.加少量NaOH固体 | D.通入HCl |
您最近一年使用:0次
2022-11-16更新
|
213次组卷
|
3卷引用:湖北省十堰市县区普通高中联合体2022-2023学年高二上学期11月期中联考化学试题
9 . 醋酸溶液中发生如下电离CH3COOH CH3COO-+H+,下列条件能使电离程度增大的有
CH3COO-+H+,下列条件能使电离程度增大的有
①加水稀释②加NaOH固体③加CH3COONa固体④通入HCl气体⑤升温⑥加入冰醋酸
 CH3COO-+H+,下列条件能使电离程度增大的有
CH3COO-+H+,下列条件能使电离程度增大的有①加水稀释②加NaOH固体③加CH3COONa固体④通入HCl气体⑤升温⑥加入冰醋酸
| A.①②⑤ | B.①②⑤⑥ | C.①②③⑤⑥ | D.①②③④⑤⑥ |
您最近一年使用:0次
解题方法
10 . 25 ℃时,50 mL 0.10 mol/L醋酸中存在电离平衡:CH3COOH CH3COO-+H+
CH3COO-+H+
(1)加入少量冰醋酸,上述平衡向_______ 移动〔填“左”、“右”、“不”,下同〕。
(2)加入少量0.1mol/L盐酸,上述平衡向_______ 移动。
(3)加入一定量蒸馏水,上述平衡向_______ 移动。
(4)加入20mL 0.1mol/LNaCl溶液,上述平衡向_______ 移动。
 CH3COO-+H+
CH3COO-+H+(1)加入少量冰醋酸,上述平衡向
(2)加入少量0.1mol/L盐酸,上述平衡向
(3)加入一定量蒸馏水,上述平衡向
(4)加入20mL 0.1mol/LNaCl溶液,上述平衡向
您最近一年使用:0次



