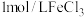名校
解题方法
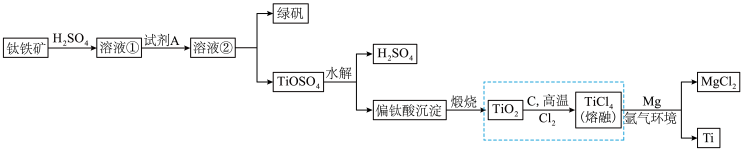
1 . 钛被称为继铁、铝之后的第三金属,性能优越,广泛用于航天航空等领域,有人说“21世纪将是钛的世纪”。冶炼金属钛的主要原料为钛铁矿(主要成分FeTiO3,含FeO、Fe2O3等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾(FeSO4·7H2O)。
(1)Ti在元素周期表中的位置为___________ , 的键角
的键角___________ H2O分子的键角(填 “>”“<”或“=”)。
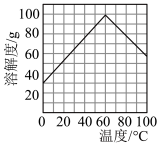
(2)试剂A为___________ 。已知绿矾的溶解度随温度变化的曲线如图所示,从溶液②获得绿矾的操作方法为___________ 、过滤、洗涤、干燥。
(3)已知常温下,Ksp[Fe(OH)2]=8×10-16,若溶液②中c(Fe2+)=0.5mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过___________ (lg2=0.3)。
(4)TiOSO4水解生成偏钛酸(H2TiO3)沉淀的化学方程式为___________ 。
(5)TiCl4的水解程度很大,可以利用其稀溶液制备纳米级TiO2·xH2O,该反应的化学方程式为___________ 。

(1)Ti在元素周期表中的位置为
 的键角
的键角(2)试剂A为

(3)已知常温下,Ksp[Fe(OH)2]=8×10-16,若溶液②中c(Fe2+)=0.5mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过
(4)TiOSO4水解生成偏钛酸(H2TiO3)沉淀的化学方程式为
(5)TiCl4的水解程度很大,可以利用其稀溶液制备纳米级TiO2·xH2O,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . 下列各组离子,在给定条件下一定能够大量共存的是
A. =1012的溶液中:K+、Na+、S2O =1012的溶液中:K+、Na+、S2O 、F- 、F- |
B.常温下pH=7的溶液中:Fe3+、Na+、Cl-、SO |
C.使甲基橙变黄色的溶液中:Na+、NH 、SO 、SO 、NO 、NO |
D.常温下水电离出的c(H+)=1.0×10-10 mol/L的溶液中:Na+、ClO-、SO 、I- 、I- |
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式的书写符合要求的是
A.用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
B.泡沫灭火器的反应原理:2Al3++3CO +3H2O=2Al(OH)3↓+3CO2↑ +3H2O=2Al(OH)3↓+3CO2↑ |
| C.用K3[Fe(CN)6]检验Fe2+:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓ |
| D.铅酸蓄电池的正极反应式:PbO2+2e-+4H+=Pb2++2H2O |
您最近一年使用:0次
4 . 下列说法正确的是
| A.冰在室温下自动熔化成水,是ΔS<0的过程 |
| B.霓虹灯发光与原子核外电子跃迁有关,属于化学变化 |
| C.任何化学反应的反应热均可以通过实验直接进行测定 |
| D.FeCl3溶液和Fe2(SO4)3溶液分别蒸干,所得固体的成分不同 |
您最近一年使用:0次
解题方法
5 . 钛白粉学名二氧化钛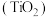 是性能最佳、应用最广、用量最大的白色颜料。钛铁矿
是性能最佳、应用最广、用量最大的白色颜料。钛铁矿 中往往含有
中往往含有 等杂质。一种硫酸法钛白粉生产工艺如图:
等杂质。一种硫酸法钛白粉生产工艺如图:
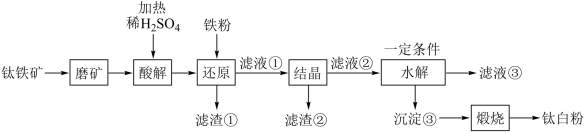
已知:①酸解后,钛主要以 形式存在,强电解质
形式存在,强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。
② 不溶于水和稀酸。
不溶于水和稀酸。
(1)写出基态 原子的价层电子排布式
原子的价层电子排布式___________ 。
(2)磨矿的目的是___________ 。
(3)滤渣①的主要成分是___________ 。
(4)酸解过程中,写出 发生反应的化学方程式
发生反应的化学方程式___________ 。
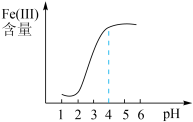
(5)还原过程中,加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中
。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于4~6之间时,
介于4~6之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因:___________ 。
(6)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为___________ 。
②一定量 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中
的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理___________ 。
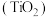 是性能最佳、应用最广、用量最大的白色颜料。钛铁矿
是性能最佳、应用最广、用量最大的白色颜料。钛铁矿 中往往含有
中往往含有 等杂质。一种硫酸法钛白粉生产工艺如图:
等杂质。一种硫酸法钛白粉生产工艺如图:
已知:①酸解后,钛主要以
 形式存在,强电解质
形式存在,强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。②
 不溶于水和稀酸。
不溶于水和稀酸。(1)写出基态
 原子的价层电子排布式
原子的价层电子排布式(2)磨矿的目的是
(3)滤渣①的主要成分是
(4)酸解过程中,写出
 发生反应的化学方程式
发生反应的化学方程式(5)还原过程中,加入铁粉的目的是还原体系中的
 。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中
。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于4~6之间时,
介于4~6之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因:
(6)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为
②一定量
 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中
的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
您最近一年使用:0次
解题方法
6 . 化学与生产、生活密切相关,下列事实与盐类水解无关的是
| A.热纯碱能除去物品表面的油污 |
| B.蓝矾可用于饮用水的杀菌消毒 |
| C.使用泡沫灭火器时将内筒与外筒的Al2(SO4)3溶液和NaHCO3溶液倒立混合 |
| D.将FeCl3饱和溶液滴入沸水中制取Fe(OH)3胶体 |
您最近一年使用:0次
7 . 下列事实不能用勒夏特列原理解释的是
| A.碳酸饮料打开瓶盖后有大量气泡冒出 |
B.其他条件不变,对 、 、 和 和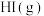 组成的平衡体系加压后颜色变深 组成的平衡体系加压后颜色变深 |
| C.实验室制备乙酸乙酯时,使用过量的乙醇 |
| D.洗涤厨房里的油污时常使用热的纯碱的水溶液 |
您最近一年使用:0次
2024-01-22更新
|
45次组卷
|
2卷引用:辽宁省葫芦岛市普通高中2023-2024学年高二上学期学业质量监测考试化学试题
名校
解题方法
8 . 某化学兴趣小组探究 溶液与
溶液与 的反应历程。
的反应历程。
Ⅰ.药品制备。
(1)实验室制备 的装置如图,仪器a中的试剂是
的装置如图,仪器a中的试剂是__________ 。 溶液的方法是
溶液的方法是__________ 。
Ⅱ.探究 溶液与
溶液与 的反应
的反应
(3)兴趣小组预测, 能使
能使 溶液由黄色变为浅绿色,反应的离子方程式为
溶液由黄色变为浅绿色,反应的离子方程式为__________ 。
向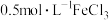 溶液中通入
溶液中通入 至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置
至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置 后变回黄色,静置
后变回黄色,静置 后,变为浅绿色。
后,变为浅绿色。
查阅资料:血红色物质可能与 饱和溶液中的主要微粒:
饱和溶液中的主要微粒: 、
、 、
、 、
、 、
、 有关。
有关。
①取少量上述血红色溶液,立即滴加几滴 溶液A,溶液又褪为黄色。据此推测:红色物质的产生与
溶液A,溶液又褪为黄色。据此推测:红色物质的产生与 无关。物质A的化学式为
无关。物质A的化学式为__________ 。
②向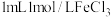 溶液中滴加
溶液中滴加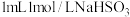 溶液,溶液变为血红色,滴加几滴
溶液,溶液变为血红色,滴加几滴 溶液A,褪成黄色。据此推测:红色物质的产生与
溶液A,褪成黄色。据此推测:红色物质的产生与 和
和 无关,主要与
无关,主要与 或
或 有关。
有关。
③利用分光光度仪测定红色物质的浓度(吸光度越高,浓度越大),实验数据如下:
结论:溶液变血红色的主要原因是 和
和__________ 发生配合反应。
(5)由以上探究结果说明该条件下, 与
与 溶液反应的活化能:配合反应
溶液反应的活化能:配合反应__________ (填“大于”“小于”“等于”)氧化还原反应。
(6)兴趣小组在某次实验中,通入 后未封闭试管,发现血红色更快变回黄色。其可能原因是
后未封闭试管,发现血红色更快变回黄色。其可能原因是__________ (用离子方程式表示)。
 溶液与
溶液与 的反应历程。
的反应历程。Ⅰ.药品制备。
(1)实验室制备
 的装置如图,仪器a中的试剂是
的装置如图,仪器a中的试剂是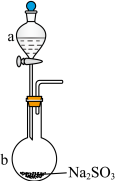
 溶液的方法是
溶液的方法是Ⅱ.探究
 溶液与
溶液与 的反应
的反应(3)兴趣小组预测,
 能使
能使 溶液由黄色变为浅绿色,反应的离子方程式为
溶液由黄色变为浅绿色,反应的离子方程式为向
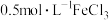 溶液中通入
溶液中通入 至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置
至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置 后变回黄色,静置
后变回黄色,静置 后,变为浅绿色。
后,变为浅绿色。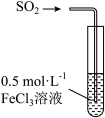
查阅资料:血红色物质可能与
 饱和溶液中的主要微粒:
饱和溶液中的主要微粒: 、
、 、
、 、
、 、
、 有关。
有关。①取少量上述血红色溶液,立即滴加几滴
 溶液A,溶液又褪为黄色。据此推测:红色物质的产生与
溶液A,溶液又褪为黄色。据此推测:红色物质的产生与 无关。物质A的化学式为
无关。物质A的化学式为②向
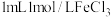 溶液中滴加
溶液中滴加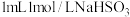 溶液,溶液变为血红色,滴加几滴
溶液,溶液变为血红色,滴加几滴 溶液A,褪成黄色。据此推测:红色物质的产生与
溶液A,褪成黄色。据此推测:红色物质的产生与 和
和 无关,主要与
无关,主要与 或
或 有关。
有关。③利用分光光度仪测定红色物质的浓度(吸光度越高,浓度越大),实验数据如下:
| 吸光度 | ||
|
|
| |
0.5 | 4.0 | 0.0 | 0.412 |
0.5 | 3.6 | 0.4 | 0.359 |
0.5 | 3.2 | 0.8 | 0.331 |
0.5 | 2.8 | 1.2 | 0.297 |
 和
和(5)由以上探究结果说明该条件下,
 与
与 溶液反应的活化能:配合反应
溶液反应的活化能:配合反应(6)兴趣小组在某次实验中,通入
 后未封闭试管,发现血红色更快变回黄色。其可能原因是
后未封闭试管,发现血红色更快变回黄色。其可能原因是
您最近一年使用:0次
解题方法
9 . 下列有关生产、生活的表述与盐类水解无关的是
| A.明矾用作净水剂 |
| B.草木灰去油污 |
C.工业上用TiCl4制备 |
| D.盛放NaOH溶液的试剂瓶不能用磨口玻璃塞 |
您最近一年使用:0次
解题方法
10 . 按如图所示的实验装置或方案进行实验,能达到相应实验目的的是
选项 | A | B | C | D |
装置或方案 |
|
|
|
|
实验目的 | 加热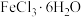 制取无水 制取无水 | 防止铁管道腐蚀 | 验证浓度对化学反应速率的影响 | 铁片表面镀铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次