钛白粉学名二氧化钛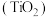 是性能最佳、应用最广、用量最大的白色颜料。钛铁矿
是性能最佳、应用最广、用量最大的白色颜料。钛铁矿 中往往含有
中往往含有 等杂质。一种硫酸法钛白粉生产工艺如图:
等杂质。一种硫酸法钛白粉生产工艺如图:
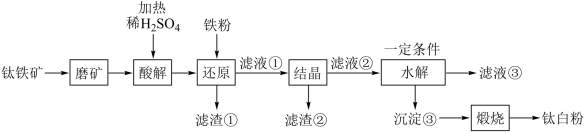
已知:①酸解后,钛主要以 形式存在,强电解质
形式存在,强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。
② 不溶于水和稀酸。
不溶于水和稀酸。
(1)写出基态 原子的价层电子排布式
原子的价层电子排布式___________ 。
(2)磨矿的目的是___________ 。
(3)滤渣①的主要成分是___________ 。
(4)酸解过程中,写出 发生反应的化学方程式
发生反应的化学方程式___________ 。
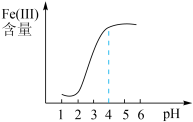
(5)还原过程中,加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中
。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于4~6之间时,
介于4~6之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因:___________ 。
(6)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为___________ 。
②一定量 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中
的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理___________ 。
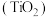 是性能最佳、应用最广、用量最大的白色颜料。钛铁矿
是性能最佳、应用最广、用量最大的白色颜料。钛铁矿 中往往含有
中往往含有 等杂质。一种硫酸法钛白粉生产工艺如图:
等杂质。一种硫酸法钛白粉生产工艺如图:
已知:①酸解后,钛主要以
 形式存在,强电解质
形式存在,强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。②
 不溶于水和稀酸。
不溶于水和稀酸。(1)写出基态
 原子的价层电子排布式
原子的价层电子排布式(2)磨矿的目的是
(3)滤渣①的主要成分是
(4)酸解过程中,写出
 发生反应的化学方程式
发生反应的化学方程式(5)还原过程中,加入铁粉的目的是还原体系中的
 。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中
。为探究最佳反应条件,某实验室做如下尝试:在其它条件不变的情况下,体系中 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于4~6之间时,
介于4~6之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因:
(6)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为
②一定量
 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中
的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
的含量,实验室常用酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理
更新时间:2024-02-06 23:34:49
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】以废钒电池负极电解液(主要化学成分是V3+、V2+、H2SO4) 为原料,回收其中的钒制备V2O5的工艺流程如图所示:
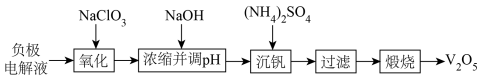
已知:氯酸浓度较高或受热时易发生分解。
回答下列问题:
(1)在“氧化”中低价态钒都转化为 ,其中V3+转化反应的离子方程式为
,其中V3+转化反应的离子方程式为___________ ,实际生产中的氧化剂不选择HClO3的原因是___________ 。
(2)“浓缩”至钒溶液质量浓度(折合V2O5质量浓度)为27.3 g·L-1'时,则溶液中c( )=
)=___________ mol·L-1。(结果保留1位小数)
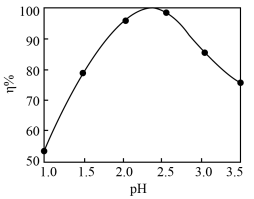
(3)pH对沉钒率(η)的影响如图所示,则沉钒时控制钒液合适的pH范围是___________ ,沉淀产物为2NH4V3O8·H2O,则加(NH4)2SO4沉钒的化学方程式是___________ 。
(4)“过滤”后对沉淀进行洗涤,采用稀(NH4)2SO4作洗涤液的目的是___________ 。检验沉淀已洗涤干净的操作是___________ 。
(5)“煅烧”需要在通风或氧化气氛下进行,其目的是___________ 。

已知:氯酸浓度较高或受热时易发生分解。
回答下列问题:
(1)在“氧化”中低价态钒都转化为
 ,其中V3+转化反应的离子方程式为
,其中V3+转化反应的离子方程式为(2)“浓缩”至钒溶液质量浓度(折合V2O5质量浓度)为27.3 g·L-1'时,则溶液中c(
 )=
)=(3)pH对沉钒率(η)的影响如图所示,则沉钒时控制钒液合适的pH范围是

(4)“过滤”后对沉淀进行洗涤,采用稀(NH4)2SO4作洗涤液的目的是
(5)“煅烧”需要在通风或氧化气氛下进行,其目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
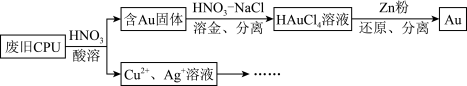
【推荐2】用如图方法回收废旧CPU中的单质 (金)、
(金)、 和
和 。
。 溶解。②
溶解。② :
:
(1)浓、稀 均可作酸溶试剂,溶解等量的
均可作酸溶试剂,溶解等量的 消耗
消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:________ 。
(2) 与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
①将溶金反应的化学方程式补充完整:_____ 
②关于溶金的下列说法正确的是_____ 。
A.用到了 的氧化性B.王水中浓盐酸的主要作用是增强溶液的酸性
的氧化性B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与 也可使
也可使 溶解
溶解
(3)若用 粉将溶液中的
粉将溶液中的 完全还原,则参加反应的
完全还原,则参加反应的 的物质的量为
的物质的量为_____  。
。
(4)用适当浓度的盐酸、 溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收
溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收 和
和 (图中标注的试剂和物质均不同)。
(图中标注的试剂和物质均不同)。_____ ,试剂2是_________ 。
 (金)、
(金)、 和
和 。
。
 溶解。②
溶解。② :
:(1)浓、稀
 均可作酸溶试剂,溶解等量的
均可作酸溶试剂,溶解等量的 消耗
消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:(2)
 与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。
与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同。①将溶金反应的化学方程式补充完整:

②关于溶金的下列说法正确的是
A.用到了
 的氧化性B.王水中浓盐酸的主要作用是增强溶液的酸性
的氧化性B.王水中浓盐酸的主要作用是增强溶液的酸性C.用浓盐酸与
 也可使
也可使 溶解
溶解(3)若用
 粉将溶液中的
粉将溶液中的 完全还原,则参加反应的
完全还原,则参加反应的 的物质的量为
的物质的量为 。
。(4)用适当浓度的盐酸、
 溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收
溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收 和
和 (图中标注的试剂和物质均不同)。
(图中标注的试剂和物质均不同)。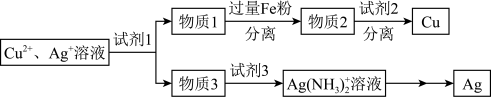
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】铬的化合物应用广泛,工业上以铬铁矿(含Al、Si氧化物等杂质)为主要原料制备红矾钠( )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。
(1)与基态铬原子的最外层电子数相同且同周期的元素有_________ 种。
(2)为了提高“焙烧”效果,可采取的一种措施是____________ 。
(3)“浸取”所得的滤渣为 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为________ 。
(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[ ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度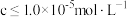 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为________ ;“酸化”过程中的离子方程式为____________ 。 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。
①若电解后溶液中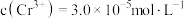 ,则
,则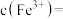
__________  {已知
{已知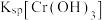
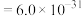 ,
,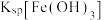 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。
②电解法处理含 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是_________ (填标号)。
A.阳极反应为
B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol 被还原
被还原
 )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。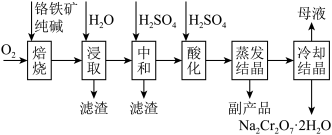
(1)与基态铬原子的最外层电子数相同且同周期的元素有
(2)为了提高“焙烧”效果,可采取的一种措施是
(3)“浸取”所得的滤渣为
 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[
 ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度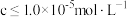 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为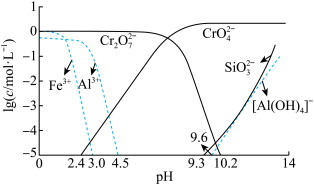
 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。①若电解后溶液中
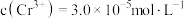 ,则
,则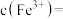
 {已知
{已知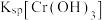
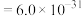 ,
,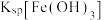 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。②电解法处理含
 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是A.阳极反应为

B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol
 被还原
被还原
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】运用所学知识,解决下列问题:
(1)AgNO3的水溶液呈______ (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_____ ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的是______ 。
(2)今有常温下五种溶液:NH4Cl溶液 CH3COONa溶液 (NH4)2SO4溶液 NH4HSO4溶液 NaOH溶液
①NH4Cl溶液的pH_____ 7(填“>”、“<”或“=”),升高温度可以_______ (填“促进”或“抑制”)NH4Cl的水解;
②pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH_______ NaOH溶液的pH(填“>”“=”或“<”);
③浓度相同的下列三种溶液:(A)NH4Cl溶液(B) (NH4)2SO4溶液(C)NH4HSO4 溶液,则c(NH4+)由大到小的顺序为____ >___ >____ (用序号填空)。
(3)蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合并加热,可得到无水AlCl3,试解释原因________ 。 (提示:SOCl2与水反应的化学方程式为SOCl2 +H2O = SO2↑+ 2HCl↑)
(1)AgNO3的水溶液呈
(2)今有常温下五种溶液:NH4Cl溶液 CH3COONa溶液 (NH4)2SO4溶液 NH4HSO4溶液 NaOH溶液
①NH4Cl溶液的pH
②pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH
③浓度相同的下列三种溶液:(A)NH4Cl溶液(B) (NH4)2SO4溶液(C)NH4HSO4 溶液,则c(NH4+)由大到小的顺序为
(3)蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合并加热,可得到无水AlCl3,试解释原因
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
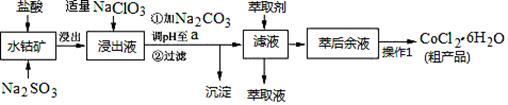
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式_________________ 。
(2)写出NaClO3发生反应的主要离子方程式________________ ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式_________________ 。
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为___________________ 。
(4)“操作1”中包含3个基本实验操作,它们依次是_____________ 、____________ 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是__________________ 。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是______________ ;其使用的最佳pH范围是_________ 。
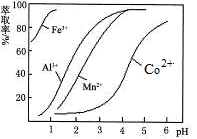
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是______________________ 。(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式
(2)写出NaClO3发生反应的主要离子方程式
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为
(4)“操作1”中包含3个基本实验操作,它们依次是
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是

A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】利用酸解法制钛白粉产生的废液[含有大量的FeSO4、H2SO4和少量的Fe2(SO4)3、TiOSO4]生产铁红和补血剂乳酸亚铁的工艺流程如图所示:
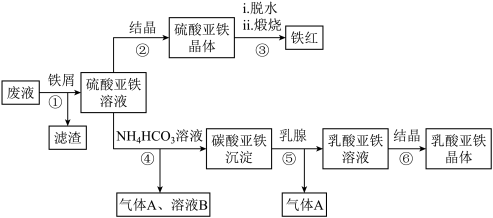
已知:TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-,TiO2+水解成TiO2·xH2O沉淀为可逆反应;乳酸结构简式为CH3CH(OH)COOH。
回答下列问题:
(1)TiOSO4中钛元素的化合价是____________ ,步骤①中分离硫酸亚铁溶液和滤渣的操作是___________ 。
(2)滤渣的主要成分为TiO2·xH2O,结合离子方程式解释得到滤渣的原因:________ 。
(3)从硫酸亚铁溶液中得到硫酸亚铁晶体的操作方法是____________________ ;硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应的氧化剂和还原剂的物质的量之比为______ 。
(4)步骤④中发生反应的离子方程式为______________________ 。
(5)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及____________________ 。
(6)实验室中检验溶液B中主要阳离子的方法是______________________ 。

已知:TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-,TiO2+水解成TiO2·xH2O沉淀为可逆反应;乳酸结构简式为CH3CH(OH)COOH。
回答下列问题:
(1)TiOSO4中钛元素的化合价是
(2)滤渣的主要成分为TiO2·xH2O,结合离子方程式解释得到滤渣的原因:
(3)从硫酸亚铁溶液中得到硫酸亚铁晶体的操作方法是
(4)步骤④中发生反应的离子方程式为
(5)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及
(6)实验室中检验溶液B中主要阳离子的方法是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】(Ⅰ)Q、W、X、Y、Z五种短周期元素原子序数依次增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)W、X、Y三种元素的第一电离能由大到小的顺序是__________ 。
(2) 与
与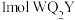 所含
所含 键的比值为
键的比值为__________ 。
(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为__________ 。
①该化合物的化学式为:__________ 。
②预测该化合物熔点应__________ 金刚石(填“高于”或“低于”)。
(Ⅱ)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5) 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的电子排布式为
的电子排布式为__________ 。
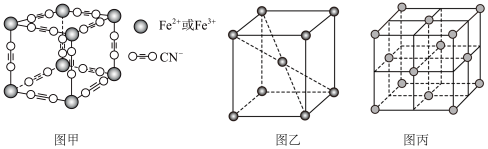
(6)普鲁士蓝俗称铁蓝,结构如图甲所示( 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为__________ 。又知该晶体中铁元素有 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为__________ 。
(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为__________ 。
(1)W、X、Y三种元素的第一电离能由大到小的顺序是
(2)
 与
与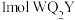 所含
所含 键的比值为
键的比值为(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为
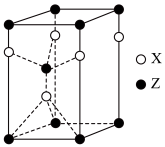
①该化合物的化学式为:
②预测该化合物熔点应
(Ⅱ)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5)
 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的电子排布式为
的电子排布式为(6)普鲁士蓝俗称铁蓝,结构如图甲所示(
 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、二氧化碳、青霉素、硝酸钾、乙醇、氨等“分子”改变过人类的世界。
(1)铁原子在基态时,外围电子排布式为____________ 。
(2)CO2的电子式为____________ ,1 mol CO2分子中含有σ键的物质的量为____________ 。
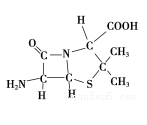
(3)6-氨基青霉烷酸的结构如图所示:
①其中C、N、O原子半径的大小关系为____________ ,电负性的大小关系为____________ ;
②其中采用sp3杂化的原子有C、____________ 。
(4)硝酸钾中NO3-的空间构型为____________ ,写出与NO3-互为等电子体的一种由前二周期元素原子构成的非极性分子化学式____________ 。
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是____________ 。
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为____________ g/cm3(用NA表示阿伏伽德罗常数)。
(1)铁原子在基态时,外围电子排布式为
(2)CO2的电子式为
(3)6-氨基青霉烷酸的结构如图所示:
①其中C、N、O原子半径的大小关系为
②其中采用sp3杂化的原子有C、
(4)硝酸钾中NO3-的空间构型为
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】一种从火法炼铜烟道灰(主要成分是 的硫酸盐,还有少量
的硫酸盐,还有少量 和
和 的氧化物)中回收铅,并制取三盐基硫酸铅(
的氧化物)中回收铅,并制取三盐基硫酸铅(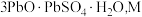 为
为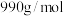 )的工艺如图:
)的工艺如图:
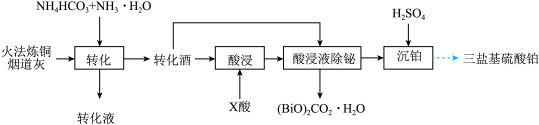
已知: 微溶于水
微溶于水
(1)写出铅原子的核外电子排布式:
_______ ,它位于元素周期表的_______ 区。
(2)转化过程温度选择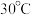 ,原因是
,原因是_______ 。
(3)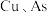 元素均进入转化液中,相关的离子分别为
元素均进入转化液中,相关的离子分别为_______ 、_______ (填离子符号)。
(4)转化渣主要成分为碳酸铅和碳酸氧铋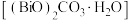 ,写出
,写出 转化为
转化为 的离子反应方程式:
的离子反应方程式:_______ 。
(5)加入适量的 酸,
酸, 酸宜为_______(填序号)。
酸宜为_______(填序号)。
(6)转化渣除铋的离子方程式为_______ 。
(7)若使用 烟道灰,最终制得纯度为
烟道灰,最终制得纯度为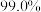 的三盐基硫酸铅
的三盐基硫酸铅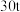 ,已知该工艺铅的回收率约为
,已知该工艺铅的回收率约为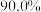 ,则烟道灰中含铅的质量分数为
,则烟道灰中含铅的质量分数为_______ 。
 的硫酸盐,还有少量
的硫酸盐,还有少量 和
和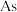 的氧化物)中回收铅,并制取三盐基硫酸铅(
的氧化物)中回收铅,并制取三盐基硫酸铅(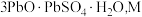 为
为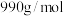 )的工艺如图:
)的工艺如图:
已知:
 微溶于水
微溶于水(1)写出铅原子的核外电子排布式:

(2)转化过程温度选择
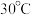 ,原因是
,原因是(3)
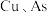 元素均进入转化液中,相关的离子分别为
元素均进入转化液中,相关的离子分别为(4)转化渣主要成分为碳酸铅和碳酸氧铋
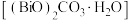 ,写出
,写出 转化为
转化为 的离子反应方程式:
的离子反应方程式:(5)加入适量的
 酸,
酸, 酸宜为_______(填序号)。
酸宜为_______(填序号)。| A.盐酸 | B.硫酸 | C.硝酸 | D.氢硫酸 |
(6)转化渣除铋的离子方程式为
(7)若使用
 烟道灰,最终制得纯度为
烟道灰,最终制得纯度为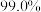 的三盐基硫酸铅
的三盐基硫酸铅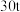 ,已知该工艺铅的回收率约为
,已知该工艺铅的回收率约为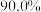 ,则烟道灰中含铅的质量分数为
,则烟道灰中含铅的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】工业上用钛铁精矿(FeTiO3)提炼TiO2的工艺流程如下:
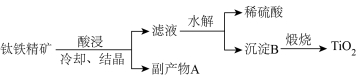
(1)写出硫酸酸浸溶解钛铁精矿的离子方程式____________ 。酸浸时为了提高浸出率,可以采取的措施为_______________ 。
(2)钛铁精矿后冷却、结晶得到的副产物A为__________ ,结晶析出A时,为保持较高的酸度不能加水,其原因可能为__________________ 。
(3)工业上将TiO2和碳粉混合加热氯化生成的TiCl4,然后在高温下用金属镁还原TiCl4得到金属钛,写出TiO2制备Ti的化学方程式:______________ 。

(1)写出硫酸酸浸溶解钛铁精矿的离子方程式
(2)钛铁精矿后冷却、结晶得到的副产物A为
(3)工业上将TiO2和碳粉混合加热氯化生成的TiCl4,然后在高温下用金属镁还原TiCl4得到金属钛,写出TiO2制备Ti的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某研究小组以 为原料制备新型耐热材料
为原料制备新型耐热材料 。
。
步骤一: 水解制备
水解制备 (实验装置如图A,夹持装置省略):滴入
(实验装置如图A,夹持装置省略):滴入 ,边搅拌边加热,使混合液升温至
,边搅拌边加热,使混合液升温至 ,保温3小时。离心分离白色沉淀
,保温3小时。离心分离白色沉淀 并洗涤,煅烧制得
并洗涤,煅烧制得 。
。
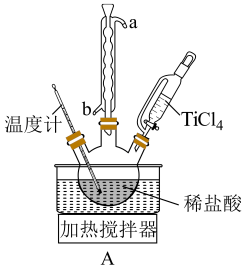
(1)装置A中冷凝水的入口为_____________ (填“a”或“b”)
(2) 反应生成
反应生成 的化学方程式为
的化学方程式为_____________________
(3)判断 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有_________________ 。
步骤二:由 制备
制备 并测定产率(实验装置如下图,夹持装置省略)
并测定产率(实验装置如下图,夹持装置省略)
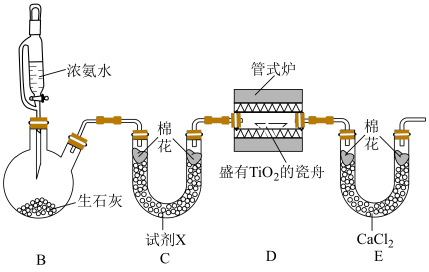
(4)装置C中试剂X为______________ 。
(5)装置D中加热至 ,反应生成
,反应生成 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为________________ 。
(6)实验中部分操作如下:
a.反应前,称取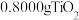 样品;
样品;
b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至 左右;
左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为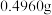 。
。
①正确的操作顺序为:a→__________________ →f(填标号);② 的产率为
的产率为_____________________ 。
 为原料制备新型耐热材料
为原料制备新型耐热材料 。
。步骤一:
 水解制备
水解制备 (实验装置如图A,夹持装置省略):滴入
(实验装置如图A,夹持装置省略):滴入 ,边搅拌边加热,使混合液升温至
,边搅拌边加热,使混合液升温至 ,保温3小时。离心分离白色沉淀
,保温3小时。离心分离白色沉淀 并洗涤,煅烧制得
并洗涤,煅烧制得 。
。
(1)装置A中冷凝水的入口为
(2)
 反应生成
反应生成 的化学方程式为
的化学方程式为(3)判断
 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有步骤二:由
 制备
制备 并测定产率(实验装置如下图,夹持装置省略)
并测定产率(实验装置如下图,夹持装置省略)
(4)装置C中试剂X为
(5)装置D中加热至
 ,反应生成
,反应生成 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(6)实验中部分操作如下:
a.反应前,称取
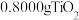 样品;
样品;b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至
 左右;
左右;e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为
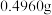 。
。①正确的操作顺序为:a→
 的产率为
的产率为
您最近一年使用:0次
【推荐3】一种以钛铁矿( ,含
,含 等杂质)为主要原料制备钛白粉
等杂质)为主要原料制备钛白粉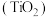 的工艺流程如图所示。
的工艺流程如图所示。
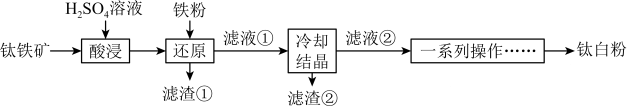
已知:①“酸浸”后钛元素主要以 形式存在;
形式存在;
② 在
在 时生成沉淀,
时生成沉淀, 时沉淀完全。
时沉淀完全。
(1)“酸浸”时,常将钛铁矿粉碎,并进行搅拌,其目的是___________ 。
(2)“酸浸”时, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)滤渣①的主要成分是___________ (填化学式)。
(4)流程中加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某化学兴趣小组在保持反应时间相同的情况下进行探究得到结果如下。保持其它反应条件不变,还原体系中
。为探究最佳反应条件,某化学兴趣小组在保持反应时间相同的情况下进行探究得到结果如下。保持其它反应条件不变,还原体系中 (Ⅲ)(
(Ⅲ)( 价的铁元素)含量随
价的铁元素)含量随 变化如图所示。
变化如图所示。
①试分析 点以后体系中
点以后体系中 (Ⅲ)含量随着
(Ⅲ)含量随着 大而增大的原因是
大而增大的原因是___________ 。
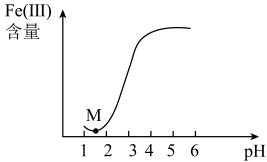
②保持其它反应条件不变,还原体系中 (Ⅲ)含量随温度变化如图所示。由图可知,还原体系中
(Ⅲ)含量随温度变化如图所示。由图可知,还原体系中 (Ⅲ)的最佳反应温度为
(Ⅲ)的最佳反应温度为___________ 
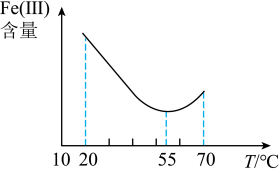
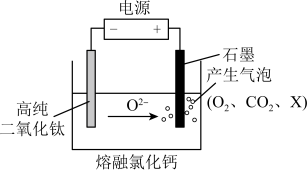
(5)如图为 剑桥法用固体二氧化钛
剑桥法用固体二氧化钛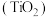 生产海绵钛的装置示意图,其原理是在较低的阴极电位下,
生产海绵钛的装置示意图,其原理是在较低的阴极电位下, (阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为
(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为___________ ,产生的气体中 的化学式为
的化学式为___________ 。
 ,含
,含 等杂质)为主要原料制备钛白粉
等杂质)为主要原料制备钛白粉 的工艺流程如图所示。
的工艺流程如图所示。
已知:①“酸浸”后钛元素主要以
 形式存在;
形式存在;②
 在
在 时生成沉淀,
时生成沉淀, 时沉淀完全。
时沉淀完全。(1)“酸浸”时,常将钛铁矿粉碎,并进行搅拌,其目的是
(2)“酸浸”时,
 发生反应的化学方程式为
发生反应的化学方程式为(3)滤渣①的主要成分是
(4)流程中加入铁粉的目的是还原体系中的
 。为探究最佳反应条件,某化学兴趣小组在保持反应时间相同的情况下进行探究得到结果如下。保持其它反应条件不变,还原体系中
。为探究最佳反应条件,某化学兴趣小组在保持反应时间相同的情况下进行探究得到结果如下。保持其它反应条件不变,还原体系中 (Ⅲ)(
(Ⅲ)( 价的铁元素)含量随
价的铁元素)含量随 变化如图所示。
变化如图所示。
①试分析
 点以后体系中
点以后体系中 (Ⅲ)含量随着
(Ⅲ)含量随着 大而增大的原因是
大而增大的原因是②保持其它反应条件不变,还原体系中
 (Ⅲ)含量随温度变化如图所示。由图可知,还原体系中
(Ⅲ)含量随温度变化如图所示。由图可知,还原体系中 (Ⅲ)的最佳反应温度为
(Ⅲ)的最佳反应温度为

(5)如图为
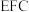 剑桥法用固体二氧化钛
剑桥法用固体二氧化钛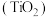 生产海绵钛的装置示意图,其原理是在较低的阴极电位下,
生产海绵钛的装置示意图,其原理是在较低的阴极电位下, (阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为
(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为 的化学式为
的化学式为
您最近一年使用:0次



