解题方法
1 .  在生产和生活中用途广泛。
在生产和生活中用途广泛。
Ⅰ. 溶液的配制及浓度的标定
溶液的配制及浓度的标定
(1) 溶液的配制
溶液的配制
①配制100mL一定浓度的 溶液需用到的仪器有
溶液需用到的仪器有___________ (填字母)。 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为___________ 。
(2) 溶液浓度的标定
溶液浓度的标定
量取10.00mL 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用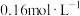
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为___________  。
。
Ⅱ. 与
与 反应的探究
反应的探究
(3)预测现象1:向 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为___________ (用离子方程式表示)。
预测现象2:向 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。
(4)实验验证:小组同学设计以下实验探究溶液中 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
①请补充表格中的数据:a=___________ 。
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是___________ 。
③实验ⅵ和ⅶ的实验现象说明溶液中 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:___________ 。
④甲同学认为实验ⅵ和ⅶ中, 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,___________ (填实验操作与现象),则说明猜想成立。
(5)请举出一种水解反应在生产或生活中的应用:___________ 。
 在生产和生活中用途广泛。
在生产和生活中用途广泛。Ⅰ.
 溶液的配制及浓度的标定
溶液的配制及浓度的标定(1)
 溶液的配制
溶液的配制①配制100mL一定浓度的
 溶液需用到的仪器有
溶液需用到的仪器有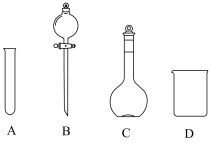
 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为(2)
 溶液浓度的标定
溶液浓度的标定量取10.00mL
 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用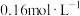
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为 。
。Ⅱ.
 与
与 反应的探究
反应的探究(3)预测现象1:向
 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为预测现象2:向
 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。(4)实验验证:小组同学设计以下实验探究溶液中
 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:| 序号 | ⅰ | ⅱ | ⅲ | ⅳ | ⅴ | ⅵ | ⅶ |
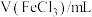 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 |
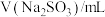 | 0 | 1.0 | 2.0 | 5.0 | a | 20.0 | 26.0 |
 | 38.0 | 37.0 | 36.0 | 33.0 | 23.0 | 18.0 | 12.0 |
| 现象 | 溶液接近无色透明 | 出现褐色沉淀 | |||||
| pH | 1.7 | 1.7 | 1.7 | 1.8 | 2.8 | 5.4 | 6.2 |
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是
③实验ⅵ和ⅶ的实验现象说明溶液中
 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:④甲同学认为实验ⅵ和ⅶ中,
 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,(5)请举出一种水解反应在生产或生活中的应用:
您最近一年使用:0次
2 . 钪(Sc)是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从“赤泥”矿(主要成分为 、
、 、
、 、
、 )中回收钪,同时生产聚合氯化铁铝[
)中回收钪,同时生产聚合氯化铁铝[ ]具有极其重要的工业价值,一种工艺流程如图所示:
]具有极其重要的工业价值,一种工艺流程如图所示:

已知:钪离子可以在不同pH下生成 (n=1~6)。请回答以下问题:
(n=1~6)。请回答以下问题:
(1)基态钪原子的价电子排布式为_______ ,过氧化氢的电子式为_______ 。
(2)“还原”步骤中发生的主要离子反应方程式为_______ 。
(3)“反萃取”时若加入的氢氧化钠大量过量,则生成的含Sc元素的粒子主要为_______ 。
(4)为了使水解步骤反应更加彻底,可以采取的措施为_______ (不能添加化学式剂,任答一条即可)。
(5)步骤X中生成聚合氯化铁铝[ ]的化学反应方程式为
]的化学反应方程式为_______ 。
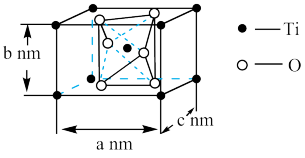
(6)如图是 晶胞的示意图,晶胞中含有的氧原子数目为
晶胞的示意图,晶胞中含有的氧原子数目为_______ 个,已知Ti原子的配位数为6,则O原子的配位数为_______ ,该晶体的密度约为_______  。(NA取
。(NA取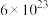 ,结果用含a、b、c的最简分数表达式表示)。
,结果用含a、b、c的最简分数表达式表示)。
 、
、 、
、 、
、 )中回收钪,同时生产聚合氯化铁铝[
)中回收钪,同时生产聚合氯化铁铝[ ]具有极其重要的工业价值,一种工艺流程如图所示:
]具有极其重要的工业价值,一种工艺流程如图所示:
已知:钪离子可以在不同pH下生成
 (n=1~6)。请回答以下问题:
(n=1~6)。请回答以下问题:(1)基态钪原子的价电子排布式为
(2)“还原”步骤中发生的主要离子反应方程式为
(3)“反萃取”时若加入的氢氧化钠大量过量,则生成的含Sc元素的粒子主要为
(4)为了使水解步骤反应更加彻底,可以采取的措施为
(5)步骤X中生成聚合氯化铁铝[
 ]的化学反应方程式为
]的化学反应方程式为(6)如图是
 晶胞的示意图,晶胞中含有的氧原子数目为
晶胞的示意图,晶胞中含有的氧原子数目为 。(NA取
。(NA取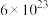 ,结果用含a、b、c的最简分数表达式表示)。
,结果用含a、b、c的最简分数表达式表示)。
您最近一年使用:0次
名校
解题方法
3 . 某学习小组查阅资料发现:①硫元素处于-2价和+4价的物质有较强的还原性,Fe3+具有较强的氧化性;②大多数自发的氧化还原反应是放热反应。该学习小组进行了一系列探究:
(1)利用下图装置探究SO2与FeCl3溶液的反应(夹持装置已略去):
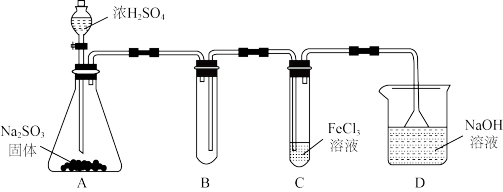
①用FeCl3晶体配制一定浓度FeCl3溶液的方法是_______ 。
②实验开始一段时间后,C中溶液由深黄色变为浅绿色,据此写出C中反应的离子方程式:_______ ,检验有Fe2+(溶液中仍有少量Fe3+)的方法是:取少量C试管溶液,加入无色溶液_______ (仅填一种物质化学式),生成_______ (现象),证明有Fe2+。
③取少量反应后的C中溶液,加入盐酸酸化,再加入Ba(NO3)2溶液,产生白色沉淀,即可证明反应生成了 ,该做法
,该做法_______ (填“合理”或“不合理”),理由是_______ 。
(2)利用0.10mol/L的NaHS溶液a(常温pH=8.1)和0.10mol/LFeCl3溶液b(常温pH=1.3)探究NaHS和FeCl3的反应:
①常温下,将溶液a和溶液b按3:1的体积比混合于试管中,发现有红褐色沉淀生成,仔细观察还有一些黄色固体,该红褐色沉淀是_______ ,黄色固体是_______ 。
②学习小组继续将溶液a和溶液b按3:1的体积比混合,分装在两支试管中,第一支置于沸水浴中,第二支置于冰水浴中,发现第一支试管只有红褐色沉淀,并产生臭鸡蛋气味气体,原因是_______ ;第二支试管只有黄色沉淀,没有气体产生,原因是_______ 。
(1)利用下图装置探究SO2与FeCl3溶液的反应(夹持装置已略去):

①用FeCl3晶体配制一定浓度FeCl3溶液的方法是
②实验开始一段时间后,C中溶液由深黄色变为浅绿色,据此写出C中反应的离子方程式:
③取少量反应后的C中溶液,加入盐酸酸化,再加入Ba(NO3)2溶液,产生白色沉淀,即可证明反应生成了
 ,该做法
,该做法(2)利用0.10mol/L的NaHS溶液a(常温pH=8.1)和0.10mol/LFeCl3溶液b(常温pH=1.3)探究NaHS和FeCl3的反应:
①常温下,将溶液a和溶液b按3:1的体积比混合于试管中,发现有红褐色沉淀生成,仔细观察还有一些黄色固体,该红褐色沉淀是
②学习小组继续将溶液a和溶液b按3:1的体积比混合,分装在两支试管中,第一支置于沸水浴中,第二支置于冰水浴中,发现第一支试管只有红褐色沉淀,并产生臭鸡蛋气味气体,原因是
您最近一年使用:0次
2022-05-14更新
|
431次组卷
|
2卷引用:广东省新高考普通高中2022届高三联合质量测评冲刺模拟考试化学试题
名校
解题方法
4 . 化学实验小组探究0.1mol/LNa2S溶液与0.1mol/LFeCl3溶液的反应。查阅文献得相关信息如下:
(1)【猜想预测】
预测1:若产生红褐色沉淀,说明发生双水解反应;
预测2:若产生黑色沉淀时,说明发生复分解反应:
预测3:Fe3+具有___ ,若产生黄色沉淀,说明发生氧化还原反应。
(2)【实验探究】
实验Ⅰ.向装有5mL、0.1mol/L的FeCl3的溶液中滴加1mL、0.1mol/LNa2S溶液,迅速生成黑色沉淀,由此可知,预测1、3不成立,预测2成立。试解释预测2成立而预测1不成立的原因:___ 。实验过程中,该小组同学发现黑色沉淀放置一段时间后逐渐消失,并有黄色沉淀生成。为探明原因,分离滤渣和滤液进行如下实验:
实验Ⅱ.为探究实验Ⅰ中Fe2S3后续发生氧化还原反应的原因,该组同学进行如下探究实验:【限选试剂:Fe2S3、稀盐酸、稀硝酸、饱和FeCl3溶液、饱和Fe(NO3)3溶液、H2O2】

| 物质 | 相关信息 |
| 0.1mol/LNa2S溶液 | 无色透明液体,pH=12 |
| 0.1mol/LFeCl3溶液 | 黄褐色透明液体,pH=2 |
| S单质 | 微溶于酒精,难溶于水,含硫的酒精溶于水会出现乳白色浑浊 |
| Fe(OH)3 | 红褐色固体,Ksp=1.1×10-36 |
| Fe2S3 | 黑色固体,Ksp=1.0×10-88 |
预测1:若产生红褐色沉淀,说明发生双水解反应;
预测2:若产生黑色沉淀时,说明发生复分解反应:
预测3:Fe3+具有
(2)【实验探究】
实验Ⅰ.向装有5mL、0.1mol/L的FeCl3的溶液中滴加1mL、0.1mol/LNa2S溶液,迅速生成黑色沉淀,由此可知,预测1、3不成立,预测2成立。试解释预测2成立而预测1不成立的原因:
| 实验 | 操作 | 现象 | 结论 |
| ① | 取滤渣用酒精充分浸取,取上层浸液少许加入到盛有蒸馏水的试管中 | 滤渣中含有S | |
| ② | 取滤液加入几滴K3[Fe(CN)6]溶液 | 滤液中含有Fe2+;证明Fe2S3后续发生了氧化还原反应 |

| 实验 | 操作 | 现象 | 结论 |
| ① | 往A中滴加 | A中黑色固体消失,并有黄色沉淀生成;B中有黑色沉淀生成 | Fe2S3在酸性条件下发生了氧化还原,反应的离子反应方程式: |
| ② | 往A中滴加 | A中黑色固体消失,并有黄色沉淀生成;B中无黑色沉淀生成 | Fe3+可以氧化Fe2S3,反应的离子反应方程式: |
您最近一年使用:0次
名校
解题方法
5 . Ⅰ.亚硫酸氢钠,在染料、造纸制革、化学合成等工业中可用作还原剂。
(1)实验室以浓硫酸、铜与 溶液为原料制取少量
溶液为原料制取少量 的装置如图所示。
的装置如图所示。

①仪器a的名称是___________ 。为使分液漏斗内的浓硫酸顺利滴下,需进行的操作为将分液漏斗上部的玻璃塞打开或___________ 。
②装置D用于吸收尾气,当观察到D中溶液即将褪为无色时熄灭酒精灯,其中发生反应的离子方程式为___________ 。
Ⅱ.小组同学欲探究 与
与 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。
已知:氯化亚铜( )是不溶于水的白色沉淀
)是不溶于水的白色沉淀
假设1: 与
与 仅发生双水解反应
仅发生双水解反应
假设2: 可以还原
可以还原
设计实验如下:
Ⅰ.向

 溶液中加入
溶液中加入

 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。
Ⅱ.向Ⅰ所得绿色溶液中加入适量 固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
(2)实验证实假设___________ 合理,设计实验验证实验Ⅱ中产生的无色气体为 :
:___________ 。
(3)从平衡原理角度解释加入 后产生实验Ⅱ中现象的原因:
后产生实验Ⅱ中现象的原因:___________ 。
(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差 [其中
[其中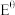 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
①根据上述实验结论,推测甲、乙两实验现象的区别:___________ (写出两条即可)。
②根据所查资料,解释产生上述现象的原因为___________ 。
(1)实验室以浓硫酸、铜与
 溶液为原料制取少量
溶液为原料制取少量 的装置如图所示。
的装置如图所示。
①仪器a的名称是
②装置D用于吸收尾气,当观察到D中溶液即将褪为无色时熄灭酒精灯,其中发生反应的离子方程式为
Ⅱ.小组同学欲探究
 与
与 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。已知:氯化亚铜(
 )是不溶于水的白色沉淀
)是不溶于水的白色沉淀假设1:
 与
与 仅发生双水解反应
仅发生双水解反应假设2:
 可以还原
可以还原
设计实验如下:
Ⅰ.向


 溶液中加入
溶液中加入

 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。Ⅱ.向Ⅰ所得绿色溶液中加入适量
 固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。(2)实验证实假设
 :
:(3)从平衡原理角度解释加入
 后产生实验Ⅱ中现象的原因:
后产生实验Ⅱ中现象的原因:(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差
 [其中
[其中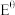 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:| 编号 | 甲 | 乙 |
| 实验 |  |  |
②根据所查资料,解释产生上述现象的原因为
您最近一年使用:0次
2022-01-21更新
|
740次组卷
|
3卷引用: 广东省深圳市光明区2021-2022学年高三上学期(1月)第二次调研测试化学试题
广东省深圳市光明区2021-2022学年高三上学期(1月)第二次调研测试化学试题(已下线)化学-2022年高考押题预测卷02(广东卷)重庆市天星桥中学2021-2022学年高三下学期学业质量调研抽测化学试题
名校
解题方法
6 . 铋是一种稀有金属,铋及其化合物在工业生产中用途广泛,如氯氧化铋常用于电子设备、汽车装饰材料、塑料助剂及生产干电池阴极。以下是一种用铋精矿(主要成分是Bi2S3还含有FeS2、 Cu2S、PbO2及不溶性杂质)制备 BiOCl的一种方法,其流程如图:

已知: ① Fe(OH)3开始沉淀的 pH值为2.7,沉淀完全时的 pH值为3.7。
② 对浸出渣的处理,直至得到产品,都在封闭的管道内进行。
③ pH>3,则 BiCl3极易水解生成不溶性的 BiOCl 沉淀。
请回答以下问题:
(1)铋精矿在浸取时会先进行粉碎,目的是___________ 。
(2)加压氧化氨浸过程中,已知 CuS2发生如下反应: ,
, 生成
生成 ,FeS2在此过程中也生成某氧化物,请写出发生反应的化学方程式
,FeS2在此过程中也生成某氧化物,请写出发生反应的化学方程式___________ 。
(3)操作Ⅰ为:___________ 。
(4)根据流程分析,盐酸羟胺在反应中起到什么作用:___________ 。
(5)流程中生成 BiOCl 的离子方程式:___________ 。
(6)滤液 3 中含有的金属阳离子有:___________ 。

已知: ① Fe(OH)3开始沉淀的 pH值为2.7,沉淀完全时的 pH值为3.7。
② 对浸出渣的处理,直至得到产品,都在封闭的管道内进行。
③ pH>3,则 BiCl3极易水解生成不溶性的 BiOCl 沉淀。
请回答以下问题:
(1)铋精矿在浸取时会先进行粉碎,目的是
(2)加压氧化氨浸过程中,已知 CuS2发生如下反应:
 ,
, 生成
生成 ,FeS2在此过程中也生成某氧化物,请写出发生反应的化学方程式
,FeS2在此过程中也生成某氧化物,请写出发生反应的化学方程式(3)操作Ⅰ为:
(4)根据流程分析,盐酸羟胺在反应中起到什么作用:
(5)流程中生成 BiOCl 的离子方程式:
(6)滤液 3 中含有的金属阳离子有:
您最近一年使用:0次
2021-03-03更新
|
642次组卷
|
4卷引用:广东省珠海市2021届高三第一次学业质量监测化学试题
广东省珠海市2021届高三第一次学业质量监测化学试题(已下线)押山东卷第16题 化工流程综合题-备战2021年高考化学临考题号押题(山东卷)2022届重庆市缙云教育联盟高三第〇次诊断性检测化学试题河南省范县第一中学2021-2022学年高二上学期期中检测化学试题



