名校
1 . 下列表述的化学用语正确的是
| A.Fe2+可用K3[Fe(CN)6)]溶液进行检验:3Fe2++2[Fe(CN)6)]3-=Fe3[Fe(CN)6)]2↓ |
B.NaHCO3溶液水解方程式: +H2O +H2O H3O++ H3O++ |
C.泡沫灭火器原理:3 +2Al3++3H2O=2Al(OH)3↓+3CO2↑ +2Al3++3H2O=2Al(OH)3↓+3CO2↑ |
| D.向苯酚钠溶液中通入少量的CO2气体:2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3 |
您最近一年使用:0次
名校
解题方法
2 . 请按照下列要求回答问题:
(1)硫化钠水解的离子方程式:______ 。
(2)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理______ 。
(3)将25℃下pH=12的Ba(OH)2溶液a L与pH=1的HCl溶液b L混合,若所得混合液为中性,则a:b=_____ 。(溶液体积变化忽略不计)。
(4)pH=3的NH4Cl溶液,由水电离出的c(H+)=__ 。
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留的c(Fe3+)<10-5 mol·L-1),则溶液的pH应大于____ 。
(6)用如图装置进行模拟电解NO2气体实验,可回收硝酸。

①外接电源a极为_____ 极,左室发生的电极反应式为_______ 。
②若有标准状况下2.24 LNO2被吸收,通过质子交换膜(只允许质子通过)的H+为__ mol。
(7)在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。

①Ag2CrO4的Ksp为______ 。
②由Y点变到Z点的方法______ 。
(1)硫化钠水解的离子方程式:
(2)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理
(3)将25℃下pH=12的Ba(OH)2溶液a L与pH=1的HCl溶液b L混合,若所得混合液为中性,则a:b=
(4)pH=3的NH4Cl溶液,由水电离出的c(H+)=
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留的c(Fe3+)<10-5 mol·L-1),则溶液的pH应大于
(6)用如图装置进行模拟电解NO2气体实验,可回收硝酸。

①外接电源a极为
②若有标准状况下2.24 LNO2被吸收,通过质子交换膜(只允许质子通过)的H+为
(7)在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。

①Ag2CrO4的Ksp为
②由Y点变到Z点的方法
您最近一年使用:0次
3 . 物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看做化学平衡。请根据所学的知识回答:
(1)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为__ 。
(2)B为0.1mol·L-1NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:__ 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入__ 以抑制其水解,若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为_ 。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)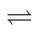 Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
①100mL蒸馏水中;②100mL0.2mol·L-1AgNO3溶液中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__ (填序号);向②中加入足量氯化银后,氯离子的浓度为__ mol·L-1。
(1)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为
(2)B为0.1mol·L-1NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)
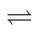 Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:①100mL蒸馏水中;②100mL0.2mol·L-1AgNO3溶液中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
您最近一年使用:0次
2020-06-16更新
|
110次组卷
|
4卷引用:四川省遂宁市船山区第二中学校2019-2020学年高二下学期期中考试化学试题
名校
解题方法
4 . (1)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=______ mol•L﹣1;往溶液中加入少量NaOH固体,则溶液中
_____ (填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:______ 。
(2)甲醇(CH3OH)是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,甲醇在_____ 极反应(填“正”或“负”),电极反应式为_____ 。
(3)泡沫灭火器的原理:________________________ (用离子反应方程式表示)。
(4)Na2CO3溶液中所有离子的大小关系是:____________________ 。

(2)甲醇(CH3OH)是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,甲醇在
(3)泡沫灭火器的原理:
(4)Na2CO3溶液中所有离子的大小关系是:
您最近一年使用:0次
名校
解题方法
5 . 常温下,下列各组离子在特定溶液中一定能大量共存的是
A.pH=12的澄清的溶液中:K+、Na+、MnO 、SO 、SO |
B.c(Al3+)=0.1mol•L﹣1的溶液中:Na+、Cl﹣、HCO 、SO 、SO |
C.甲基橙呈红色的溶液中:NH 、Ba2+、AlO 、Ba2+、AlO 、Cl﹣ 、Cl﹣ |
D.加入少量铝粉后能产生氢气的溶液中:NH 、Fe2+、NO 、Fe2+、NO 、SO 、SO |
您最近一年使用:0次
2020-06-15更新
|
106次组卷
|
2卷引用:四川省遂宁市射洪县射洪中学校2019-2020学年高二下学期期中考试化学试题
6 . 某无色溶液X,由Na+、Mg2+、Ba2+、Al3+、AlO2-、MnO 、CO
、CO 、SO
、SO 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
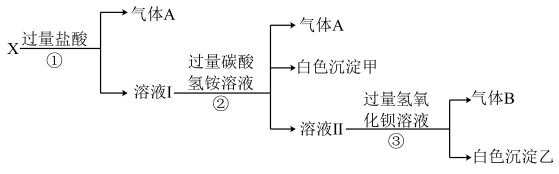
(1)气体A的成分是_______ (填电子式),气体B的成分是_______ (填结构式)
(2)X溶液中一定不存在的离子是______________ 。
(3)写出步骤①中发生反应的所有离子方程式:________________ 。
(4)写出步骤②中形成白色沉淀的离子方程式:________________ 。
(5)通过上述实验,溶液X中不能确定是否存在的离子是______________ ;只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是__________________ 。
 、CO
、CO 、SO
、SO 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
(1)气体A的成分是
(2)X溶液中一定不存在的离子是
(3)写出步骤①中发生反应的所有离子方程式:
(4)写出步骤②中形成白色沉淀的离子方程式:
(5)通过上述实验,溶液X中不能确定是否存在的离子是
您最近一年使用:0次
2020-06-10更新
|
181次组卷
|
2卷引用:四川省眉山市仁寿第一中学北校区2019-2020学年高二下学期6月月考(期中)理综化学试题
名校
7 . 下列实验操作能达到目的的是
①用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体②用加热蒸发K2CO3溶液的方法获得K2CO3晶体③用Na2S溶液和CuSO4溶液反应制取CuS固体④加热MgCl2溶液制取MgCl2固体
①用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体②用加热蒸发K2CO3溶液的方法获得K2CO3晶体③用Na2S溶液和CuSO4溶液反应制取CuS固体④加热MgCl2溶液制取MgCl2固体
| A.②③ | B.①② | C.③④ | D.①③ |
您最近一年使用:0次
2020-04-28更新
|
125次组卷
|
13卷引用:四川省邻水实验学校2017-2018学年高二上学期第三次月考化学试题
四川省邻水实验学校2017-2018学年高二上学期第三次月考化学试题四川省广元川师大万达中学2019-2020学年高二上学期期末教学质量检测化学试题四川省遂宁市第二中学校2017-2018学年高二下学期期中考试化学试题2015-2016学年湖北省孝感市六校教学联盟高二上期末联考化学试卷2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷黑龙江省齐齐哈尔市第八中学2017-2018学年高二12月月考化学试题山西省晋城一中2017--2018学年度高二12月月考化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题黑龙江省大庆市铁人中学2019-2020学年高二上学期期末考试化学试题江苏省镇江市吕叔湘中学2019-2020学年高二下学期4月诊断考试化学试题吉林省长春外国语学校2020-2021学年高二下学期期初考试化学试题黑龙江省龙西北地区八校2020-2021学年高二下学期3月联考化学试题山西省太原市英才学校2021-2022学年高二上学期第二次月考化学试题
名校
8 . FeCl3溶液与下列物质的反应,其中与Fe3+的水解无关的是
①紫色石蕊试液 ②碘化钾 ③煮沸的蒸馏水 ④硫化氢 ⑤铜粉 ⑥小苏打溶液
①紫色石蕊试液 ②碘化钾 ③煮沸的蒸馏水 ④硫化氢 ⑤铜粉 ⑥小苏打溶液
| A.①②③④ | B.②④⑤ | C.③⑤⑥ | D.①⑥ |
您最近一年使用:0次
9 . 下列相关方程式或离子方程式正确的是
A.碳酸的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
B.向沸水中滴加饱和FeCl3溶液制胶体:Fe3++3 H2O Fe(OH)3(胶体)+3 H+ Fe(OH)3(胶体)+3 H+ |
| C.泡沫灭火器原理可表示为:2Al3++3CO32-+3 H2O=2Al(OH)3↓+3CO2↑ |
D.NaClO溶液呈碱性:ClO—+H2O HClO+OH- HClO+OH- |
您最近一年使用:0次
名校
10 . 下列方程式书写正确的是
A.HCO3−的电离方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
B.泡沫灭火器的原理:Al3++3HCO3-  Al(OH)3↓+3CO2↑ Al(OH)3↓+3CO2↑ |
C.NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+ NH3·D2O+H+ |
D.Na2S显碱性原因:S2-+2H2O H2S+2OH- H2S+2OH- |
您最近一年使用:0次



