1 . 以钴渣(主要成分是 、
、 含少量Ni、
含少量Ni、 等杂质)为原料制取
等杂质)为原料制取 ,工艺流程如下.下列说法错误的是
,工艺流程如下.下列说法错误的是
①碱性条件下, 会转化成
会转化成
② 被萃取原理:
被萃取原理:
 、
、 含少量Ni、
含少量Ni、 等杂质)为原料制取
等杂质)为原料制取 ,工艺流程如下.下列说法错误的是
,工艺流程如下.下列说法错误的是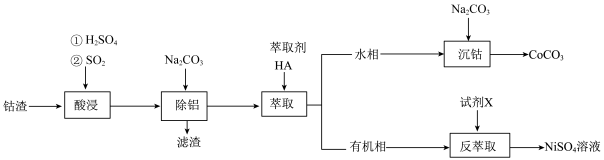
①碱性条件下,
 会转化成
会转化成
②
 被萃取原理:
被萃取原理:
| A.试剂X为稀硫酸 |
B.“酸浸”中 反应的离子方程式为 反应的离子方程式为 |
| C.为保证工艺所得产品的纯度,萃取过程中,添加萃取剂应采用少量多次的方法进行 |
D.“沉钴”时,应向上一步所得含 的溶液中逐滴滴加 的溶液中逐滴滴加 溶液,以提高 溶液,以提高 产率 产率 |
您最近一年使用:0次
解题方法
2 . 碳酸铈[ ]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备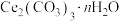 的工艺流程如下,下列说法正确的是
的工艺流程如下,下列说法正确的是

 ]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备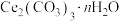 的工艺流程如下,下列说法正确的是
的工艺流程如下,下列说法正确的是
| A.“焙烧”时可使用陶瓷容器 |
| B.滤渣Ⅰ的成分只有2种 |
| C.“除铝”过程中的絮凝剂可以是硅酸胶体 |
D.“沉铈”过程离子方程式为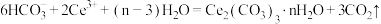 |
您最近一年使用:0次
2023-11-23更新
|
223次组卷
|
2卷引用:山东省济南市2023-2024学年高三上学期11月期中考试化学试题
名校
解题方法
3 . 银项链因表面产生硫化银而变得暗沉无光,可利用原电池原理使其恢复原貌:将银项链和药片包装铝箔接触后浸泡在食盐溶液中,银项链会迅速变得光亮如新。若继续浸泡一段时间后可观察到溶液中出现白色胶状沉淀,同时产生具有臭鸡蛋气味的气体。下列叙述错误的是
| A.溶液中钠离子向铝箔移动 |
| B.在银项链表面上的反应式为Ag2S+2e-=2Ag+S2- |
| C.铝箔表面的反应式为Al-3e-+3OH-=Al(OH)3 |
| D.继续浸泡时,溶液中反应的离子方程式为 2Al3++3S2-+6H2O=2Al(OH)3 ↓+3H2S ↑ |
您最近一年使用:0次
4 . 下列离子方程式正确的是
A.用次氯酸钠溶液吸收少量二氧化硫气体: |
B.少量草酸溶液加入到酸性高锰酸钾溶液中: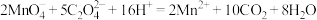 |
C.向 溶液中加入 溶液中加入 溶液得到沉淀的化学式可以表示为 溶液得到沉淀的化学式可以表示为 ,则发生的离子方程式为 ,则发生的离子方程式为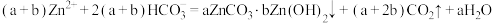 |
D.用酸性重铬酸钾溶液测定白酒中乙醇的含量: |
您最近一年使用:0次
解题方法
5 . 化合物甲、乙、丙、丁分别由H+、Na+、Al3+、Ba2+、OH-、Cl-、 离子中的两种组成,它们之间可发生下图所示转化,下列说法正确的是
离子中的两种组成,它们之间可发生下图所示转化,下列说法正确的是
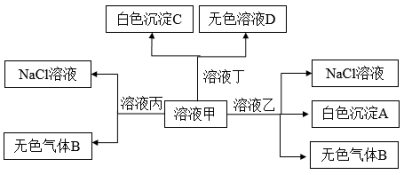
 离子中的两种组成,它们之间可发生下图所示转化,下列说法正确的是
离子中的两种组成,它们之间可发生下图所示转化,下列说法正确的是
| A.甲为AlCl3,乙为NaHCO3 |
| B.Al3+、Ba2+、Cl-能大量共存于溶液丙中 |
| C.白色沉淀A为Al(OH)3 |
| D.白色沉淀C不能溶于强酸 |
您最近一年使用:0次
解题方法
6 . 某固体混合物X,含有Al2(SO4)3、FeCl3、Na2CO3和KCl中的几种,进行如下实验:
①X与水作用有气泡冒出,得到沉淀Y和碱性溶液Z;
②沉淀Y与足量NaOH溶液作用,沉淀部分溶解。
下列说法正确的是
①X与水作用有气泡冒出,得到沉淀Y和碱性溶液Z;
②沉淀Y与足量NaOH溶液作用,沉淀部分溶解。
下列说法正确的是
| A.混合物X中必定含有Al2(SO4)3、FeCl3、Na2CO3 |
| B.溶液Z中溶质一定只含有钠盐 |
| C.灼烧沉淀Y,可以得到氧化铝和氧化铁的混合物 |
| D.往溶液Z中先加入盐酸再加氯化钡溶液可以确定混合物X中是否含有KCl |
您最近一年使用:0次
名校
解题方法
7 . 有一无色溶液,仅含有K+、Al3+、Mg2+、 、Cl-、
、Cl-、 、
、
 、
、 中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是
中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是
 、Cl-、
、Cl-、 、
、
 、
、 中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是
中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是A.肯定有Al3+、 、Cl-,可能有 、Cl-,可能有 | B.肯定没有 、 、 、 、 |
| C.肯定有Al3+、Mg2+、Cl-,可能有K+ | D.肯定有K+、Al3+、 ,可能有 ,可能有 |
您最近一年使用:0次
2020-09-25更新
|
265次组卷
|
2卷引用:山东省邹城市兖矿第一中学2021届高三上学期9月份月考化学试题



