1 . 25℃时,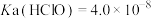 ,
,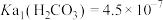 ,
, ,有关NaClO溶液说法正确的是
,有关NaClO溶液说法正确的是
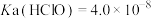 ,
,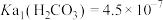 ,
, ,有关NaClO溶液说法正确的是
,有关NaClO溶液说法正确的是| A.长期露置在空气中,pH增大,漂白能力减弱 |
B. NaClO溶液中, NaClO溶液中,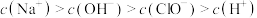 |
C.25℃, 的NaClO和HClO的混合溶液中, 的NaClO和HClO的混合溶液中,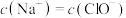 |
D.通入少量 ,反应的离子方程式为 ,反应的离子方程式为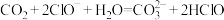 |
您最近一年使用:0次
解题方法
2 . 电解质在工农业生产和社会生活中的应用越来越广泛。回答下列问题:
(1)常温下,0.1 mol∙L−1的CH3COOH溶液与pH=13的NaOH溶液等体积混合后,溶液中的pH_____ 7(填“>”、“<”或“=”)。
(2)明矾常用作净水剂,请用离子方程式解释其净水原理_____ 。
(3)硫氢化钠(NaHS)常用作有机合成的中间体,其水溶液显碱性。则NaHS溶液中Na+、H+、HS-、OH-离子浓度由大到小的顺序为_____ 。
(4)碳酸钠的水溶液中存在着多种离子和分子,以下关系式正确的是_____ (填字母序号)。
a.c(Na+)+c(H+)=c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
b.c(Na+)=2c(CO )+2c(HCO
)+2c(HCO )+2c(H2CO3)
)+2c(H2CO3)
c.c(OH-)=c(H+)+c(HCO )+c(H2CO3)
)+c(H2CO3)
(5)常温下,0.1 mol∙L−1的H2SO4溶液与pH=13的KOH溶液等体积混合后,混合溶液pH=_____ 。(已知lg2=0.3;lg5=0.7)
(1)常温下,0.1 mol∙L−1的CH3COOH溶液与pH=13的NaOH溶液等体积混合后,溶液中的pH
(2)明矾常用作净水剂,请用离子方程式解释其净水原理
(3)硫氢化钠(NaHS)常用作有机合成的中间体,其水溶液显碱性。则NaHS溶液中Na+、H+、HS-、OH-离子浓度由大到小的顺序为
(4)碳酸钠的水溶液中存在着多种离子和分子,以下关系式正确的是
a.c(Na+)+c(H+)=c(CO
 )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)b.c(Na+)=2c(CO
 )+2c(HCO
)+2c(HCO )+2c(H2CO3)
)+2c(H2CO3)c.c(OH-)=c(H+)+c(HCO
 )+c(H2CO3)
)+c(H2CO3)(5)常温下,0.1 mol∙L−1的H2SO4溶液与pH=13的KOH溶液等体积混合后,混合溶液pH=
您最近一年使用:0次



