2024·黑龙江·模拟预测
1 . 数字化实验是研究化学变化的重要手段,为验证次氯酸光照分解的产物,某同学采用三种传感器分别测得氯水光照过程中pH、Cl-浓度、 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是
 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是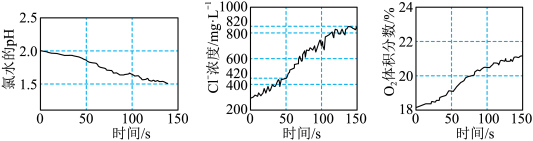
A.从0s到150s,溶液pH降低的原因是 右移 右移 |
B.氯水在光照过程中可能出现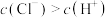 |
C.从50 s到150 s, 的平均生成速率约为 的平均生成速率约为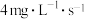 |
D.从0 s到150 s,溶液中 增加到起始浓度的 增加到起始浓度的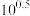 倍 倍 |
您最近半年使用:0次
名校
解题方法
2 . 在不同温度下,水溶液中 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是
 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是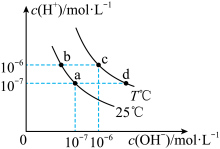
A.c点对应的溶液 ,溶液呈弱酸性 ,溶液呈弱酸性 |
B.b点对应的溶液中可以大量共存: 、 、 、 、 、 、 |
C.若a点表示 和 和 的混合溶液,则该溶液中的离子浓度大小为: 的混合溶液,则该溶液中的离子浓度大小为: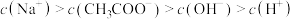 |
D.若d点表示某等浓度、等体积的 和 和 混合溶液,则溶液中的离子浓度存在如下关系: 混合溶液,则溶液中的离子浓度存在如下关系: |
您最近半年使用:0次
解题方法
3 . 常温下, 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是
 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是A. 溶液中存在平衡: 溶液中存在平衡: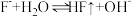 |
B.加热, 溶液的碱性增强 溶液的碱性增强 |
C. 溶液中: 溶液中: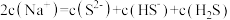 |
D. 溶液中: 溶液中: |
您最近半年使用:0次
4 . NA为阿伏加德罗常数的值,下列说法不正确的是
| A.1molHCN中含π键的数目为NA |
| B.6.5gZn与一定量浓硫酸反应完全溶解,转移的电子数为0.2NA |
C.将1molNH4CI溶于稀氨水中使溶液呈中性,溶液中 数目为NA 数目为NA |
| D.23gNa与O2充分反应生成Na2O和Na2O2的混合物,消耗O2的分子数在0.25NA和0.5NA之间 |
您最近半年使用:0次
解题方法
5 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近半年使用:0次
6 . 下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中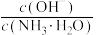 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近半年使用:0次
7 . 常温下,向0.1 的
的 溶液中加入一定量的NaOH溶液,当溶液中存在
溶液中加入一定量的NaOH溶液,当溶液中存在
 时,溶液中的主要溶质为
时,溶液中的主要溶质为
 的
的 溶液中加入一定量的NaOH溶液,当溶液中存在
溶液中加入一定量的NaOH溶液,当溶液中存在
 时,溶液中的主要溶质为
时,溶液中的主要溶质为A. | B.NaHS | C.NaHS和 | D. 和NaOH 和NaOH |
您最近半年使用:0次
8 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.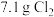 通入水中并充分反应,转移电子数目小于 通入水中并充分反应,转移电子数目小于 |
B.标准状况下, 中电子数目为 中电子数目为 |
C.向 溶液中通氨气至中性, 溶液中通氨气至中性, 目大于 目大于 |
D.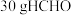 中含有 中含有 键数目为 键数目为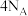 |
您最近半年使用:0次
9 . 已知 的
的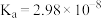 ,
, 的
的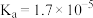 ,下列有关说法正确的是
,下列有关说法正确的是
 的
的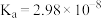 ,
, 的
的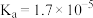 ,下列有关说法正确的是
,下列有关说法正确的是A.温度一定时在 的叠氮酸中加入少量 的叠氮酸中加入少量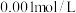 的稀盐酸,溶液的 的稀盐酸,溶液的 不会改变 不会改变 |
B.等浓度等体积的 和溶液 和溶液 前者所含离子总数比后者多 前者所含离子总数比后者多 |
C.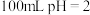 的新制氯水中: 的新制氯水中: |
D.将 通入 通入 溶液中,若溶液呈中性,则溶液中存在4种微粒 溶液中,若溶液呈中性,则溶液中存在4种微粒 |
您最近半年使用:0次
10 . 缓冲溶液是指加少量水稀释或外加少量酸、碱,自身pH不发生显著变化的溶液。1L含1mol乳酸(HLac)和1mol乳酸钠(NaLac)的溶液就是一种缓冲溶液,该溶液的pH为3.85。下图是此缓冲溶液的pH随通入HCl(g)或加入NaOH(s)的物质的量变化的示意图(溶液体积保持1L),已知lg3=0.48。下列说法错误的是
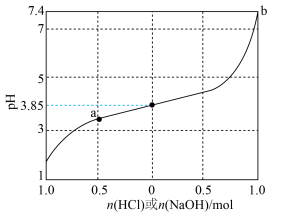
A.此缓冲溶液中(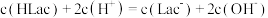 |
| B.通过计算可得出,a点溶液的pH约为3.37 |
| C.根据图像可以判断,b点溶液已失去缓冲能力 |
D.当加入NaOH,且横坐标为0.5时,对应溶液中(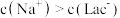 |
您最近半年使用:0次



