名校
1 .  是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是
 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.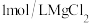 溶液中 溶液中 的数目小于 的数目小于 |
B. 与足量水反应转移的电子数目为 与足量水反应转移的电子数目为 |
C.标准状况下, 盐酸含有 盐酸含有 个 个 分子 分子 |
D.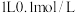 的 的 溶液中 溶液中 和 和 离子数之和为 离子数之和为 |
您最近一年使用:0次
2024-02-14更新
|
142次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 常温下,下列有关溶液的说法一定正确的是
A.NaHCO3溶液加水稀释,c(Na+)与c(HCO )的比值将减小 )的比值将减小 |
| B.pH=1的一元酸和pH=13的一元碱等体积混合后:c(OH-)=c(H+) |
C.0.1 mol·L-1硫酸铵溶液中:c(NH ) > c(SO ) > c(SO ) >c(H+)>c(OH-) ) >c(H+)>c(OH-) |
| D.0.1 mol·L-1硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
您最近一年使用:0次
名校
解题方法
3 . 填空题(共12分)
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c( )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值____ 7(填“>”、“<”或“=”,下同),混合前c(NH3·H2O)_____ c(HCl)
(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者______ 后者。
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______ 。
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的________ 。
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为________ 。
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c(
 )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
名校
解题方法
4 . 如图所示,某兴趣小组用油性笔在一小块覆铜板上写上“化学”,然后浸入盛有 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中 与
与 之比为2:3。下列说法不正确的是
之比为2:3。下列说法不正确的是

 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中 与
与 之比为2:3。下列说法不正确的是
之比为2:3。下列说法不正确的是
A.反应后的溶液中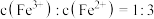 |
B.反应的离子方程式为 |
C.反应后的溶液中 |
D.使反应后的溶液再生为 溶液,可通过加入足量铁粉,过滤,向滤液中通入 溶液,可通过加入足量铁粉,过滤,向滤液中通入 来实现 来实现 |
您最近一年使用:0次
名校
5 . 用0.10 mol·L-1 NaOH溶液滴定20.0 mL0.10 mol·L-1 溶液,溶液pH和温度随
溶液,溶液pH和温度随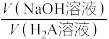 的变化曲线如图所示,下列说法不正确的
的变化曲线如图所示,下列说法不正确的

 溶液,溶液pH和温度随
溶液,溶液pH和温度随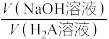 的变化曲线如图所示,下列说法不正确的
的变化曲线如图所示,下列说法不正确的
| A.滴定终点X可选用甲基橙作为指示剂 |
B.25℃, 的电离常数 的电离常数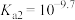 |
C.当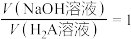 时, 时,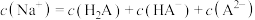 |
D.从W至Z点, 增大,且 增大,且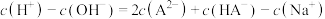 |
您最近一年使用:0次
名校
6 . 电位滴定法是根据滴定过程中被测离子浓度发生突跃,指示电极电位也产生突跃,从而确定滴定终点的一种滴定分析方法。常温下,利用盐酸滴定一定物质的量浓度的碳酸钠溶液,其电位滴定曲线与pH曲线如图所示(已知:碳酸的电离常数 )。下列说法不正确的是
)。下列说法不正确的是
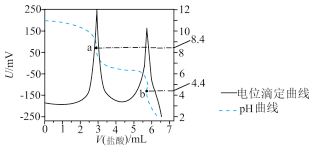
 )。下列说法不正确的是
)。下列说法不正确的是
| A.该实验中,需先后用酚酞和甲基橙作指示剂 |
B.a点: |
| C.水的电离程度:a点>b点 |
D.b点: 比值为 比值为 |
您最近一年使用:0次
名校
7 . Ⅰ. 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
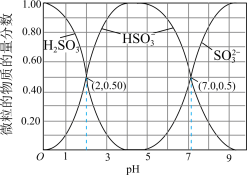
请回答以下问题:
(1)下列说法正确的是_______。
(2)若向 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得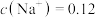 mol∙L−1,则溶液中
mol∙L−1,则溶液中
_______ mol∙L−1;
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
Ⅱ.工业上可用纯碱吸收二氧化硫法制备 ,流程如下图所示。
,流程如下图所示。
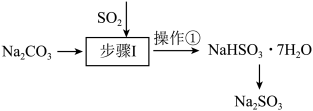
(4)步骤I中边搅拌边向 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是_______ ,操作①的名称为_______ ;
(5)某小组同学用0.1000 mol∙L−1的酸性 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:
①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性 溶液滴定;
溶液滴定;
③消耗 溶液体积为20.00 mL;
溶液体积为20.00 mL;
试计算样品中 的纯度
的纯度_______ 。
(6)连二亚硫酸钠( )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为_______ 。

 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
请回答以下问题:
(1)下列说法正确的是_______。
A. 溶液显碱性 溶液显碱性 |
B. 时,溶液中 时,溶液中 |
C. 溶液中 溶液中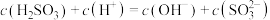 |
D. 溶液中 溶液中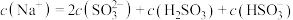 |
 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得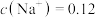 mol∙L−1,则溶液中
mol∙L−1,则溶液中
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
| 碳酸 | 次氯酸 | 醋酸 |
 |  | 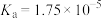 |
 |
A.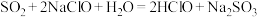 |
B.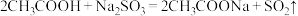 |
C. |
D. |
Ⅱ.工业上可用纯碱吸收二氧化硫法制备
 ,流程如下图所示。
,流程如下图所示。
(4)步骤I中边搅拌边向
 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是(5)某小组同学用0.1000 mol∙L−1的酸性
 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性
 溶液滴定;
溶液滴定;③消耗
 溶液体积为20.00 mL;
溶液体积为20.00 mL;试计算样品中
 的纯度
的纯度(6)连二亚硫酸钠(
 )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
您最近一年使用:0次
名校
解题方法
8 . 常温下,将一定浓度的HA和HB两种酸溶液分别与0.1mol•L﹣1NaOH溶液等体积混合,实验记录如表:
下列说法正确的是
| 混合液 | pH | 加入的酸 | 酸的浓度/(mol•L﹣1) |
| ① | 8.6 | HA | 0.10 |
| ② | 2.0 | HB | 0.12 |
| A.HA为强酸,HB为弱酸 |
| B.溶液①中存在:c(A﹣)>c(Na+)>c(OH﹣)>c(H+) |
| C.升高温度,溶液①中c(A﹣)﹣c(HA)的值会增大 |
| D.溶液②中存在:c(Na+)+c(H+)=c(OH﹣)+(B﹣) |
您最近一年使用:0次
2023-03-22更新
|
244次组卷
|
2卷引用:重庆市第一中学校2020-2021学年高二下学期期末考试化学试题
真题
名校
9 . 某小组模拟成垢-除垢过程如图。
100mL0.1mol•L-1CaCl2水溶液 ……
……
忽略体积变化,且步骤②中反应完全。下列说法正确的是
100mL0.1mol•L-1CaCl2水溶液
 ……
……忽略体积变化,且步骤②中反应完全。下列说法正确的是
| A.经过步骤①,溶液中c(Ca2+)+c(Na+)=c(Cl-) |
B.经过步骤②,溶液中c(Na+)=4c(SO ) ) |
C.经过步骤②,溶液中c(Cl-)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.经过步骤③,溶液中c(CH3COOH)+c(CH3COO-)=c(Cl-) |
您最近一年使用:0次
2023-02-22更新
|
4510次组卷
|
9卷引用:2022年重庆高考真题化学试题
2022年重庆高考真题化学试题(已下线)2022年重庆高考真题化学试题变式题(选择题11-14)(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)第14练 水溶液中粒子浓度的关系判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)广西壮族自治区南宁市第二中学2022-2023学年高二下学期期末化学考试试卷
解题方法
10 . 室温下,对于 的
的 溶液,下列判断中正确的是
溶液,下列判断中正确的是
 的
的 溶液,下列判断中正确的是
溶液,下列判断中正确的是A.稀释后,溶液中 增大 增大 | B.溶液中 |
C.溶液中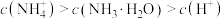 | D.若溶液的 ,则 ,则 的水解百分率为10% 的水解百分率为10% |
您最近一年使用:0次



