名校
解题方法
1 . 常温下,下列有关溶液的说法一定正确的是
A.NaHCO3溶液加水稀释,c(Na+)与c(HCO )的比值将减小 )的比值将减小 |
| B.pH=1的一元酸和pH=13的一元碱等体积混合后:c(OH-)=c(H+) |
C.0.1 mol·L-1硫酸铵溶液中:c(NH ) > c(SO ) > c(SO ) >c(H+)>c(OH-) ) >c(H+)>c(OH-) |
| D.0.1 mol·L-1硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
您最近一年使用:0次
名校
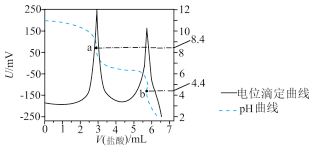
2 . 电位滴定法是根据滴定过程中被测离子浓度发生突跃,指示电极电位也产生突跃,从而确定滴定终点的一种滴定分析方法。常温下,利用盐酸滴定一定物质的量浓度的碳酸钠溶液,其电位滴定曲线与pH曲线如图所示(已知:碳酸的电离常数 )。下列说法不正确的是
)。下列说法不正确的是
 )。下列说法不正确的是
)。下列说法不正确的是
| A.该实验中,需先后用酚酞和甲基橙作指示剂 |
B.a点: |
| C.水的电离程度:a点>b点 |
D.b点: 比值为 比值为 |
您最近一年使用:0次
名校
3 . Ⅰ. 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
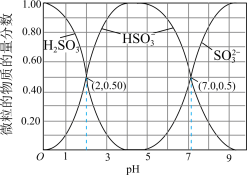
请回答以下问题:
(1)下列说法正确的是_______。
(2)若向 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得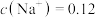 mol∙L−1,则溶液中
mol∙L−1,则溶液中
_______ mol∙L−1;
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
Ⅱ.工业上可用纯碱吸收二氧化硫法制备 ,流程如下图所示。
,流程如下图所示。
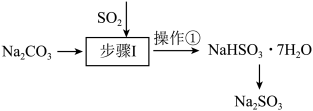
(4)步骤I中边搅拌边向 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是_______ ,操作①的名称为_______ ;
(5)某小组同学用0.1000 mol∙L−1的酸性 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:
①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性 溶液滴定;
溶液滴定;
③消耗 溶液体积为20.00 mL;
溶液体积为20.00 mL;
试计算样品中 的纯度
的纯度_______ 。
(6)连二亚硫酸钠( )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为_______ 。

 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
请回答以下问题:
(1)下列说法正确的是_______。
A. 溶液显碱性 溶液显碱性 |
B. 时,溶液中 时,溶液中 |
C. 溶液中 溶液中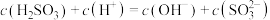 |
D. 溶液中 溶液中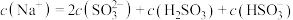 |
 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得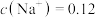 mol∙L−1,则溶液中
mol∙L−1,则溶液中
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
| 碳酸 | 次氯酸 | 醋酸 |
 |  | 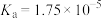 |
 |
A.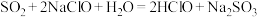 |
B.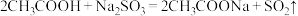 |
C. |
D. |
Ⅱ.工业上可用纯碱吸收二氧化硫法制备
 ,流程如下图所示。
,流程如下图所示。
(4)步骤I中边搅拌边向
 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是(5)某小组同学用0.1000 mol∙L−1的酸性
 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性
 溶液滴定;
溶液滴定;③消耗
 溶液体积为20.00 mL;
溶液体积为20.00 mL;试计算样品中
 的纯度
的纯度(6)连二亚硫酸钠(
 )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
您最近一年使用:0次
2023·河北·模拟预测
名校
4 . 25℃时,用 盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及
盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及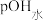 [
[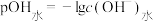 ,
, 为水电离出的
为水电离出的 的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
 盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及
盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及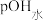 [
[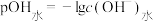 ,
, 为水电离出的
为水电离出的 的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是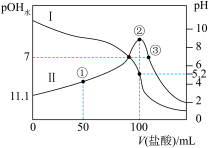
A.25℃时,MOH的电离常数数量级为 |
B.点①溶液中: |
C.点②溶液呈酸性,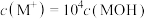 |
D.点③溶液呈中性, |
您最近一年使用:0次
2023-04-21更新
|
339次组卷
|
6卷引用:重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题
重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题(已下线)2023年普通高中学业水平选择性考试化学押题卷(五)湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题(已下线)选择题21-23河南省驻马店高级中学2023-2024学年高三上学期12月阶段检测化学试题 湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷
2022高三·全国·专题练习
真题
名校
5 . 某小组模拟成垢-除垢过程如图。
100mL0.1mol•L-1CaCl2水溶液 ……
……
忽略体积变化,且步骤②中反应完全。下列说法正确的是
100mL0.1mol•L-1CaCl2水溶液
 ……
……忽略体积变化,且步骤②中反应完全。下列说法正确的是
| A.经过步骤①,溶液中c(Ca2+)+c(Na+)=c(Cl-) |
B.经过步骤②,溶液中c(Na+)=4c(SO ) ) |
C.经过步骤②,溶液中c(Cl-)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.经过步骤③,溶液中c(CH3COOH)+c(CH3COO-)=c(Cl-) |
您最近一年使用:0次
2023-02-22更新
|
4721次组卷
|
9卷引用:2022年重庆高考真题化学试题
2022年重庆高考真题化学试题(已下线)2022年重庆高考真题化学试题变式题(选择题11-14)(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)第14练 水溶液中粒子浓度的关系判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)广西壮族自治区南宁市第二中学2022-2023学年高二下学期期末化学考试试卷
解题方法
6 . 室温下,对于 的
的 溶液,下列判断中正确的是
溶液,下列判断中正确的是
 的
的 溶液,下列判断中正确的是
溶液,下列判断中正确的是A.稀释后,溶液中 增大 增大 | B.溶液中 |
C.溶液中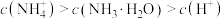 | D.若溶液的 ,则 ,则 的水解百分率为10% 的水解百分率为10% |
您最近一年使用:0次
名校
解题方法
7 . 25℃时,向20mL0.1mol/LH2R(二元弱酸)溶液中滴加0.1mol/LNaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示。下列说法正确的是


A.a点对应的溶液中: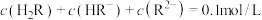 |
B.b点对应的溶液中: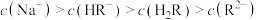 |
| C.a、b、c、d四点中,d点对应的溶液中水的电离程度最大 |
D.a、b、c、d各点溶液中均有: |
您最近一年使用:0次
2022-08-24更新
|
388次组卷
|
5卷引用:重庆市铜梁一中等三校2022-2023学年高二上学期期末考试化学试题
重庆市铜梁一中等三校2022-2023学年高二上学期期末考试化学试题黑龙江省哈尔滨市2022-2023学年高三上学期学业质量监测化学试题四川省泸县第四中学2022-2023学年高二上学期期末考试化学试题(已下线)河南省湘豫名校2023届高三下学期第一次模拟化学试题变式题(选择题11-13)湖南省 邵阳市第二中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
8 . 已知NA代表阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,22. 4L正戊烷、异戊烷、新戊烷混合物含有共价键数为16 NA |
| B.1mol Na2O2与CaC2固体混合物中含阴离子数目大于NA |
| C.1mol 碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数为2 NA |
D.1L1mol· L-1氯化铵水溶液中 与H+离子数之和大于NA 与H+离子数之和大于NA |
您最近一年使用:0次
名校
解题方法
9 . 缓冲溶液可以抗御少量酸碱对溶液 的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系
的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系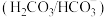 ,维持血液的
,维持血液的 保持稳定。已知在人体正常体温时,反应
保持稳定。已知在人体正常体温时,反应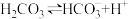 的
的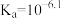 ,正常人的血液中
,正常人的血液中 。则下列判断正确的是
。则下列判断正确的是
 的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系
的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系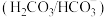 ,维持血液的
,维持血液的 保持稳定。已知在人体正常体温时,反应
保持稳定。已知在人体正常体温时,反应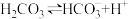 的
的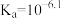 ,正常人的血液中
,正常人的血液中 。则下列判断正确的是
。则下列判断正确的是A.正常人血液内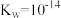 |
B.由题给数据可算得正常人血液的 约为7.4 约为7.4 |
C.正常人血液中存在: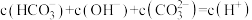 |
D.当过量的碱进入血液中时,只有发生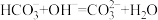 的反应 的反应 |
您最近一年使用:0次
名校
10 .  相同的以下溶液:①
相同的以下溶液:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ 溶液中,溶质物质的量浓度大小比较,正确的顺序是
溶液中,溶质物质的量浓度大小比较,正确的顺序是
 相同的以下溶液:①
相同的以下溶液:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ 溶液中,溶质物质的量浓度大小比较,正确的顺序是
溶液中,溶质物质的量浓度大小比较,正确的顺序是| A.⑤>④>①>②>③ | B.②>③>①>④>⑤ |
| C.④>⑤>②>③>① | D.③>②>①>④>⑤ |
您最近一年使用:0次



