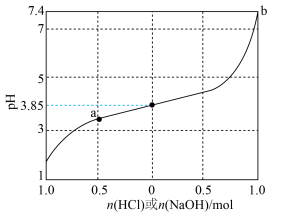
1 . 缓冲溶液是指加少量水稀释或外加少量酸、碱,自身pH不发生显著变化的溶液。1L含1mol乳酸(HLac)和1mol乳酸钠(NaLac)的溶液就是一种缓冲溶液,该溶液的pH为3.85。下图是此缓冲溶液的pH随通入HCl(g)或加入NaOH(s)的物质的量变化的示意图(溶液体积保持1L),已知lg3=0.48。下列说法错误的是
A.此缓冲溶液中(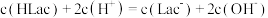 |
| B.通过计算可得出,a点溶液的pH约为3.37 |
| C.根据图像可以判断,b点溶液已失去缓冲能力 |
D.当加入NaOH,且横坐标为0.5时,对应溶液中(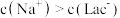 |
您最近半年使用:0次
名校
2 . 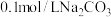 溶液的
溶液的 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是

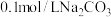 溶液的
溶液的 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是
A.温度高于 时, 时, 变化主要受水的电离平衡移动的影响 变化主要受水的电离平衡移动的影响 |
B.常温下: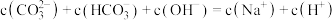 |
C.常温下: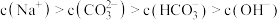 |
| D.升高温度,溶液中的水解平衡逆向移动,导致溶液pH减小 |
您最近半年使用:0次
名校
3 . 氢氧化钠、碳酸钠和碳酸氢钠等都是常见的化合物,应用广泛,如 与
与 两种溶液可用作泡沫灭火剂。下列相关说法错误的是
两种溶液可用作泡沫灭火剂。下列相关说法错误的是
 与
与 两种溶液可用作泡沫灭火剂。下列相关说法错误的是
两种溶液可用作泡沫灭火剂。下列相关说法错误的是| A.碳酸氢钠溶液呈碱性 |
B.0.1 碳酸钠溶液中: 碳酸钠溶液中: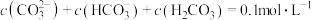 |
C. 的 的 溶液中由水电离出的 溶液中由水电离出的 大于等 大于等 的氨水中由水电离出的 的氨水中由水电离出的 |
D.泡沫灭火器的工作原理: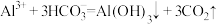 |
您最近半年使用:0次
2024-02-01更新
|
144次组卷
|
3卷引用:河南省郑州市宇华实验学校2023-2024学年高三下学期开学化学试题
河南省郑州市宇华实验学校2023-2024学年高三下学期开学化学试题安徽省亳州市2023-2024学年高三上学期期末考试化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
4 . 已知 是阿伏伽德罗常数的值,下列有关说法正确的是
是阿伏伽德罗常数的值,下列有关说法正确的是
 是阿伏伽德罗常数的值,下列有关说法正确的是
是阿伏伽德罗常数的值,下列有关说法正确的是A.常温常压下,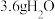 和 和 混合物中所含的质子数目为 混合物中所含的质子数目为 |
B. 时, 时, 的 的 溶液中含有 溶液中含有 的数目为 的数目为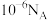 |
C.向 醋酸钡溶液中加入醋酸至中性,混合液中 醋酸钡溶液中加入醋酸至中性,混合液中 数目为 数目为 |
D. 的物质类别属于正盐,则 的物质类别属于正盐,则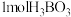 与过量氢氧化钠溶液反应,消耗 与过量氢氧化钠溶液反应,消耗 的数目为 的数目为 |
您最近半年使用:0次
5 . 常温下,在一定浓度的草酸溶液中滴加一定浓度的NaOH溶液,混合溶液中 和
和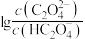 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
 和
和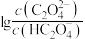 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
A.直线甲代表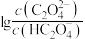 与溶液pH的关系 与溶液pH的关系 |
B.草酸的电离常数之比: |
C.d点溶液中: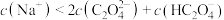 |
| D.若滴加NaOH的物质的量等于开始时草酸的物质的量,所得溶液显碱性 |
您最近半年使用:0次
名校
6 . 设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.向1L0.1mol·L-1CH3COOH溶液中通入氨气至中性,铵根离子的数目为0.1NA |
| B.N2和H2反应生成1molNH3转移电子数目为3NA |
| C.2L1mol·L-1CuSO4溶液中,Cu2+的数目为2NA |
| D.相同物质的量的C2H5OH与CH3OCH3所含的共价键数目不同 |
您最近半年使用:0次
2024-01-07更新
|
130次组卷
|
2卷引用:河南省顶级名校2023-2024学年高三上学期12月教学质量测评理科综合试题
名校
解题方法
7 . 重铬酸钾是强氧化剂,在实验室和工业中都有很广泛的应用。用于制铬矾、火柴、铬颜料、电镀、有机合成等。
(1)K2Cr2O7溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i) (aq)+H2O(l)⇌2HCrO
(aq)+H2O(l)⇌2HCrO (aq) K1=3.0×10-2(25℃)
(aq) K1=3.0×10-2(25℃)
(ii)HCrO (aq)⇌
(aq)⇌ (aq)+H+(aq) K2=3.3×10-7(25℃)
(aq)+H+(aq) K2=3.3×10-7(25℃)
①下列有关K2Cr2O7溶液的说法正确的有___________ 。
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(i)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时c2(HCrO )与c(
)与c( )的比值保持不变
)的比值保持不变
②25℃时,0.10mol•L-1K2Cr2O7溶液中 、HCrO
、HCrO 与
与 的平衡浓度分别为x、y、zmol•L-1,则x、y、z之间的关系式为
的平衡浓度分别为x、y、zmol•L-1,则x、y、z之间的关系式为___________ =0.10。
(2)现有含少量杂质的FeCl2⋅nH2O,为测定n值进行如下实验:
称取m1g样品,用足量稀硫酸溶解后,用cmol/LK2Cr2O7标准溶液滴定Fe2+达终点时消耗VmL(滴定过程中 转化为Cr3+,Cl-不反应)。
转化为Cr3+,Cl-不反应)。
①滴定时应将K2Cr2O7溶液加入___________ (填“酸式”或“碱式”)滴定管中,在规格为50.00mL的滴定管中,若起始读数为10.00mL,此时滴定管中溶液的实际体积为___________ (填标号)。
A.10.00mL B.40mL C.大于40mL D.小于40mL
②滴定过程中操作滴定管的图示正确的是___________ 。
A. B.
B.  C.
C.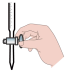
③下列关于滴定分析的操作,不正确的是___________ 。
A.滴定前应将滴定管烘干后再装溶液
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
④下列情况会导致n测量值偏小的是___________ (填标号)。
①样品中含少量FeO杂质;
②实验中,称重后样品发生了潮解;
③滴定达终点时发现滴定管尖嘴内有气泡生成;
④滴定时,滴定管洗涤后直接装标准液;
⑤滴定前平视读数,滴定后俯视读数。
(1)K2Cr2O7溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)
 (aq)+H2O(l)⇌2HCrO
(aq)+H2O(l)⇌2HCrO (aq) K1=3.0×10-2(25℃)
(aq) K1=3.0×10-2(25℃)(ii)HCrO
 (aq)⇌
(aq)⇌ (aq)+H+(aq) K2=3.3×10-7(25℃)
(aq)+H+(aq) K2=3.3×10-7(25℃)①下列有关K2Cr2O7溶液的说法正确的有
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(i)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时c2(HCrO
 )与c(
)与c( )的比值保持不变
)的比值保持不变②25℃时,0.10mol•L-1K2Cr2O7溶液中
 、HCrO
、HCrO 与
与 的平衡浓度分别为x、y、zmol•L-1,则x、y、z之间的关系式为
的平衡浓度分别为x、y、zmol•L-1,则x、y、z之间的关系式为(2)现有含少量杂质的FeCl2⋅nH2O,为测定n值进行如下实验:
称取m1g样品,用足量稀硫酸溶解后,用cmol/LK2Cr2O7标准溶液滴定Fe2+达终点时消耗VmL(滴定过程中
 转化为Cr3+,Cl-不反应)。
转化为Cr3+,Cl-不反应)。①滴定时应将K2Cr2O7溶液加入
A.10.00mL B.40mL C.大于40mL D.小于40mL
②滴定过程中操作滴定管的图示正确的是
A.
 B.
B.  C.
C.
③下列关于滴定分析的操作,不正确的是
A.滴定前应将滴定管烘干后再装溶液
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
④下列情况会导致n测量值偏小的是
①样品中含少量FeO杂质;
②实验中,称重后样品发生了潮解;
③滴定达终点时发现滴定管尖嘴内有气泡生成;
④滴定时,滴定管洗涤后直接装标准液;
⑤滴定前平视读数,滴定后俯视读数。
您最近半年使用:0次
解题方法
8 . 实验研究发现:25℃时,向0.1mol·L—1NaHCO3溶液(pH=8.2)中加入过量0.1mol·L—1CaCl2溶液,有白色沉淀产生,静置获得上层清液。下列说法正确的是
A.上层清液中 |
B.产生白色沉淀的过程中 的电离度不断增大 的电离度不断增大 |
C.产生白色沉淀的离子方程式为 |
D.0.1mol·L-1NaHCO3溶液中: |
您最近半年使用:0次
名校
解题方法
9 . 如果Fe3+、 、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
 、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是| A.Na+ | B. | C. | D.Cl- |
您最近半年使用:0次
名校
10 . 25℃时,用 盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及
盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及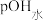 [
[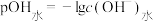 ,
, 为水电离出的
为水电离出的 的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
 盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及
盐酸滴定100mL等浓度的MOH溶液,混合溶液的pH及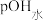 [
[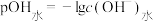 ,
, 为水电离出的
为水电离出的 的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是
的浓度]与滴入盐酸体积的关系如图所示。下列说法正确的是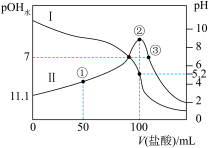
A.25℃时,MOH的电离常数数量级为 |
B.点①溶液中: |
C.点②溶液呈酸性,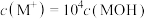 |
D.点③溶液呈中性, |
您最近半年使用:0次
2023-04-21更新
|
311次组卷
|
5卷引用:河南省驻马店高级中学2023-2024学年高三上学期12月阶段检测化学试题
河南省驻马店高级中学2023-2024学年高三上学期12月阶段检测化学试题 (已下线)2023年普通高中学业水平选择性考试化学押题卷(五)湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题(已下线)选择题21-23湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷



