解题方法
1 . 下列叙述正确的是
| A.向蒸馏水中加入浓硫酸,KW不变 |
B.向稀氨水中加少量 NH4Cl固体,  将减小 将减小 |
C.向 CH₃COONa溶液中通入HCl气体至溶液呈中性,  |
D.0.2mol/L H2S 溶液与0.2mol/L NaOH 溶液等体积混合,忽略溶液混合的体积变化:  |
您最近一年使用:0次
名校
解题方法
2 . 室温下,0.1mol∙L-1 NaHCO3溶液的pH约为8,通过下列实验探究NaHCO3、Na2CO3溶液的性质。
实验1:向0.1mol∙L-1 NaHCO3溶液中滴加等体积0.1 mol∙L-1 CaCl2溶液,产生白色沉淀。
实验2:向0.1mol∙L-1 Na2CO3溶液中通入CO2,溶液pH从12下降到约为9。
实验3:向0.1mol∙L-1 Na2CO3溶液中滴加新制饱和氯水,氯水颜色褪去。
下列说法不正确的是
实验1:向0.1mol∙L-1 NaHCO3溶液中滴加等体积0.1 mol∙L-1 CaCl2溶液,产生白色沉淀。
实验2:向0.1mol∙L-1 Na2CO3溶液中通入CO2,溶液pH从12下降到约为9。
实验3:向0.1mol∙L-1 Na2CO3溶液中滴加新制饱和氯水,氯水颜色褪去。
下列说法不正确的是
A.室温下,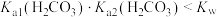 |
| B.由实验1事实可知,水的电离程度不断增大 |
C.实验2进行过程中,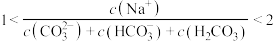 |
| D.实验3进行过程中,存在三个以上的平衡移动过程 |
您最近一年使用:0次
3 . 某研究小组利用电位滴定法研究盐酸滴定 溶液过程中的化学变化,得到电极电位U和溶液pH随滴加盐酸的体积变化曲线如图所示。[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸
溶液过程中的化学变化,得到电极电位U和溶液pH随滴加盐酸的体积变化曲线如图所示。[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸 是二元弱酸,其电离常数分别是
是二元弱酸,其电离常数分别是 ],下列说法正确的是
],下列说法正确的是
 溶液过程中的化学变化,得到电极电位U和溶液pH随滴加盐酸的体积变化曲线如图所示。[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸
溶液过程中的化学变化,得到电极电位U和溶液pH随滴加盐酸的体积变化曲线如图所示。[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,进而确定滴定终点。②亚磷酸 是二元弱酸,其电离常数分别是
是二元弱酸,其电离常数分别是 ],下列说法正确的是
],下列说法正确的是
| A.开始滴定时溶液呈酸性 |
| B.实验中,需加入甲基橙作指示剂 |
C.c点溶液中: |
D.a点溶液中: |
您最近一年使用:0次
4 . 室温下,某 溶液体系中满足
溶液体系中满足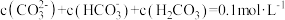 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合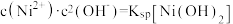 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合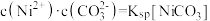 ,不同pH下
,不同pH下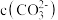 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
 溶液体系中满足
溶液体系中满足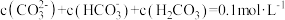 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合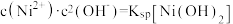 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合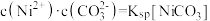 ,不同pH下
,不同pH下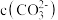 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
A.由图1, 的水解平衡常数的数量级是 的水解平衡常数的数量级是 |
B.图2中M点,溶液中存在 |
C.图2中P点,存在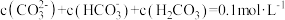 |
D.沉淀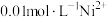 制备 制备 时,选用 时,选用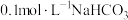 溶液比 溶液比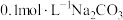 溶液效果好 溶液效果好 |
您最近一年使用:0次
2024-05-16更新
|
372次组卷
|
3卷引用:2024届重庆市涪陵第五中学校高三下学期模拟预测化学试题
名校
解题方法
5 . 常温下,向新制氯水中滴加NaOH溶液,溶液中水电离出的OH-浓度与NaOH溶液体积之间的关系如下图所示。下列推断不正确的是
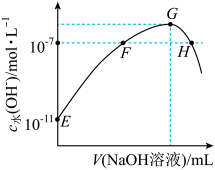
| A.E点溶液pH=3,H点溶液pH>7 |
| B.Kw:H点>F点>E点 |
C.F点溶液中: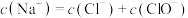 |
D.G点溶液中: |
您最近一年使用:0次
名校
解题方法
6 . 室温下,通过下列实验探究0.0100mol/L Na2C2O4溶液的性质。
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
A.该Na2C2O4溶液中满足: >2 >2 |
B.实验2滴加盐酸过程中可能存在;c(Na+ )= c( )+2c( )+2c( )+c(Cl-) )+c(Cl-) |
C.实验3所得上层清液中:c( )=5×10-7mol⋅L-1 )=5×10-7mol⋅L-1 |
D.实验3所得上层清液中:2c(Ca2+)+c(H+ )=c( )+2c( )+2c( )+0.02+c(OH-) )+0.02+c(OH-) |
您最近一年使用:0次
7 . 常温下,用0.2mol/L盐酸滴定25.00mL0.2mol/L某弱碱ROH溶液,所得溶液pH、R+和ROH的物质的量分数与滴加盐酸体积的关系如图所示。下列叙述正确的是
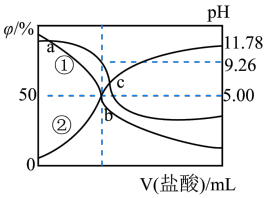

| A.曲线②代表ROH |
| B.若c点加入HCl溶液体积为25mL,则溶液中存在c(H+)>c(OH-)+c(ROH) |
| C.RCl的水解平衡常数为1.0×10-5 |
| D.a、b、c三点的溶液,水的电离程度:a<b<c |
您最近一年使用:0次
解题方法
8 . 常温下,分别向相同浓度的NaHCO3、Na2CO3溶液中逐滴加入盐酸,滴加过程中溶液的pH变化如下图所示。下列说法正确的是
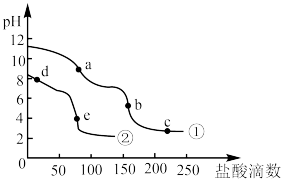
| A.曲线①表示盐酸滴入NaHCO3溶液的过程 |
| B.d、e点水的电离程度:d>e |
| C.a点的KW大于d点的KW |
D.b、c、e点均满足: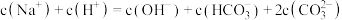 |
您最近一年使用:0次
2024-04-16更新
|
128次组卷
|
2卷引用:重庆市康德2024年普通高中学业水平选择性考试高三下学期高考模拟调研卷(三)化学试题
名校
9 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,11.2L苯中含有 个 个 键 键 |
B.0.1mol 晶体中所含离子数目为 晶体中所含离子数目为 |
C. 的NaOH溶液中, 的NaOH溶液中, 的数目为 的数目为 |
D.将1mol 通入足量水中,HClO、 通入足量水中,HClO、 、 、 微粒数之和为 微粒数之和为 |
您最近一年使用:0次
名校
解题方法
10 . 室温下,向10.0mL 溶液中逐滴加入0.100
溶液中逐滴加入0.100 盐酸,滴定曲线如图所示,其中b、c为滴定终点。下列说法正确的是
盐酸,滴定曲线如图所示,其中b、c为滴定终点。下列说法正确的是

 溶液中逐滴加入0.100
溶液中逐滴加入0.100 盐酸,滴定曲线如图所示,其中b、c为滴定终点。下列说法正确的是
盐酸,滴定曲线如图所示,其中b、c为滴定终点。下列说法正确的是
| A.溶液中水的电离程度:c点>b点>a点 |
| B.在逐滴加入盐酸的过程中所有离子浓度都减小 |
C.a、b、c三点均存在: |
D.a点溶液中: |
您最近一年使用:0次



