1 . 次氯酸为一元弱酸,具有漂白和杀菌作用。常温下其电离平衡体系中各成分的组成分数 [
[ ,X为
,X为 或
或 ]与
]与 的关系如图所示下列说法正确的是
的关系如图所示下列说法正确的是

 [
[ ,X为
,X为 或
或 ]与
]与 的关系如图所示下列说法正确的是
的关系如图所示下列说法正确的是
A.对新制氯水加热,可使 增大,漂白和杀菌作用更好 增大,漂白和杀菌作用更好 |
B.向 溶液中滴加稀 溶液中滴加稀 溶液至恰好中和的过程中,水的电离程度先增大后减小 溶液至恰好中和的过程中,水的电离程度先增大后减小 |
C.常温下 的电离常数: 的电离常数: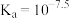 |
D.在含 和 和 的溶液中,随着 的溶液中,随着 的变化,则有: 的变化,则有: |
您最近一年使用:0次
名校
2 . 2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
| A.醋酸钠是强电解质 |
B.醋酸钠与 都是离子化合物 都是离子化合物 |
C.常温下,醋酸钠溶液的 |
D.醋酸钠溶液中 |
您最近一年使用:0次
名校
3 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.100mL 1mol/L NH4Cl溶液中含有阳离子的数目大于0.1NA |
| B.0.1mol的11B中,含有0.6NA个电子 |
| C.25℃时,pH=13的Ba(OH)2溶液中含有氢氧根离子数为0.1NA |
| D.标准状况下,5.6L CO2中含有的共用电子对数为0.5 NA |
您最近一年使用:0次
名校
解题方法
4 . 如图所示,某兴趣小组用油性笔在一小块覆铜板上写上“化学”,然后浸入盛有 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中 与
与 之比为2:3。下列说法不正确的是
之比为2:3。下列说法不正确的是

 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干。对反应后的溶液进行分析,溶液中 与
与 之比为2:3。下列说法不正确的是
之比为2:3。下列说法不正确的是
A.反应后的溶液中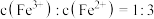 |
B.反应的离子方程式为 |
C.反应后的溶液中 |
D.使反应后的溶液再生为 溶液,可通过加入足量铁粉,过滤,向滤液中通入 溶液,可通过加入足量铁粉,过滤,向滤液中通入 来实现 来实现 |
您最近一年使用:0次
名校
解题方法
5 . 请根据要求填写:
Ⅰ.电化学:如图为燃料电池简单示意图,其中两电极均为石墨电极。若a处通入CH4,b处通入O2;
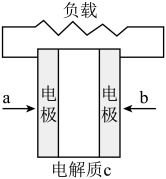
(1)若电解质溶液为KOH溶液,则负极电极反应式为:___________
(2)若电解质为熔融K2CO3,则负极电极反应式为:___________
(3)若电解质为熔融氧化物(Y2O3),则负极电极反应式为:___________
(4)请写出用惰性电极电解CuSO4溶液的电极反应方程式阴极:___________ ;阳极:___________ ;总反应方程式:___________
Ⅱ.回答下列问题
(5)常温下,pH=3的NH4Cl溶液中,由水电离出的氢离子浓度___________ ,溶液中氢氧根离子浓度为___________
(6)将一定浓度和体积的氨水与氯化铵溶液混合后pH=7,则离子浓度大小关系为___________
(7)某溶液中n(Na2CO3):n(NaHCO3)=1:2,写出该溶液中含钠微粒与含碳微粒之间的物料守恒式___________
(8)等NH 浓度的下列溶液中,溶质浓度的大小关系为:
浓度的下列溶液中,溶质浓度的大小关系为:___________
①NH4Cl ②CH3COONH4 ③(NH4)2SO4 ④(NH4)2CO3
Ⅰ.电化学:如图为燃料电池简单示意图,其中两电极均为石墨电极。若a处通入CH4,b处通入O2;

(1)若电解质溶液为KOH溶液,则负极电极反应式为:
(2)若电解质为熔融K2CO3,则负极电极反应式为:
(3)若电解质为熔融氧化物(Y2O3),则负极电极反应式为:
(4)请写出用惰性电极电解CuSO4溶液的电极反应方程式阴极:
Ⅱ.回答下列问题
(5)常温下,pH=3的NH4Cl溶液中,由水电离出的氢离子浓度
(6)将一定浓度和体积的氨水与氯化铵溶液混合后pH=7,则离子浓度大小关系为
(7)某溶液中n(Na2CO3):n(NaHCO3)=1:2,写出该溶液中含钠微粒与含碳微粒之间的物料守恒式
(8)等NH
 浓度的下列溶液中,溶质浓度的大小关系为:
浓度的下列溶液中,溶质浓度的大小关系为:①NH4Cl ②CH3COONH4 ③(NH4)2SO4 ④(NH4)2CO3
您最近一年使用:0次
名校
解题方法
6 . CO2溶于水生成碳酸。已知下列数据:
现有常温下1mol/L的(NH4)2CO3溶液,下列说法正确的是
| 弱电解质 | H2CO3 | NH3·H2O |
| 电离平衡常数(25℃) | Ka1=4.5×10-7 Ka2=4.7×10-11 | Kb=1.8×10-5 |
| A.由数据可判断该溶液呈酸性 |
B.c( )>c( )>c( )>c( )>c( )>c(NH3·H2O) )>c(NH3·H2O) |
C.c( )+c(NH3·H2O)=2c( )+c(NH3·H2O)=2c( )+2c( )+2c( )+2c(H2CO3) )+2c(H2CO3) |
D.c( )+c(H+)=( )+c(H+)=( )+c(OH-)+c( )+c(OH-)+c( ) ) |
您最近一年使用:0次
名校
7 . 用 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是
 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是A.常温常压下,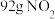 和 和 的混合气体含有的原子数为 的混合气体含有的原子数为 |
B.将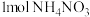 固体溶于一定浓度氨水中,溶液呈中性,溶液中 固体溶于一定浓度氨水中,溶液呈中性,溶液中 数目为 数目为 |
C.向 溶液中通入适量 溶液中通入适量 ,当有 ,当有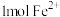 被氧化时,共转移电子的数目为 被氧化时,共转移电子的数目为 |
D. 中含有 中含有 键的数目为 键的数目为 |
您最近一年使用:0次
名校
解题方法
8 . 已知:25℃时,CH3COOH和NH3·H2O的电离平衡常数近似相等。
(1)关于0.1 mol/LCH3COOH溶液,回答下列问题。
①25℃时,测得0.1 mol/LCH3COOH溶液的pH= 3,则由水电离出的H+的浓度为______ mol/L。
②CH3COONa溶液显____ (填“酸性”“碱性”或“中性”),用离子方程式表示其原因:_____ 。
③能证明醋酸是弱酸的实验事实是_____ (填字母)。
a.同浓度的CH3COOH溶液和盐酸分别与相同的Mg条反应。放出H2的初始速率醋酸慢
b.常温下0.1 mol/LCH3COONa溶液的pH >7
c.CH3COOH溶液与Na2CO3反应生成CO2
d.0.1 mol/LCH3COOH溶液可使紫色石蕊溶液变红
e.常温下0.1mol/L醋酸溶液的pH > 1
(2)关于0.1 mol/L氨水,回答下列问题。
①NH3·H2O的电离方程式为,NH3·H2O的电离平衡常数表达式Kb=_______ 。
②25℃时,0.1 mol/L氨水的pH=___________ 。
③25℃时,向10 mL0.1 mol/L氨水中加入同体积同浓度的盐酸。下列说法正确的是________ 。
a.c(Cl-)>c( )>c(OH-)>c(H+) b.c(Cl-) = c(
)>c(OH-)>c(H+) b.c(Cl-) = c( ) + c(NH3·H2O)
) + c(NH3·H2O)
(1)关于0.1 mol/LCH3COOH溶液,回答下列问题。
①25℃时,测得0.1 mol/LCH3COOH溶液的pH= 3,则由水电离出的H+的浓度为
②CH3COONa溶液显
③能证明醋酸是弱酸的实验事实是
a.同浓度的CH3COOH溶液和盐酸分别与相同的Mg条反应。放出H2的初始速率醋酸慢
b.常温下0.1 mol/LCH3COONa溶液的pH >7
c.CH3COOH溶液与Na2CO3反应生成CO2
d.0.1 mol/LCH3COOH溶液可使紫色石蕊溶液变红
e.常温下0.1mol/L醋酸溶液的pH > 1
(2)关于0.1 mol/L氨水,回答下列问题。
①NH3·H2O的电离方程式为,NH3·H2O的电离平衡常数表达式Kb=
②25℃时,0.1 mol/L氨水的pH=
③25℃时,向10 mL0.1 mol/L氨水中加入同体积同浓度的盐酸。下列说法正确的是
a.c(Cl-)>c(
 )>c(OH-)>c(H+) b.c(Cl-) = c(
)>c(OH-)>c(H+) b.c(Cl-) = c( ) + c(NH3·H2O)
) + c(NH3·H2O)
您最近一年使用:0次
名校
解题方法
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.含0.2mol 的浓硫酸与足量的锌反应,转移的电子数为 的浓硫酸与足量的锌反应,转移的电子数为 |
B.142g 和 和 的固体混合物中所含阴、阳离子的总数为 的固体混合物中所含阴、阳离子的总数为 |
C.含1.7g 的水溶液中氧原子数为 的水溶液中氧原子数为 |
D.1mol·L 的 的 溶液中, 溶液中, 、 、 、 、 三种微粒数目之和为 三种微粒数目之和为 |
您最近一年使用:0次
解题方法
10 . 对下列各溶液中,微粒的物质的量浓度关系表述正确的是
A. 的 的 溶液中: 溶液中: |
B. 的 的 溶液中: 溶液中: |
C. 的氨水中: 的氨水中: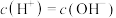 |
D.在 溶液中: 溶液中: |
您最近一年使用:0次



