解题方法
1 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近一年使用:0次
2 . 下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中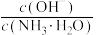 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近一年使用:0次
3 . 常温下,向0.1 的
的 溶液中加入一定量的NaOH溶液,当溶液中存在
溶液中加入一定量的NaOH溶液,当溶液中存在
 时,溶液中的主要溶质为
时,溶液中的主要溶质为
 的
的 溶液中加入一定量的NaOH溶液,当溶液中存在
溶液中加入一定量的NaOH溶液,当溶液中存在
 时,溶液中的主要溶质为
时,溶液中的主要溶质为A. | B.NaHS | C.NaHS和 | D. 和NaOH 和NaOH |
您最近一年使用:0次
4 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.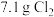 通入水中并充分反应,转移电子数目小于 通入水中并充分反应,转移电子数目小于 |
B.标准状况下, 中电子数目为 中电子数目为 |
C.向 溶液中通氨气至中性, 溶液中通氨气至中性, 目大于 目大于 |
D.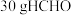 中含有 中含有 键数目为 键数目为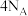 |
您最近一年使用:0次
5 . 已知 的
的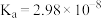 ,
, 的
的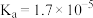 ,下列有关说法正确的是
,下列有关说法正确的是
 的
的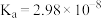 ,
, 的
的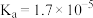 ,下列有关说法正确的是
,下列有关说法正确的是A.温度一定时在 的叠氮酸中加入少量 的叠氮酸中加入少量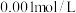 的稀盐酸,溶液的 的稀盐酸,溶液的 不会改变 不会改变 |
B.等浓度等体积的 和溶液 和溶液 前者所含离子总数比后者多 前者所含离子总数比后者多 |
C.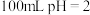 的新制氯水中: 的新制氯水中: |
D.将 通入 通入 溶液中,若溶液呈中性,则溶液中存在4种微粒 溶液中,若溶液呈中性,则溶液中存在4种微粒 |
您最近一年使用:0次
6 . 某化学兴趣小组同学在室温下用未知浓度的盐酸溶液滴定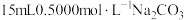 ,溶液,通过数字化仪器监测
,溶液,通过数字化仪器监测 变化,得到如下滴定曲线,
变化,得到如下滴定曲线,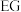 段有大量气泡产生,下列说法错误的是
段有大量气泡产生,下列说法错误的是
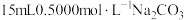 ,溶液,通过数字化仪器监测
,溶液,通过数字化仪器监测 变化,得到如下滴定曲线,
变化,得到如下滴定曲线,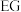 段有大量气泡产生,下列说法错误的是
段有大量气泡产生,下列说法错误的是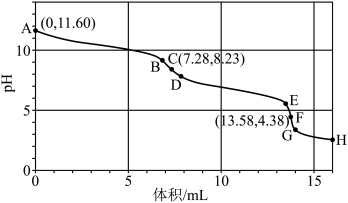
A.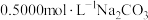 溶液中: 溶液中: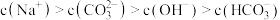 |
B.C点溶液中存在: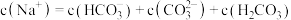 |
C.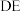 段发生的主要反应为: 段发生的主要反应为: |
D.确定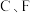 两个滴定终点。可分别用酚酞和和甲基橙做指示剂 两个滴定终点。可分别用酚酞和和甲基橙做指示剂 |
您最近一年使用:0次
7 . 缓冲溶液是指加少量水稀释或外加少量酸、碱,自身pH不发生显著变化的溶液。1L含1mol乳酸(HLac)和1mol乳酸钠(NaLac)的溶液就是一种缓冲溶液,该溶液的pH为3.85。下图是此缓冲溶液的pH随通入HCl(g)或加入NaOH(s)的物质的量变化的示意图(溶液体积保持1L),已知lg3=0.48。下列说法错误的是
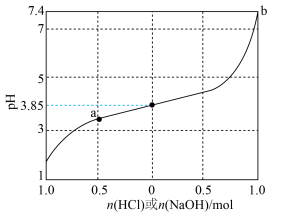
A.此缓冲溶液中(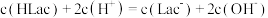 |
| B.通过计算可得出,a点溶液的pH约为3.37 |
| C.根据图像可以判断,b点溶液已失去缓冲能力 |
D.当加入NaOH,且横坐标为0.5时,对应溶液中(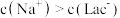 |
您最近一年使用:0次
2024-04-16更新
|
206次组卷
|
3卷引用:2024届河南省济洛平许四市高三下学期第三次质量检测(三模)理综试题-高中化学
名校
解题方法
8 . 滴定法是一种常见的定量实验分析方法,常见的有酸碱中和滴定法、氧化还原滴定法、沉淀滴定法等。常温下,用 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸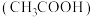 ,滴定曲线如图1所示。
,滴定曲线如图1所示。

1.在上述滴定过程中,不需要使用的玻璃仪器是 。
2.滴定过程中眼睛应注视_____ 。该实验使用的指示剂为_____ ,滴定终点的现象为_____ 。某次实验滴定终点时滴定管中液面位置如图2所示,则此时的读数为_____ mL。
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,_____ 点对应水的电离程度最大,c点溶液中,
_____  (填“>”“<”或“=”)
(填“>”“<”或“=”)
 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸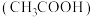 ,滴定曲线如图1所示。
,滴定曲线如图1所示。
1.在上述滴定过程中,不需要使用的玻璃仪器是 。
| A.移液管 | B.滴定管 | C.锥形瓶 | D.胶头滴管 |
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,

 (填“>”“<”或“=”)
(填“>”“<”或“=”)
您最近一年使用:0次
解题方法
9 . 回答下列问题:
(1)现有25℃时0.1mol•L-1的氨水,请回答以下问题:
①若向氨水中加入少量硫酸铵固体,此时溶液中
______ (填“增大”“减小”或“不变”)。
②若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH )=amol•L-1,则c(SO
)=amol•L-1,则c(SO )为
)为_______ 。
(2)泡沫灭火器原理(用离子方程式表示)______ 。
(3)已知NaHR溶液中c(H2R)<c(R2-),则该溶液中c(H+)_______ c(OH-)(填写“<”或“=”或“>”)。
(4)某温度(t℃)时,Kw=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,若所得混合溶液为中性,则a:b=_______ 。
(5)已知Cu(OH)2的Ksp=c(Cu2+)[c(OH-)]2=2×10-20。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某CuSO4溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH大于_______ 。
(6)在苏打溶液中存在的电荷守恒式为_______ ;质子守恒式为_______ 。
(1)现有25℃时0.1mol•L-1的氨水,请回答以下问题:
①若向氨水中加入少量硫酸铵固体,此时溶液中

②若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH
 )=amol•L-1,则c(SO
)=amol•L-1,则c(SO )为
)为(2)泡沫灭火器原理(用离子方程式表示)
(3)已知NaHR溶液中c(H2R)<c(R2-),则该溶液中c(H+)
(4)某温度(t℃)时,Kw=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,若所得混合溶液为中性,则a:b=
(5)已知Cu(OH)2的Ksp=c(Cu2+)[c(OH-)]2=2×10-20。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某CuSO4溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH大于
(6)在苏打溶液中存在的电荷守恒式为
您最近一年使用:0次
解题方法
10 . 设NA为阿伏加德罗常数的值,下列说法不正确的是
| A.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为10-13NA |
B.1L0.1mol/L的NaHCO3溶液中N( )+N( )+N( )+N(H2CO3)=0.1NA )+N(H2CO3)=0.1NA |
C.3H2(g)+N2(g) 2NH3(g) 2NH3(g)  =-akJ/mol,则每NA个H2(g)与足量的N2(g)反应生成NH3放出的热量等于 =-akJ/mol,则每NA个H2(g)与足量的N2(g)反应生成NH3放出的热量等于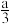 kJ kJ |
| D.4℃时,9mlH2O(l)含有的电子数约为5NA |
您最近一年使用:0次



