名校
解题方法
1 . 关于溶液中的微粒关系的讨论
Ⅰ.溶液中的离子浓度大小关系
(1)0.2mol/L NH3·H2O与0.1mol/L HCl等体积混合所得溶液(pH >7):离子浓度的比较:___ 。
(2)0.2mol/L CH3COONa与0.1mol/LHCl等体积混合液(pH <7):离子浓度的比较:______ 。
(3)等浓度的Na2CO3和NaHCO3混合溶液: 离子浓度的比较:_____________ 。
(4)NH4HSO4溶液与NaOH溶液混合后,溶液呈中性。离子浓度的比较:___ 。
(5)物质的量浓度相等的①(NH4)2SO4溶液、②NH4HSO4溶液、③(NH4)2CO3溶液、④NH4Cl溶液,c(NH )其由大到小的顺序为
)其由大到小的顺序为________ 。
Ⅱ.溶液中微粒的守恒关系
(6)KAl(SO4)2与MgCl2混合溶液中的电荷守恒_________ 。
(7)等浓度的CH3COOH和CH3COONa混合溶液,物料守恒式为______ 。
(8) (NH4)2CO3溶液中的质子守恒式为____________ 。
Ⅰ.溶液中的离子浓度大小关系
(1)0.2mol/L NH3·H2O与0.1mol/L HCl等体积混合所得溶液(pH >7):离子浓度的比较:
(2)0.2mol/L CH3COONa与0.1mol/LHCl等体积混合液(pH <7):离子浓度的比较:
(3)等浓度的Na2CO3和NaHCO3混合溶液: 离子浓度的比较:
(4)NH4HSO4溶液与NaOH溶液混合后,溶液呈中性。离子浓度的比较:
(5)物质的量浓度相等的①(NH4)2SO4溶液、②NH4HSO4溶液、③(NH4)2CO3溶液、④NH4Cl溶液,c(NH
 )其由大到小的顺序为
)其由大到小的顺序为Ⅱ.溶液中微粒的守恒关系
(6)KAl(SO4)2与MgCl2混合溶液中的电荷守恒
(7)等浓度的CH3COOH和CH3COONa混合溶液,物料守恒式为
(8) (NH4)2CO3溶液中的质子守恒式为
您最近一年使用:0次
解题方法
2 . 在室温下,下列五种溶液:
①
 溶液 ②
溶液 ② 硫酸 ③
硫酸 ③

④0.1 mo/L NaOH溶液 ⑤
 溶液
溶液
(1)加水稀释100倍后,①中的pH___________ 5,②中的pH___________ 5(填“>”、“<”或“=”)。
(2)若溶液③达到平衡时已电离的 为
为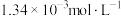 ,电离常数的值为
,电离常数的值为___________ 。
(3)溶液③中,
___________  。
。
(4)若取④0.1 mol/L NaOH溶液10mL与⑤
 溶液15 mL混合,假设混合后溶液体积为25 mL,测混合后溶液的
溶液15 mL混合,假设混合后溶液体积为25 mL,测混合后溶液的 ___________(填序号)。(已知
___________(填序号)。(已知 )
)
①

 溶液 ②
溶液 ② 硫酸 ③
硫酸 ③

④0.1 mo/L NaOH溶液 ⑤

 溶液
溶液(1)加水稀释100倍后,①中的pH
(2)若溶液③达到平衡时已电离的
 为
为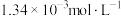 ,电离常数的值为
,电离常数的值为(3)溶液③中,

 。
。(4)若取④0.1 mol/L NaOH溶液10mL与⑤

 溶液15 mL混合,假设混合后溶液体积为25 mL,测混合后溶液的
溶液15 mL混合,假设混合后溶液体积为25 mL,测混合后溶液的 ___________(填序号)。(已知
___________(填序号)。(已知 )
)| A.12 | B.11.7 | C.2 | D.1.7 |
您最近一年使用:0次
名校
3 . 某温度下,体积和pH均相同的NaOH和CH3COONa溶液加水稀释时pH变化曲线如图所示,下列判断不正确的是


| A.曲线I为CH3COONa溶液稀释时的pH值变化曲线 |
| B.b、c两点溶液的导电能力相同 |
C.图象中a、b两点所处的溶液中 相同 相同 |
| D.a、b、c三点溶液水的电离程度a>b>c |
您最近一年使用:0次
2021-11-05更新
|
298次组卷
|
4卷引用:天津市武清区杨村第一中学2021-2022学年高二上学期第三次月考化学试题
4 . 鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用
)是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
表示)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 )是一种有机弱碱,可与盐酸反应生成盐酸盐(用
)是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
表示)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.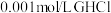 水溶液的 水溶液的 |
B.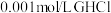 水溶液加水稀释, 水溶液加水稀释, 升高 升高 |
C. 在水中的电离方程式为: 在水中的电离方程式为: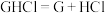 |
D. 水溶液中: 水溶液中: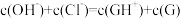 |
您最近一年使用:0次
2021-06-11更新
|
10375次组卷
|
44卷引用:天津市耀华中学2021-2022学年高三上学期第一次月考化学试题
天津市耀华中学2021-2022学年高三上学期第一次月考化学试题2021年新高考广东化学高考真题山东省淄博市2020-2021学年高二下学期期末考试化学试题(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第23讲 盐类水解(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)2021年广东省高考化学试卷变式题1-10题(已下线)第八单元 水溶液中的离子平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省吴兴高级中学2021-2022学年高二上学期12月月考化学试题天津市南开区2022届高三一模化学试题天津市耀华中学2023-2024学年高二上学期11月期中化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)上海市曹杨中学2021-2022 学年高三下学期期中考试化学试题福建省泉州市泉港一中、厦门外国语石狮分校2021-2022学年高二下学期期中联考化学试题(已下线)专题10 水溶液中的离子平衡-三年(2020-2022)高考真题分项汇编(已下线)第13练 以pH的计算突破弱电解质的电离、溶液酸碱性-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第32练 盐类的水解-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第23讲 盐类水解 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)浙江省杭州高级中学2022-2023学年高三上学期模拟考试化学试题广东省深圳市龙华区2021-2022学年高二上学期期末学业质量监测化学试题(已下线)专题20 溶液中粒子浓度大小的比较-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第49讲 盐类的水解甘肃省张掖市高台县第一中学2022-2023学年高二下学期2月月考化学试题重庆市长寿区2022-2023学年高二上学期期末质量检测化学试题(已下线)题型26 电离平衡常数、水解平衡常数及其应用图像(已下线)第14练 水溶液中粒子浓度的关系判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点2 水的电离与溶液的pH (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第4讲 盐类的水解广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(三)化学试题湖北省武汉市育才高级中学等2校2023-2024学年高二上学期化学模拟试卷2024届广东省高州市第一中学高三下学期5月考前热身训练化学试题
名校
解题方法
5 . 下列比较中,正确的是
| A.同温度同物质的量浓度时,HF比HCN易电离,则相同条件下NaF溶液的pH比NaCN溶液大 |
B.同浓度的下列溶液中,①(NH4)2SO4②NH4Cl③CH3COONH4.④NH3∙H2O;c( )由大到小的顺序是:①>②>③>④ )由大到小的顺序是:①>②>③>④ |
C.0.2mol∙L-1NH4Cl和0.1mol∙L-1NaOH溶液等体积混合后:c( )>c(Cl-)>c(Na+)>c(OH-)>c(H+) )>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| D.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
您最近一年使用:0次
2021-03-10更新
|
290次组卷
|
5卷引用:天津市咸水沽第二中学2021-2022学年高二上学期期中化学试题
天津市咸水沽第二中学2021-2022学年高二上学期期中化学试题湖南省邵阳市邵东创新实验学校2020-2021学年高二上学期期末考试化学(选考)试题湖南省常德市芷兰实验中学2020-2021学年高二下学期第一次月考化学试题(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版选修4)湖南省临湘市第五中学2021-2022学年高二上学期第三次月考化学试题
名校
6 . 把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,则混合液中微粒浓度关系正确的为
| A.c(CH3COO-)<c (Na+) |
| B.c(OH-)>c (H+) |
| C.c(CH3COOH)>c (CH3COO-) |
| D.c(CH3COOH)+c (CH3COO-)=0.01mol/L |
您最近一年使用:0次
2020-11-24更新
|
151次组卷
|
3卷引用:天津市静海区四校2021-2022学年高二上学期12月份阶段性检测化学试题
7 . 设NA为阿伏加 德罗常数值。关于常温下pH=2的H3PO4溶液,下列说法正确的是
| A.每升溶液中的H+数目为0.02NA |
B.c(H+)= c( )+2c( )+2c( )+3c( )+3c( )+ c(OH−) )+ c(OH−) |
| C.加水稀释使电离度增大,溶液pH减小 |
| D.加入NaH2PO4固体,溶液酸性增强 |
您最近一年使用:0次
2019-06-09更新
|
13824次组卷
|
68卷引用:天津市第三中学2021届高三下学期2月月考化学试题
天津市第三中学2021届高三下学期2月月考化学试题(已下线)专题02 化学用语及常用物理量——备战2021年高考化学纠错笔记(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)四川省雅安中学2020-2021学年高二下学期期中考试理综化学试题(已下线)课时13 阿伏加德罗常数运用-2022年高考化学一轮复习小题多维练(全国通用)选择性必修1(SJ)专题3专题培优专练(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题讲座(一) 阿伏加德罗常数的突破(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)广东省深圳市第七高级中学2022届高三第一次月考化学试卷(已下线)第21讲 电离平衡(讲)-2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向24 弱电解质的电离平衡-备战2022年高考化学一轮复习考点微专题吉林省长春市第二实验中学2021-2022学年高二上学期期中考试化学试题山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题(已下线)3.2.1 水的电离 溶液的酸碱性(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题2019年全国统一高考化学试题(新课标Ⅲ)(已下线)专题02 化学计量与化学计算——2019年高考真题和模拟题化学分项汇编(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编湖南省娄底市娄星区2019-2020学年高二上学期期中考试化学试题贵州省遵义市南白中学2019-2020学年高二上学期期中考试化学试题(已下线)专题8.1 弱电解质的电离平衡(练)-《2020年高考一轮复习讲练测》(已下线)专题8.1 弱电解质的电离平衡(讲)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练16 盐类的水解(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)专题三 化学常用计量与阿伏加德罗常数(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训2020届四川省成都市第七中学高三三月份网络教学质量监测卷化学试题四川省宜宾市叙州区第一中学校2020届高三下学期第四学月考试理综化学试题河北省冀州中学2020届高三11月月考化学试题(已下线)小题必刷11 物质的量浓度与溶液的配制——2021年高考化学一轮复习小题必刷(通用版)鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解(已下线)3.1+弱电解质的电离-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 高考帮广西桂林市第十八中学2021届高三上学期第二次月考理科综合化学试题黑龙江省伊春市伊美区第二中学2021届高三上学期开学考试化学试题北京二中2020-2021学年高二上学期10月月考化学试题安徽涡阳县育萃中学2020-2021学年高二上学期第二次月考化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关第25讲 弱电解质的电离平衡(精讲)-2021年高考化学一轮复习讲练测(已下线)3.2.1 水的电离和溶液的酸碱性(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)四川省邻水实验学校2020-2021学年高二上学期第三阶段考试化学试题吉林省四平市实验中学2020-2021学年高二12月月考化学试题河北省石家庄第二中学2020-2021学年高二上学期期中考试化学试题广东省珠海市第二中学2020-2021学年高二上学期10月月考化学试题(已下线)专题02 NA及其应用—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点02 阿伏加德罗常数及应用-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题02化学计量与化学计算-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古包头市第四中学2020-2021学年高二上学期期中考试化学试题湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题(已下线)第21讲 电离平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)广东省中山大学附属中学2022-2023学年高二上学期期中考试化学试题(已下线)第一部分 二轮专题突破 专题14 溶液中的三大平衡及应用湖北省罗田县第一中学2022-2023学年高二上学期12月月考化学试题浙江省宁波市奉化区2022-2023学年高二上学期期末联考化学试题(已下线)T11-电解质溶液第1讲 弱电解质的电离平衡05-2023新东方高二上期中考化学湖南省岳阳市华容县2023-2024学年高二上学期期末考试化学试题辽宁省大连市第四十四中学2022-2023学年高三上学期10月考试化学试题广东省茂名市高州中学2023-2024学年高一下学期期中考试化学试题



