解题方法
1 .  溶液的
溶液的 随温度的变化如图所示。下列说法正确的是
随温度的变化如图所示。下列说法正确的是
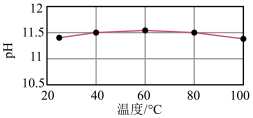
 溶液的
溶液的 随温度的变化如图所示。下列说法正确的是
随温度的变化如图所示。下列说法正确的是
| A.温度高于60℃时,pH变化主要受水的电离平衡移动的影响 |
B.常温下: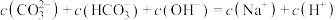 |
C.常温下: |
D.升高温度, 平衡逆向移动 平衡逆向移动 |
您最近一年使用:0次
2 . 草酸( )及其化合物普遍存在于动植物中,在工业上草酸可广泛用作还原剂、除锈剂、沉淀剂等。回答下列问题:
)及其化合物普遍存在于动植物中,在工业上草酸可广泛用作还原剂、除锈剂、沉淀剂等。回答下列问题:
(1)菠菜中含有丰富的草酸及草酸盐,某实验小组为检测菠菜中铁元素的存在,利用灼烧后的菠菜灰(主要含 )进行检验,实验方案如下:
)进行检验,实验方案如下:

①草酸亚铁中碳元素的化合价为___________ ;灼烧过程需要在___________ (填仪器名称)进行。
②试剂M为___________ 。
③取少量滤液,滴加 溶液,溶液的紫红色褪去,说明待测液中含有
溶液,溶液的紫红色褪去,说明待测液中含有 ,该实验方法不严谨,原因是
,该实验方法不严谨,原因是___________ (用离子方程式表示)。
(2)常温下,用 溶液滴定
溶液滴定 溶液,用pH传感器测定滴定过程中溶液的pH变化,滴定曲线如图所示。草酸电离平衡常数
溶液,用pH传感器测定滴定过程中溶液的pH变化,滴定曲线如图所示。草酸电离平衡常数 。
。

①Y点溶质主要成分为___________ 。
②下列说法正确的是___________ (填标号)。
A.滴加NaOH溶液至过量,水的电离程度先增大,后减小
B. 水溶液呈碱性
水溶液呈碱性
C.X点溶液中:
D.Y点溶液中存在关系:
(3)某废水中含少量 ,加入足量
,加入足量 悬浊液将
悬浊液将 转化为
转化为 沉淀除去。已知该温度下
沉淀除去。已知该温度下 、
、 。
。
①该反应的离子方程式为___________ ;
②当 时达至排放标准,恰好达到排放标准时,溶液中
时达至排放标准,恰好达到排放标准时,溶液中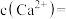
___________ mol/L(保留2位有效数字)。
 )及其化合物普遍存在于动植物中,在工业上草酸可广泛用作还原剂、除锈剂、沉淀剂等。回答下列问题:
)及其化合物普遍存在于动植物中,在工业上草酸可广泛用作还原剂、除锈剂、沉淀剂等。回答下列问题:(1)菠菜中含有丰富的草酸及草酸盐,某实验小组为检测菠菜中铁元素的存在,利用灼烧后的菠菜灰(主要含
 )进行检验,实验方案如下:
)进行检验,实验方案如下:
①草酸亚铁中碳元素的化合价为
②试剂M为
③取少量滤液,滴加
 溶液,溶液的紫红色褪去,说明待测液中含有
溶液,溶液的紫红色褪去,说明待测液中含有 ,该实验方法不严谨,原因是
,该实验方法不严谨,原因是(2)常温下,用
 溶液滴定
溶液滴定 溶液,用pH传感器测定滴定过程中溶液的pH变化,滴定曲线如图所示。草酸电离平衡常数
溶液,用pH传感器测定滴定过程中溶液的pH变化,滴定曲线如图所示。草酸电离平衡常数 。
。
①Y点溶质主要成分为
②下列说法正确的是
A.滴加NaOH溶液至过量,水的电离程度先增大,后减小
B.
 水溶液呈碱性
水溶液呈碱性C.X点溶液中:

D.Y点溶液中存在关系:

(3)某废水中含少量
 ,加入足量
,加入足量 悬浊液将
悬浊液将 转化为
转化为 沉淀除去。已知该温度下
沉淀除去。已知该温度下 、
、 。
。①该反应的离子方程式为
②当
 时达至排放标准,恰好达到排放标准时,溶液中
时达至排放标准,恰好达到排放标准时,溶液中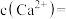
您最近一年使用:0次
名校
解题方法
3 . 常温下,用0.1 mol/LNaOH溶液滴定20 mL等浓度的HA溶液的滴定曲线如图所示,下列说法正确的是


A.常温下,HA的电离平衡常数 |
B.b点溶液中: |
C.d点溶液中: |
| D.水的电离程度:d>c>e |
您最近一年使用:0次
2022-01-19更新
|
209次组卷
|
2卷引用:广东省佛山市2021-2022学年高二上学期期末考试化学试题
解题方法
4 . 已知常温下 HCOOH的电离平衡常数Ka=1.75×10-5,向1 L0.1 mol·L-1的HCOONa溶液中通入HCl气体,溶液中HCOO-和 HCOOH的物质的量浓度变化曲线如图所示(忽略溶液体积变化),下列说法错误的是


| A.0.1 mol·L-I HCOOH溶液pH≈3 |
| B.由N点到M点,溶液的pH不断减小 |
| C.N点溶液中可能存在c(Na+)>c(HCOO-)>c(Cl-)>c(OH-)>c(H+) |
| D.M点时溶液呈碱性 |
您最近一年使用:0次
2021-02-04更新
|
262次组卷
|
2卷引用:广东省佛山市2020-2021学年高二上学期期末考试化学试题
5 . 草酸铵用于制安全炸药和供分析试剂等用,已知数据如表:
关于常温下0.40mol·L-1的(NH4)2C2O4溶液,下列说法错误的是
| 弱电解质 | 草酸(H2C2O4) |  |
| 电离常数(25℃) | K1=5.4×10-2,K2=5.4×10-5 | K=1.8×10-5 |
| A.由表中数据可判断该溶液呈酸性 |
B. |
C.稀释溶液, 减小 减小 |
D. 的水解平衡常数是Kh,Kh的数量级为10-5 的水解平衡常数是Kh,Kh的数量级为10-5 |
您最近一年使用:0次
6 . 常温下,向20mL0.1moL/L的H3PO4溶液中滴加0.1moL/L的 NaOH溶液,所得溶液的pH与NaOH溶液体积的关系如图所示,下列说法正确的是


| A.H3PO4溶液第一步滴定可用酚酞作指示剂 |
| B.A点溶液中c(H2PO4-)>c(H3PO4)>c(HPO42-) |
C.图象中A、B、C三处溶液中 相等 相等 |
| D.B点溶液存在2c(Na+)=c(PO43-)+c(H2PO4-)+c(HPO42-)+c(H3PO4) |
您最近一年使用:0次
2019-01-14更新
|
817次组卷
|
2卷引用:【市级联考】广东省佛山市2019届高三上学期1月教学质量检测(一)理科综合化学试题
7 . 生产碳酸饮料时常加入防腐剂NaA,再加压充入CO2。已知室温下,HA的Ka=6.3×10-5,H2CO3的Ka1=4.2×10-7,Ka2=4.9×10-11,下列说法正确的是
| A.充入CO2能使溶液中c(A-)增大 |
B.当c(H+)= 6.3×10-5,饮料中 =1 =1 |
| C.充入CO2时发生反应;CO2+H2O+A-==HA+HCO3- |
| D.该饮料中粒子浓度关系为:c(HA)+c(H+)=c(OH-)+c(HCO3-)+2(CO32- ) |
您最近一年使用:0次



