解题方法
1 . 甲胺( )是一种一元弱碱。常温下,向
)是一种一元弱碱。常温下,向 中加入等体积
中加入等体积 的
的 。下列说法中正确的是
。下列说法中正确的是
 )是一种一元弱碱。常温下,向
)是一种一元弱碱。常温下,向 中加入等体积
中加入等体积 的
的 。下列说法中正确的是
。下列说法中正确的是A. 在水溶液的电离方程式为: 在水溶液的电离方程式为: |
B.混合后溶液中 |
C. 的 的 溶液中,水电离出来的 溶液中,水电离出来的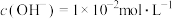 |
D.混合后的溶液中: |
您最近一年使用:0次
名校
2 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多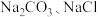 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的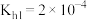 ,则当
,则当 溶液中
溶液中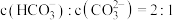 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数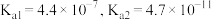 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加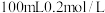 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
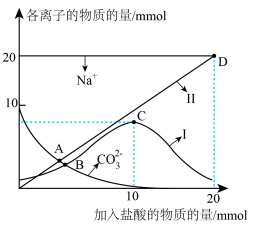
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,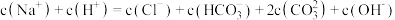
b.滴加至 点时,
点时,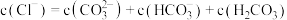
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为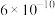 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
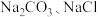 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的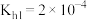 ,则当
,则当 溶液中
溶液中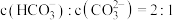 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
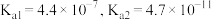 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加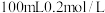 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,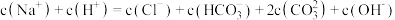
b.滴加至
 点时,
点时,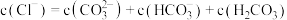
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为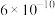 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近一年使用:0次
2023-12-13更新
|
64次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题
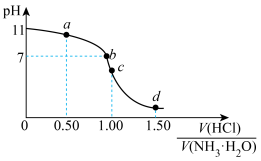
3 . 常温下,用 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示。下列说法错误的是
氨水的滴定曲线如图所示。下列说法错误的是
 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示。下列说法错误的是
氨水的滴定曲线如图所示。下列说法错误的是
A. 时, 时,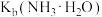 的数量级为 的数量级为 |
B. 点溶液中: 点溶液中: |
C.水的电离程度: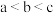 |
D. 点溶液中: 点溶液中: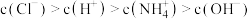 |
您最近一年使用:0次
2023-12-13更新
|
128次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题
名校
4 . 常温下,下列溶液中有关物质的量浓度的关系错误的是
A.pH相等的 、NaOH和 、NaOH和 三种溶液: 三种溶液: |
B.物质的量浓度相等的 和 和 溶液等体积混合: 溶液等体积混合: |
C. 的HA溶液与 的HA溶液与 的MOH溶液以任意比例混合: 的MOH溶液以任意比例混合: |
D. 的NaHA溶液的 的NaHA溶液的 : : |
您最近一年使用:0次
2023-06-08更新
|
151次组卷
|
2卷引用:广东省佛山市龙江中学、勒流中学、北滘中学等十五校2022-2023学年高二上学期12月联考化学试题
名校
5 . 磷能形成次磷酸 、亚磷酸
、亚磷酸 等多种含氧酸,请根据所学知识回答下列问题:
等多种含氧酸,请根据所学知识回答下列问题:
(1)已知 溶液中存在的含磷微粒只有
溶液中存在的含磷微粒只有 、
、 。
。
① 属于
属于_________ 酸。
②写出将 的NaOH溶液逐滴加入10mL
的NaOH溶液逐滴加入10mL 溶液中至过量时发生反应的离子方程式:
溶液中至过量时发生反应的离子方程式:_________ 。
(2)亚磷酸 是二元中强酸,常温下,其电离平衡常数为
是二元中强酸,常温下,其电离平衡常数为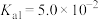 、
、 ,
, 。
。
①常温下, 的
的 溶液呈
溶液呈_________ (填“酸”或“碱”)性,该溶液中含磷微粒的浓度由大到小的顺序为_________ 。
②常温下,向 的
的 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至 ,此时溶液中的
,此时溶液中的
_________ (填精确值) 。
。
③常温下,将NaOH溶液滴加到亚磷酸溶液中,混合溶液的pH随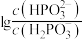 或
或 变化的关系如图所示。
变化的关系如图所示。
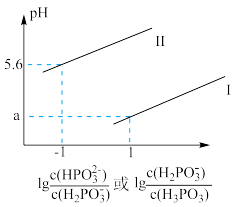
表示 的是曲线
的是曲线_________ (填“Ⅰ”或“Ⅱ”),
_________ 。
 、亚磷酸
、亚磷酸 等多种含氧酸,请根据所学知识回答下列问题:
等多种含氧酸,请根据所学知识回答下列问题:(1)已知
 溶液中存在的含磷微粒只有
溶液中存在的含磷微粒只有 、
、 。
。①
 属于
属于②写出将
 的NaOH溶液逐滴加入10mL
的NaOH溶液逐滴加入10mL 溶液中至过量时发生反应的离子方程式:
溶液中至过量时发生反应的离子方程式:(2)亚磷酸
 是二元中强酸,常温下,其电离平衡常数为
是二元中强酸,常温下,其电离平衡常数为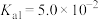 、
、 ,
, 。
。①常温下,
 的
的 溶液呈
溶液呈②常温下,向
 的
的 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至 ,此时溶液中的
,此时溶液中的
 。
。③常温下,将NaOH溶液滴加到亚磷酸溶液中,混合溶液的pH随
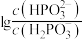 或
或 变化的关系如图所示。
变化的关系如图所示。
表示
 的是曲线
的是曲线
您最近一年使用:0次
2022-12-16更新
|
307次组卷
|
4卷引用:广东省佛山市龙江中学、勒流中学、北滘中学等十五校2022-2023学年高二上学期12月联考化学试题
名校
6 . 在0.1mol/LNa2CO3溶液中,各种微粒之间存在下列关系,其中正确的是
A.c(Na+)+c(H+)=2c(CO )+c(HCO )+c(HCO )+c(OH-) )+c(OH-) | B.2c(Na+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
C.c(OH-)=c(H+)+c(HCO )+c(H2CO3) )+c(H2CO3) | D.c(Na+)>c(OH-)>c(CO )>c(H+) )>c(H+) |
您最近一年使用:0次
2022-12-11更新
|
455次组卷
|
3卷引用:广东顺佛山市顺德区文德学校2021-2022学年高二上学期第二次阶段性测试化学试题
名校
解题方法
7 . 侯氏制碱法以NaCl、CO2、NH3和H2O为原料,制取纯碱并获得副产物NH4Cl,设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1mol NH4Cl和NaCl的混合物中含Cl- 数目为NA |
| B.11.2L CO2所含的分子数目为0.5NA |
| C.等质量的NH3和H2O中含有的电子数均为10NA |
D.1L 1.0mol·L-1 Na2CO3溶液中CO 和HCO 和HCO 的数目之和为NA 的数目之和为NA |
您最近一年使用:0次
名校
8 . 次磷酸(H3PO2)是一元弱酸,可用作杀菌剂。下列说法不正确的是
| A.0.01mol·L-1 H3PO2水溶液的pH>2 |
B.NaH2PO2的水溶液加水稀释, 增大 增大 |
C.NaH2PO2在水溶液的电离方程式为:NaH2PO2=Na+ +H2PO |
D.NaH2PO2的水溶液中:c(Na+)+c(H+)=c(OH-)+c(H2PO )+2c(HPO )+2c(HPO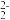 )+3c(PO )+3c(PO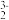 ) ) |
您最近一年使用:0次
名校
解题方法
9 . 常温下,下列有关电解质溶液的说法错误的是
| A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则Ka(HCOOH)>Ka (HF) |
| B.相同浓度的HF和NaF两溶液等体积混合后pH<7,则溶液中c(F—)>c(Na+)>c(H+)>c(OH—) |
| C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则Ksp(FeS)>Ksp(CuS) |
| D.在1mol·L-1Na2S溶液中,c(S2- )+c(HS—)+c(H2S)=1mol·L-1 |
您最近一年使用:0次
解题方法
10 . 常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1的H3PO2溶液,滴定过程中混合溶液的pH随加入的NaOH溶液体积变化关系如图所示,下列说法不正确的是
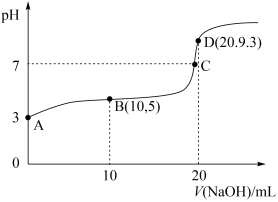

| A.常温下,Ka(H3PO2)的数量级为10—5 |
B.B点对应的溶液中:2[c(H+)—c(OH—)]=c(H2PO )—c(H3PO2) )—c(H3PO2) |
| C.H3PO2为一元弱酸 |
| D.滴定至V=20mL的过程中,溶液中由水电离出的c( H+)·(OH—)不变 |
您最近一年使用:0次
2022-05-02更新
|
548次组卷
|
6卷引用:广东省佛山市禅城区2022-2023学年高三统一调研测试(二) 化学试题
广东省佛山市禅城区2022-2023学年高三统一调研测试(二) 化学试题陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)



