常温下,下列溶液中有关物质的量浓度的关系错误的是
A.pH相等的 、NaOH和 、NaOH和 三种溶液: 三种溶液: |
B.物质的量浓度相等的 和 和 溶液等体积混合: 溶液等体积混合: |
C. 的HA溶液与 的HA溶液与 的MOH溶液以任意比例混合: 的MOH溶液以任意比例混合: |
D. 的NaHA溶液的 的NaHA溶液的 : : |
更新时间:2023-06-08 14:24:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】浓度和体积都相等的盐酸(甲)和醋酸(乙),分别与形状相同且足量的锌反应,下列说法正确的是
| A.反应所需时间:甲=乙 |
| B.反应开始时的速率:甲=乙 |
| C.反应结束所消耗的锌的质量:甲=乙 |
| D.反应结束时的pH值:甲=乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知甲酸的酸性强于乙酸,下列结论不正确 的是
A. 甲酸溶液的pH小于同浓度的乙酸溶液 甲酸溶液的pH小于同浓度的乙酸溶液 |
B. 甲酸钠溶液的pH大于同浓度的乙酸钠溶液 甲酸钠溶液的pH大于同浓度的乙酸钠溶液 |
C.相同物质的量浓度的甲酸和乙酸溶液分别与Zn反应,初始时甲酸产生 速率更快 速率更快 |
D.相同pH的甲酸和乙酸浴液分别与足量 反应,乙酸产生的 反应,乙酸产生的 总量更多 总量更多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某兴趣小组的同学向一定体积的 溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是

 溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
A.AB段溶液的导电能力不断减弱,说明生成的 不是电解质 不是电解质 |
B.B处溶液的导电能力为0,说明 不是电解质 不是电解质 |
C.a时刻 溶液与稀硫酸恰好完全中和, 溶液与稀硫酸恰好完全中和, 与 与 已完全沉淀 已完全沉淀 |
D.BC段溶液的导电能力不断增大,主要是由于过量的 电离出的离子导电 电离出的离子导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:H2A=H++HA-,HA- ⇌ H++A2-,则下列说法正确的是 ( )
| A.H2A是弱酸 |
| B.向H2A溶液中通入HCl气体,电离平衡逆向移动,则H2A浓度增大 |
| C.向H2A溶液中加入金属Na,电离平衡常数增大 |
| D.0.1mol/L H2A中pH<1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】25℃,向5mL0.1mol•L-1ZnSO4溶液中滴入2滴0.1mol•L-1Na2S溶液,生成白色沉淀ZnS,再滴入2滴0.1mol•L-1CuSO4溶液,白色沉淀变为黑色沉淀CuS。已知Ksp(CuS)=6.4×10-36,Ksp(ZnS)=1.6×10-24。下列说法正确的是
| A.滴入0.1mol•L-1CuSO4溶液后ZnS溶解,Ksp(ZnS)增大 |
| B.白色沉淀变为黑色沉淀的离子方程式为S2-+Cu2+=CuS↓ |
C.向ZnSO4、CuSO4混合溶液中加入过量Na2S溶液,充分反应后静置,则上层清液中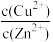 =2.5×1011 =2.5×1011 |
| D.0.1mol•L-1Na2S溶液中存在:c(Na+)=2[c(S2-)+c(HS-)+c(H2S)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,向20mL0.10mol·L 的
的 中滴加0.10mol·L
中滴加0.10mol·L 的盐酸,溶液pH随滴定百分率的变化如图所示。下列说法正确的是
的盐酸,溶液pH随滴定百分率的变化如图所示。下列说法正确的是

 的
的 中滴加0.10mol·L
中滴加0.10mol·L 的盐酸,溶液pH随滴定百分率的变化如图所示。下列说法正确的是
的盐酸,溶液pH随滴定百分率的变化如图所示。下列说法正确的是
A.a点: |
| B.b点溶液中的含碳微粒之和<0.002mol |
| C.水的电离程度:a点>b点 |
D.煮沸是为了除去 ,使突跃变小43.9 ,使突跃变小43.9 |
您最近一年使用:0次

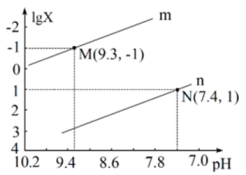
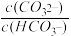 或lg
或lg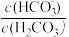 ,下列叙述正确的是
,下列叙述正确的是 +2
+2

 +OH-的平衡常数为1.0×10-7.6
+OH-的平衡常数为1.0×10-7.6
 水解被抑制
水解被抑制 )+c(
)+c(

