解题方法
1 . 氯化铬可用于铬盐生产、镀铬、催化剂生产等工业。以某铝铬铁矿(主要成分是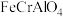 ,还含
,还含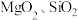 等杂质)为原料制备氯化铬和铝的工艺流程如下:
等杂质)为原料制备氯化铬和铝的工艺流程如下:
已知:镁试剂碱性条件下能与镁离子作用生成天蓝色沉淀。请回答:
(1)步骤1中主要发生反应的离子方程式为__________ ,写出溶液D中的所有阳离子的离子符号:__________ 。步骤4中加氨水调节pH的范围是__________ ,作用是__________ 。
(2)下列说法不正确 的是 。
(3)设计实验检验步骤2所得滤渣是否含镁元素:__________ 。
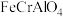 ,还含
,还含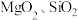 等杂质)为原料制备氯化铬和铝的工艺流程如下:
等杂质)为原料制备氯化铬和铝的工艺流程如下:
金属离子 |
|
|
|
|
|
开始沉淀的pH | 2.3 | 10.4 | 4.9 | 7.5 | 3.4 |
沉淀完全的pH | 4.1 | 12.4 | 6.8 | 9.7 | 4.7 |
(1)步骤1中主要发生反应的离子方程式为
(2)下列说法
| A.步骤1可通过粉碎矿石、加热、搅拌、使用浓硫酸等方法加快浸出速率 |
| B.试剂X和试剂Y不能发生反应 |
| C.溶液E依次通过复分解反应、分解反应、分解反应三步可制取铝单质 |
D.将 和 和 混合加热,则可以得到无水 混合加热,则可以得到无水 |
您最近一年使用:0次
名校
解题方法
2 . 碳酸钠是一种重要的无机化工原料,下列有关说法不正确的是
A.可用加热的方法鉴别固体 和 和 |
B. 溶液呈碱性,可用于洗去油污 溶液呈碱性,可用于洗去油污 |
C.向 固体中加少量水后,会出现放热现象 固体中加少量水后,会出现放热现象 |
D.在氨化的 饱和溶液中通入足量 饱和溶液中通入足量 可得到 可得到 |
您最近一年使用:0次
3 . 工业上由绿矾 和
和 在水溶液中反应得到净水剂聚合硫酸铁
在水溶液中反应得到净水剂聚合硫酸铁 ,下列说法不正确的是
,下列说法不正确的是
 和
和 在水溶液中反应得到净水剂聚合硫酸铁
在水溶液中反应得到净水剂聚合硫酸铁 ,下列说法不正确的是
,下列说法不正确的是| A.聚合硫酸铁易溶于水 |
| B.聚合硫酸铁因在水中形成氢氧化铁胶体而净水 |
C.在相同条件下, 比 比 的水解能力更强 的水解能力更强 |
| D.聚合硫酸铁净水没有杀菌消毒的作用 |
您最近一年使用:0次
名校
4 .  是一种高效氮肥,也是一种烈性炸药。下列说法不正确的是
是一种高效氮肥,也是一种烈性炸药。下列说法不正确的是
 是一种高效氮肥,也是一种烈性炸药。下列说法不正确的是
是一种高效氮肥,也是一种烈性炸药。下列说法不正确的是| A.医用硝酸铵速冷冰袋是利用硝酸铵溶于水吸热的性质 |
| B.将结块的硝酸铵置于研钵中,用研杵敲碎,研细 |
| C.施化肥时,不能将草木灰和硝酸铵混合使用 |
| D.硝酸铵可由氨气和硝酸反应制备,该反应不属于氮的固定 |
您最近一年使用:0次
5 . 下列说法不正确的是
| A.FeO是一种黑色粉末,不稳定,在空气中受热,能迅速被氧化成Fe3O4 |
| B.使用氯气对自来水消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人体有害 |
| C.检验亚铁离子时,可在氯化亚铁溶液中滴加酸性高锰酸钾溶液观察紫红色是否褪去 |
| D.硫酸亚铁、硫酸铝可用于污水处理 |
您最近一年使用:0次
解题方法
6 . 纳米 被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有
被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有 的
的 溶液制备纳米
溶液制备纳米 :
:

已知:在较高的盐酸浓度下, 与
与 、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
(1)操作B的名称是______ ,试剂X为______ 。
(2)步骤Ⅳ中发生反应的离子方程式为______ 。
(3)下列有关萃取和分液的说法正确______ 。

A.进行操作A时,溶液中加入乙醚后转移至分液漏斗中,塞上玻璃塞,如图振荡
B.振荡几次后需打开分液漏斗上口玻璃塞放气
C.一次萃取后若在水相检测到 ,需加入乙醚再次萃取
,需加入乙醚再次萃取
D.为了加快反应速率,Ⅳ应将 溶液一次性加入溶液Ⅱ中,有利于
溶液一次性加入溶液Ⅱ中,有利于 沉淀的生成
沉淀的生成
E.分液漏斗中液体的总体积不超过其容量的
(4)市售PAC是由 水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝
水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝 ,简称
,简称 。
。 含量的高低直接影响PAC的净水效能。向
含量的高低直接影响PAC的净水效能。向 溶液中缓慢滴加一定量
溶液中缓慢滴加一定量 溶液,若只生成
溶液,若只生成 ,则理论上
,则理论上
_______ 。
(5)为了发挥PAC净水的最佳效能,一般要将水的 调节在
调节在 。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因_______ 。
 被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有
被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有 的
的 溶液制备纳米
溶液制备纳米 :
:
已知:在较高的盐酸浓度下,
 与
与 、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:(1)操作B的名称是
(2)步骤Ⅳ中发生反应的离子方程式为
(3)下列有关萃取和分液的说法正确

A.进行操作A时,溶液中加入乙醚后转移至分液漏斗中,塞上玻璃塞,如图振荡
B.振荡几次后需打开分液漏斗上口玻璃塞放气
C.一次萃取后若在水相检测到
 ,需加入乙醚再次萃取
,需加入乙醚再次萃取D.为了加快反应速率,Ⅳ应将
 溶液一次性加入溶液Ⅱ中,有利于
溶液一次性加入溶液Ⅱ中,有利于 沉淀的生成
沉淀的生成E.分液漏斗中液体的总体积不超过其容量的

(4)市售PAC是由
 水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝
水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝 ,简称
,简称 。
。 含量的高低直接影响PAC的净水效能。向
含量的高低直接影响PAC的净水效能。向 溶液中缓慢滴加一定量
溶液中缓慢滴加一定量 溶液,若只生成
溶液,若只生成 ,则理论上
,则理论上
(5)为了发挥PAC净水的最佳效能,一般要将水的
 调节在
调节在 。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
您最近一年使用:0次
7 . 下列关于元素及其化合物的说法不正确的是。
| A.氢气与氯气混合点燃可用于工业制盐酸 |
| B.工业炼铁、制玻璃、水泥的原料都有石灰石 |
| C.实验室配制氯化铁溶液是将氯化铁固体溶解在浓盐酸中,再加适量水稀释 |
| D.实验室可用加热浓氨水快速制取氨气 |
您最近一年使用:0次
8 . 废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO2.某研究小组设计如图所示工艺流程制备硫酸镍晶体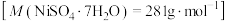 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
(1)“滤渣2”的成分是___________ (用化学式表示)。溶液中加入H2O2的目的是___________ (用离子方程式表示)。
(2)“调pH”可选用的物质___________ (填序号)。
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为___________ 。
(3)下列有关说法不正确 的是___________。
(4)测定产品的纯度。
计算产品的纯度为___________ 。
 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 7.2 | 4.0 | 2.2 | 7.5 |
| 沉淀完全的pH | 9.0 | 5.6 | 3.2 | 9.0 |
(1)“滤渣2”的成分是
(2)“调pH”可选用的物质
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为
(3)下列有关说法
| A.酸浸步骤可用水浴加热,以加速反应 |
| B.操作A中的有机溶剂可选用乙醇 |
| C.调pH后过滤,需用玻璃棒对漏斗中的混合物充分搅拌 |
| D.操作B中包含“结晶、过滤、洗涤、煅烧”等操作 |
(4)测定产品的纯度。
| 操作步骤 | 涉及反应 |
| ①准确称取制备的硫酸镍样品5.620g,加入含0.0200molEDTA的二钠盐溶液(用H2Y2-表示),充分反应后定容成100mL。 | 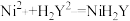 |
②取25.00mL上述溶液于锥形瓶中,加二甲酚橙作指示剂,用 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 |  |
您最近一年使用:0次
9 . 在催化剂( )作用下,HCOOH分解的一种反应机理如图所示。下列说法
)作用下,HCOOH分解的一种反应机理如图所示。下列说法不正确 的是
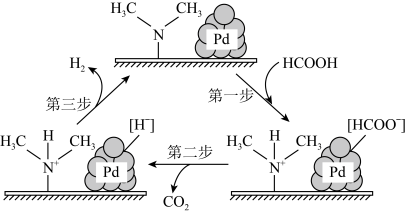
 )作用下,HCOOH分解的一种反应机理如图所示。下列说法
)作用下,HCOOH分解的一种反应机理如图所示。下列说法
A.HCOOH在该催化剂作用下的分解方程式: |
| B.催化剂降低了该反应的活化能,增加了单位体积内的活化分子百分数,有效碰撞次数增加,化学反应速率加快 |
C.若其他条件不变,用HCOOD代替HCOOH,反应除生成 外,还生成 外,还生成 |
D.若其他条件不变,用HCOOK溶液代替HCOOH最终所得气体中 的纯度更高 的纯度更高 |
您最近一年使用:0次
10 . 工业上可以利用 的水解反应生成T
的水解反应生成T ,再经焙烧可得
,再经焙烧可得 ,下列有关说法不正确的是
,下列有关说法不正确的是
 的水解反应生成T
的水解反应生成T ,再经焙烧可得
,再经焙烧可得 ,下列有关说法不正确的是
,下列有关说法不正确的是A. 生成 生成 的化学方程式可表示为: 的化学方程式可表示为: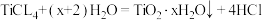 |
| B.制备时可加入大量水,同时加热,促使水解完全 |
C.利用类似方法还可制备SnO、 等化合物 等化合物 |
D. 的性质非常稳定,除制备 的性质非常稳定,除制备 外,还可广泛应用于涂料、橡胶和造纸等 外,还可广泛应用于涂料、橡胶和造纸等 |
您最近一年使用:0次
2023-02-13更新
|
135次组卷
|
2卷引用:浙江省舟山市2022-2023学年高二上学期期末检测化学试题






