1 . 某实验小组通过以下实验,探究镀件表面镀铜的最佳条件。
【查阅资料】①Cu2++2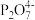
 [Cu(P2O7)2]6-K=1×109
[Cu(P2O7)2]6-K=1×109
②Cu+在溶液中不稳定,容易发生歧化。
【实验设计】用CuSO4·5H2O、Na4P2O7·10H2O(焦磷酸钠)、添加剂配制一定浓度的电镀液,分别用纯铜和镀件作为两极材料,探究电镀液的pH、电流密度、电极板间距对层的影响。
(1)要配制一定体积40g/L的CuSO4溶液,以下仪器不需要用到的是_______ (填仪器名称)。
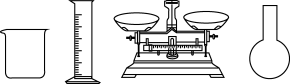
(2)镀件表面的油污可用_______ 清洗。
(3)电镀时阴极上发生的主要反应的电极反应式为_______ 。
【实验结果与数据分析】
ⅰ.其他条件不变时,电位10min,pH对电镀的影响如下表:
(4)实验3中,铜镀层的沉积速率v(Cu)=_______ mol/min(保留两位有效数字)。
(5)实验1和实验4中,酸性或碱性较强时,镀层出现斑驳的可能原因是_______ 。
ⅱ.电流密度、电极板间距与镀膜质量的关系

(6)电流密度小于0.50A/dm2时镀膜质量随电流密度增大而增大的原因是_______ 。
(7)本实验电镀的最佳条件是pH为8.5、_______ 、_______ 。
(8)使用最佳条件电镀时,在阳极附近的电镀液中出现红色固体沉积物,其可能原因用离子方程式表示为_______ ,通空气搅拌可防止红色固体沉积物形成。
【查阅资料】①Cu2++2
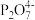
 [Cu(P2O7)2]6-K=1×109
[Cu(P2O7)2]6-K=1×109②Cu+在溶液中不稳定,容易发生歧化。
【实验设计】用CuSO4·5H2O、Na4P2O7·10H2O(焦磷酸钠)、添加剂配制一定浓度的电镀液,分别用纯铜和镀件作为两极材料,探究电镀液的pH、电流密度、电极板间距对层的影响。
(1)要配制一定体积40g/L的CuSO4溶液,以下仪器不需要用到的是

(2)镀件表面的油污可用
(3)电镀时阴极上发生的主要反应的电极反应式为
【实验结果与数据分析】
ⅰ.其他条件不变时,电位10min,pH对电镀的影响如下表:
| 实验信号 | pH值 | 镀膜质量/g | 镀层外观 |
| 1 | 3 | 0.0136 | 表面斑驳 |
| 2 | 7 | 0.0258 | 光亮,不光滑 |
| 3 | 8.5 | 0.0356 | 光亮,光滑 |
| 4 | 10 | 0.0216 | 表面部分斑驳 |
(5)实验1和实验4中,酸性或碱性较强时,镀层出现斑驳的可能原因是
ⅱ.电流密度、电极板间距与镀膜质量的关系

(6)电流密度小于0.50A/dm2时镀膜质量随电流密度增大而增大的原因是
(7)本实验电镀的最佳条件是pH为8.5、
(8)使用最佳条件电镀时,在阳极附近的电镀液中出现红色固体沉积物,其可能原因用离子方程式表示为
您最近一年使用:0次
解题方法
2 . 某工业废玻璃粉末含SiO2、Fe2O3、CeO2、FeO等。某课题小组设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵矾。
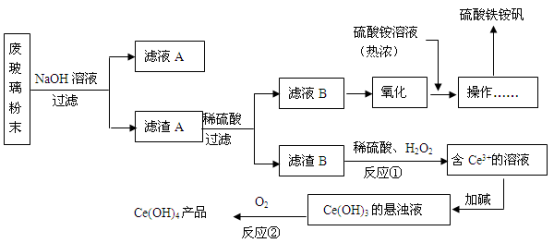
已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。
(1)硫酸铁铵矾可净水,其原理是(写离子方程式)________________________________ 。
(2)滤液A的主要成分_______________ (填写化学式)。
(3)反应①的离子方程式是_____________________________ 。
(4)反应②的化学反应方程式是__________________________ 。
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是_________ 。
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3(水层)+ 6HT(有机层) 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)
分液得到CeT3(有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是___ (从平衡移动角度回答)。

已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。
(1)硫酸铁铵矾可净水,其原理是(写离子方程式)
(2)滤液A的主要成分
(3)反应①的离子方程式是
(4)反应②的化学反应方程式是
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3(水层)+ 6HT(有机层)
 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)分液得到CeT3(有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是
您最近一年使用:0次
2016-12-08更新
|
583次组卷
|
4卷引用:2020届高三化学大二轮增分强化练—— 化学工艺流程题
2020届高三化学大二轮增分强化练—— 化学工艺流程题(已下线)专题七 工艺流程题(提分特训)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训2015届广东湛江高三第二次模拟考试理综化学试卷2015届广东省湛江市高三普通高考测试(二)理综化学试卷
3 . 废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO2.某研究小组设计如图所示工艺流程制备硫酸镍晶体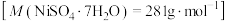 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
(1)“滤渣2”的成分是___________ (用化学式表示)。溶液中加入H2O2的目的是___________ (用离子方程式表示)。
(2)“调pH”可选用的物质___________ (填序号)。
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为___________ 。
(3)下列有关说法不正确 的是___________。
(4)测定产品的纯度。
计算产品的纯度为___________ 。
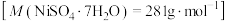 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 7.2 | 4.0 | 2.2 | 7.5 |
| 沉淀完全的pH | 9.0 | 5.6 | 3.2 | 9.0 |
(1)“滤渣2”的成分是
(2)“调pH”可选用的物质
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为
(3)下列有关说法
| A.酸浸步骤可用水浴加热,以加速反应 |
| B.操作A中的有机溶剂可选用乙醇 |
| C.调pH后过滤,需用玻璃棒对漏斗中的混合物充分搅拌 |
| D.操作B中包含“结晶、过滤、洗涤、煅烧”等操作 |
(4)测定产品的纯度。
| 操作步骤 | 涉及反应 |
| ①准确称取制备的硫酸镍样品5.620g,加入含0.0200molEDTA的二钠盐溶液(用H2Y2-表示),充分反应后定容成100mL。 | 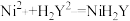 |
②取25.00mL上述溶液于锥形瓶中,加二甲酚橙作指示剂,用 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 |  |
您最近一年使用:0次
解题方法
4 . 某实验小组用废铁屑制备Fe(NO3)2·6H2O的流程如图1所示。

已知:Fe(NO3)2·6H2O呈淡绿色,熔点为60.5℃,易溶于水。FeSO4·7H2O在60℃时溶解度最大,温度降低会结晶析出。
回答下列问题:
(1)步骤Ⅰ的目的是_______ 。
(2)步骤Ⅱ的趁热过滤装置如图2所示,下列说法正确的是_______ (填标号)。

A.漏斗颈要紧贴接受滤液的容器内壁,以加快过滤速度
B.漏斗颈要短,以免过滤时溶液在漏斗颈内停留过久,因散热降温析出晶体而堵塞
C.过滤前先用少量热溶剂润湿滤纸,以免干燥的滤纸吸附溶剂而使溶液浓缩析出晶体
(3)步骤Ⅲ的抽滤装置如图3所示,若转移BaSO4沉淀时,烧杯内壁残留少量沉淀,可用吸滤瓶中的滤液进行冲洗。冲洗操作的合理顺序为(填标号,下同)→_______ →将BaSO4及滤液转移至布氏漏斗。

a.拔掉橡皮管 b.拔下布氏漏斗 c.将吸滤瓶倾斜支管口向上 d.将吸滤瓶倾斜支管口向下 e.从支管小心倒出滤液冲洗沉淀 f.从上口用玻璃棒引流部分滤液入烧杯
(4)步骤Ⅳ中一系列操作包括减压蒸馏、冷却结晶、抽滤、洗涤、真空干燥。蒸馏时减压的目的是_______ 。
(5)产品分析:称取1.000 g制备的试样,加入适量浓盐酸溶解,用还原剂除去 并将Fe3+还原成Fe2+,再除去过量还原剂,进行适当处理后用标准的氧化性试剂A进行滴定。
并将Fe3+还原成Fe2+,再除去过量还原剂,进行适当处理后用标准的氧化性试剂A进行滴定。
①用离子方程式表示加入浓盐酸,试样溶液中Fe2+变为Fe3+的原因:_______ 。
②若某同学用标准KMnO4溶液作为试剂A,测定结果总是偏大,试回答可能原因:_______ 。

已知:Fe(NO3)2·6H2O呈淡绿色,熔点为60.5℃,易溶于水。FeSO4·7H2O在60℃时溶解度最大,温度降低会结晶析出。
回答下列问题:
(1)步骤Ⅰ的目的是
(2)步骤Ⅱ的趁热过滤装置如图2所示,下列说法正确的是

A.漏斗颈要紧贴接受滤液的容器内壁,以加快过滤速度
B.漏斗颈要短,以免过滤时溶液在漏斗颈内停留过久,因散热降温析出晶体而堵塞
C.过滤前先用少量热溶剂润湿滤纸,以免干燥的滤纸吸附溶剂而使溶液浓缩析出晶体
(3)步骤Ⅲ的抽滤装置如图3所示,若转移BaSO4沉淀时,烧杯内壁残留少量沉淀,可用吸滤瓶中的滤液进行冲洗。冲洗操作的合理顺序为(填标号,下同)→

a.拔掉橡皮管 b.拔下布氏漏斗 c.将吸滤瓶倾斜支管口向上 d.将吸滤瓶倾斜支管口向下 e.从支管小心倒出滤液冲洗沉淀 f.从上口用玻璃棒引流部分滤液入烧杯
(4)步骤Ⅳ中一系列操作包括减压蒸馏、冷却结晶、抽滤、洗涤、真空干燥。蒸馏时减压的目的是
(5)产品分析:称取1.000 g制备的试样,加入适量浓盐酸溶解,用还原剂除去
 并将Fe3+还原成Fe2+,再除去过量还原剂,进行适当处理后用标准的氧化性试剂A进行滴定。
并将Fe3+还原成Fe2+,再除去过量还原剂,进行适当处理后用标准的氧化性试剂A进行滴定。①用离子方程式表示加入浓盐酸,试样溶液中Fe2+变为Fe3+的原因:
②若某同学用标准KMnO4溶液作为试剂A,测定结果总是偏大,试回答可能原因:
您最近一年使用:0次
名校
5 . 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为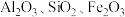 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:___________ , 的空间构型是
的空间构型是___________ 。
(2)“焙烧”时,需将赤泥粉碎的目的是___________ 。
(3)酸浸渣的主要成分是___________ (填化学式)。
(4)“氧化”时发生反应的离子方程式为___________ 。室温下,向氧化后的溶液中滴加 溶液至
溶液至 时,溶液中的
时,溶液中的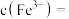
___________  。(已知
。(已知 ,
, 的
的 )
)
(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同 条件下加入PAFS【
条件下加入PAFS【 】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析
】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为___________ 。___________ ,若晶体密度为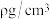 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为___________  (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示,写出计算式即可)。
表示,写出计算式即可)。
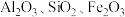 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
 的空间构型是
的空间构型是(2)“焙烧”时,需将赤泥粉碎的目的是
(3)酸浸渣的主要成分是
(4)“氧化”时发生反应的离子方程式为
 溶液至
溶液至 时,溶液中的
时,溶液中的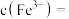
 。(已知
。(已知 ,
, 的
的 )
)(5)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同
 条件下加入PAFS【
条件下加入PAFS【 】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析
】并测定其去浊率,结果如图所示。(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为
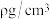 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为 (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示,写出计算式即可)。
表示,写出计算式即可)。
您最近一年使用:0次
2023-05-29更新
|
586次组卷
|
4卷引用:2023年广东卷高考真题变式题(工业流程题)
(已下线)2023年广东卷高考真题变式题(工业流程题)广东省华南师范大学附属中学2023届高三下学期第三次模拟考试化学试题广东省广州市天河外国语学校2024届高三1月校考化学试题广东省汕头市潮南区科利园实验学校2024届高三下学期第三次模拟考试化学
6 . 人民日报曾提出“废渣不废,废水金贵”,为实现资源的阶梯应用,科研工作者以镍黄渣为原料,采用以下工艺流程可制备纯净的NiCO3,相应的滤渣用于回收其他金属。已知:镍黄渣中含NiSO4,还包括铜、铁、锌、钙、镁、铝、铬、锰、钴等金属杂质离子及不溶物。
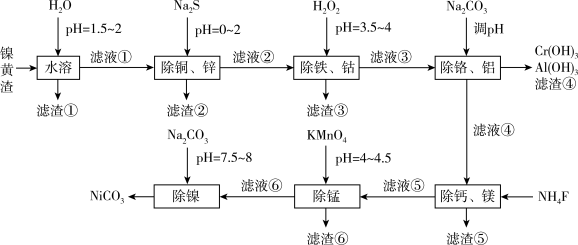
已知该工艺条件下,溶液中金属离子以氢氧化物形式开始沉淀和完全沉淀的pH如下表所示:
(已知:大多数金属离子的配位数等于它电荷数的两倍)
回答下列问题:
(1)已知实验温度下Ksp(ZnS)=2.1×10-25、Ksp (CuS)=6.3×10-35,“除铜、锌”时,当溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子已经沉淀完全,则滤液②中Cu2+的浓度不大于_______ (假设其他离子不反应)。
(2)“除铁、钴”时,H2O2可以将Co2+氧化为Co3+,由流程分析滤渣③成分是_______ 。
(3)“除铬、铝”时,理论上应调节溶液pH范围为_______ ,其中除去Al3+的离子方程式为_______ 。
(4)“除钙、镁”所得滤渣⑤在酸性条件下的溶解度增大的原因(从平衡移动的角度解释)_______ 。
(5)“除锰”时,Mn2+的氧化产物可用于实验室制备氯气,写出“除锰”反应的离子方程式:_______ 。
(6)“沉镍”时,控制终点pH=7.5~8,其主要目的是_______ 。碳酸镍可用于催化剂、电镀、陶瓷器着色等,它受热易分解,不溶于水,易溶于氨水或稀酸,写出碳酸镍溶于氨水的离子方程式:_______ 。

已知该工艺条件下,溶液中金属离子以氢氧化物形式开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Ni2+ | Co2+ | Co3+ | Al3+ | Cr3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 8.1 | 7.6 | 0.56 | 4.0 | 4.3 | 7.8 |
| 完全沉淀pH | 3.2 | 9.0 | 9.5 | 9.2 | 1.1 | 5.2 | 5.4 | 10.4 |
回答下列问题:
(1)已知实验温度下Ksp(ZnS)=2.1×10-25、Ksp (CuS)=6.3×10-35,“除铜、锌”时,当溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子已经沉淀完全,则滤液②中Cu2+的浓度不大于
(2)“除铁、钴”时,H2O2可以将Co2+氧化为Co3+,由流程分析滤渣③成分是
(3)“除铬、铝”时,理论上应调节溶液pH范围为
(4)“除钙、镁”所得滤渣⑤在酸性条件下的溶解度增大的原因(从平衡移动的角度解释)
(5)“除锰”时,Mn2+的氧化产物可用于实验室制备氯气,写出“除锰”反应的离子方程式:
(6)“沉镍”时,控制终点pH=7.5~8,其主要目的是
您最近一年使用:0次
16-17高二上·北京·期末
名校
解题方法
7 . 有一种细菌在酸性水溶液中,有氧气的情况下,可以将黄铜矿(主要成分是CuFe ,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
已知:
回答下列问题:
(1)试剂a是_________ ,调节溶液的pH值,为使Fe3+完全沉淀,合适pH的范围是_______ 。
(2)试剂b为________ ,请写出反应III的离子方程式________________ 。
(3)固体A成份是________ 。
(4)欲从滤液中获得绿矾晶体,操作I应为________________ 、洗涤干燥。
(5)反应I中参加反应的n(CuFeS2):n(O2)=________________ 。
 ,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
,含少量杂质SiO2)氧化为硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
已知:
| Fe2+ | Cu2+ | Fe3+ | |
| 开始转化成氢氧化物沉淀时的pH | 7.6 | 4.7 | 2.7 |
| 完全转化成氢氧化物沉淀时的pH | 9.6 | 6.7 | 3.7 |
回答下列问题:
(1)试剂a是
(2)试剂b为
(3)固体A成份是
(4)欲从滤液中获得绿矾晶体,操作I应为
(5)反应I中参加反应的n(CuFeS2):n(O2)=
您最近一年使用:0次



