1 . 已知p(A)=-lgc平(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
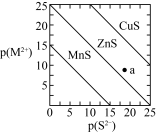

| A.a点没有ZnS沉淀生成 |
| B.可用MnS除去MnCl2溶液中混有的少量ZnCl2 |
| C.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c平(S2-)增大 |
D.CuS和MnS共存的悬浊液中,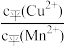 =10-20 =10-20 |
您最近一年使用:0次
2021-04-29更新
|
850次组卷
|
19卷引用:上海市上海中学2023-2024学年高二上学期期中考试化学试题
上海市上海中学2023-2024学年高二上学期期中考试化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】湖北省浠水县实验高级中学2018-2019学年高二上学期12月月考化学试题.湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题12 溶度积的应用复习题山东省临朐县实验中学2020-2021学年高二上学期12月月结学情检测化学试题青海省湟川中学2020-2021学年高二上学期期中考试化学试题四川省成都市蒲江县蒲江中学2020-2021学年高二3月月考化学试题吉林省长春市第二中学2021-2022学年高二上学期期中考试化学试题河南省潢川第一中学2022-2023学年高二上学期期末考试化学试题浙江省杭州市长河高级中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第九中学2022-2023学年高二上学期期末化学试题宁夏石嘴山市平罗中学2022-2023学年高二下学期3月月考化学试题 黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期11月月考化学试题河北省沧州市普通高中高三上学期教学质量监测(联考)化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)2022年山东省高考真题变式题(不定项选择题)甘肃省张掖市高台县第一中学2022-2023学年高三上学期第四次检测化学试题
名校
2 . 下列说法不正确的是
| A.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)⇌Mg2+(aq)+2OH-,该固体可溶于NH4Cl溶液 |
| B.向ZnS沉淀上滴加CuSO4溶液沉淀变为黑色,可推知同温下Ksp(ZnS)<Ksp(CuS) |
| C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色,反应的离子方程式为:2AgCl(s)+S2-(aq)⇌Ag2S(s)+2Cl-(aq) |
| D.向2mL浓度均为1.2 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1的AgNO3溶液,振荡沉淀呈黄色,说明Ksp(AgCl)>Ksp(AgI) |
您最近一年使用:0次
2021-01-07更新
|
394次组卷
|
10卷引用:上海市控江中学2023-2024学年高二上学期等级班阶段测验卷二 化学试题
上海市控江中学2023-2024学年高二上学期等级班阶段测验卷二 化学试题湖南省长沙市南雅中学2020-2021学年高二上学期第三次月考化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期末考试化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题山东省百师联盟2023-2024学年高二上学期12月大联考化学试题 四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
13-14高三上·湖北黄冈·期末
名校
解题方法
3 . 化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),下列说法错误的是
CuS(s)+Mn2+(aq),下列说法错误的是
 CuS(s)+Mn2+(aq),下列说法错误的是
CuS(s)+Mn2+(aq),下列说法错误的是| A.MnS的Ksp比CuS的Ksp大 |
| B.该反应达到平衡时c(Mn2+)=c(Cu2+) |
| C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 |
D.该反应的平衡常数K=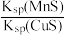 |
您最近一年使用:0次
2020-12-16更新
|
906次组卷
|
38卷引用:上海市行知中学2022-2023学年高二下学期2月月考化学试题
上海市行知中学2022-2023学年高二下学期2月月考化学试题(已下线)2013-2014学年江西省鹰潭一中高二上学期期中考试化学试卷2015-2016学年河北邯郸魏县一中、曲周县一中高二上期中化学试卷辽宁省抚顺市第十九中学2016-2017学年高二上学期期中考试化学试题内蒙古集宁一中西校区2017-2018学年高二上学期期中考试化学试题陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(基础卷)试题(已下线)2019年11月19日《每日一题》高二化学人教版(选修4)—— 沉淀溶解平衡在物质分离中的应用山西省朔州市怀仁一中2019-2020学年高二上学期第四次月考化学试题河北省邯郸市大名县第一中学2019-2020学年高二上学期12月月考化学试题(普通班)四川省广元川师大万达中学2019-2020学年高二上学期期末教学质量检测化学试题云南省丽江市华坪县第一中学2019—2020学年高二上学期期末考试化学试题辽宁省抚顺市六校协作体2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市宾县第一中学2019-2020学年高二上学期期末考试化学试题湖南省长沙市雨花区2019-2020学年高二上学期期末考试化学(选考)试题黑龙江省哈尔滨师范大学附属中学2020-2021学年高二上学期期中考试化学试题重庆市万州纯阳中学2020-2021学年高二上学期期中考试化学试题陕西省宝鸡市宝鸡中学2020-2021学年高二上学期阶段考试(一)化学试题四川省成都市郫都区川科外国语学校2020-2021学年高二11月月考化学试题黑龙江省哈尔滨市延寿县第二中学2020-2021学年高二11月月考化学试题安徽省怀宁中学2020-2021学年高二上学期第二次质量检测(普通班)化学试题陕西省榆林市第十二中学2020-2021学年高二下学期第一次月考化学试题安徽省安庆市九一六学校2020—2021学年高二4月月考化学试题云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题安徽省蚌埠第三中学2021-2022学年高二下学期开学测试化学试题第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用陕西省咸阳市秦都区2021-2022学年高二上学期期末考试化学试题青海省西宁市海湖中学2023-2024学年高二下学期开学考试化学试卷(已下线)2013届湖北省黄冈市高三上学期期末考试理综化学试卷(已下线)2014高考化学二轮复习限时集训 专题8电解质溶液练习卷A(已下线)2014高考名师推荐化学溶度积、沉淀的生成、溶解、转化(已下线)2013-2014四川省攀枝花市高三5月模拟考试理综化学试卷福建省福州市长乐高级中学2020届高三上学期第一次月考化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第5讲 难溶电解质的溶解平衡
名校
4 . 关于饱和食盐水,说法正确的是( )
| A.再加食盐不会发生溶解 | B.再加食盐不会发生结晶 |
| C.其中溶解速率等于结晶速率 | D.加水稀释不影响溶解平衡 |
您最近一年使用:0次
2020-11-10更新
|
470次组卷
|
2卷引用:上海市松江区松江二中2020-2021学年高二上学期期中考试化学试题
名校
解题方法
5 . 已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述正确的是
| A.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 |
| C.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
| D.向AgCl的饱和溶液中加入NaCl晶体有AgCl析出,溶液中c(Ag+)仍与c(Cl-)相等 |
您最近一年使用:0次
2020-11-03更新
|
273次组卷
|
4卷引用:上海市上海中学2022-2023学年高二上学期期中考试化学试题
上海市上海中学2022-2023学年高二上学期期中考试化学试题上海市新中高级中学2023-2024学年高二下学期阶段检测化学试题 重庆市秀山高级中学校2020-2021学年高二上学期10月月考化学试题(已下线)专题3.4.1 难溶电解质的溶解平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
名校
解题方法
6 . 下列关于沉淀溶解平衡的说法正确的是
| A.只有难溶电解质才存在沉淀溶解平衡 |
| B.沉淀溶解平衡是可逆的 |
C.在平衡状态时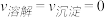 |
| D.达到沉淀溶解平衡的溶液不一定是饱和溶液 |
您最近一年使用:0次
2020-10-05更新
|
410次组卷
|
4卷引用:上海市第三女子中学2023-2024学年高二上学期等级班12月测试化学试题
解题方法
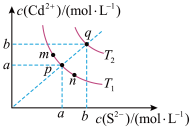
7 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料。其在水中CdS(s) Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
 Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
Cd2+(aq)+S2-(aq),达到沉淀溶解平衡时,定义溶度积Ksp=c(Cd2+)·c(S2-)。下图为CdS的沉淀溶解平衡曲线。下列说法错误的是
| A.图中a和b分别为T1、T2温度下CdS在水中的溶解度 |
| B.图中各点对应的Ksp的关系为:Ksp(m)<Ksp(n)<Ksp(p)<Ksp(q) |
| C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动 |
| D.加水稀释,q点沿qp线向p方向移动 |
您最近一年使用:0次
真题
名校
8 . 二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误的是
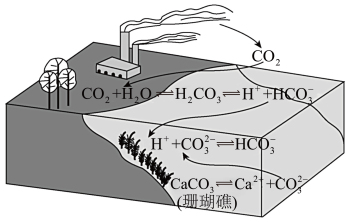

A.海水酸化能引起 浓度增大、 浓度增大、 浓度减小 浓度减小 |
| B.海水酸化能促进CaCO3的溶解,导致珊瑚礁减少 |
C.CO2能引起海水酸化,其原理为  H++ H++ |
| D.使用太阳能、氢能等新能源可改善珊瑚的生存环境 |
您最近一年使用:0次
2020-07-08更新
|
12120次组卷
|
48卷引用:上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题
上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题上海师范大学附属中学宝山分校2023-2024学年高二上学期12月阶段性测试 化学(等级)试题吉林省长春市实验中学2020-2021学年高二上学期开学考试化学试题上海市七宝中学2021届高三上学期期中考试化学试题河南省开封市铁路中学2020-2021学年高二下学期期中考试化学试题选择性必修1 专题3素养检测(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)湖北省蕲春县2021-2022学年高二上学期期中考试化学试题四川省内江市第六中学2021-2022学年高二下学期入学考试(创新班)化学试题江苏省南通市海安李堡中学2021-2022学年高二上学期期中考试化学试题广东省广州市第一中学2022-2023学年高二上学期期末考试化学试题2020年全国统一考试化学试题(新课标Ⅱ)(已下线)专题10 水溶液中的离子平衡-2020年高考真题和模拟题化学分项汇编(已下线)专题01 STSE 化学用语-2020年高考真题和模拟题化学分项汇编(已下线)第06讲 离子反应 离子方程式(精讲)——2021年高考化学一轮复习讲练测甘肃省武威第六中学2021届高三上学期第三次过关考试化学试题河南省郑州市巩义市第四高级中学2021届高三上学期期中考试化学试题(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)小题02 化学与社会生产生活环境(STSE)——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)第04讲 离子反应 离子方程式(精讲)-2022年一轮复习讲练测(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第4讲 离子反应 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向24 弱电解质的电离平衡-备战2022年高考化学一轮复习考点微专题(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)江苏省徐州市王杰中学2021-2022学年高三10月学情调研化学试题(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)2020年全国卷Ⅱ化学真题变式题天津市部分区2021-2022学年高三上学期期末考试化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)湖南省娄底涟源市第一中学2022届高三下学期四月月考化学试题新疆喀什市普通高中2021-2022学年高三上学期期末考试化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第21讲 电离平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)陕西省富平县蓝光中学2021-2022学年高三上学期期末教学检测化学试题(已下线)第一部分 二轮专题突破 专题8 常见无机物性质的转化(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第52讲 难溶电解质的溶解平衡(已下线)题型64 碳及其化合物的性质(已下线)第7讲 碳、硅及无机非金属材料(已下线)第5讲 难溶电解质的溶解平衡
名校
解题方法
9 . 某同学为了验证难溶的氯化银在水中也存在溶解平衡,设计了如下实验方案:( )
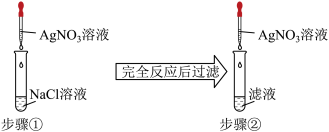

| A.步骤①中应加入过量的AgNO3溶液 |
| B.步骤①中应使NaCl溶液过量 |
| C.步骤②中现象是无沉淀产生 |
| D.步骤②中选用的AgNO3溶液浓度应小于步骤① |
您最近一年使用:0次
名校
解题方法
10 . 现有25℃时0.1mol•L-1的氨水,请回答以下问题:
(1)氨水呈碱性的原因为(用离子方程式表示)___ 。
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式___ ;若所得溶液的pH=5,则溶液中水所电离出的氢离子浓度为___ 。
(3)若向氨水中加入少量硫酸铵固体,此时溶液中
__ (填“增大”、“减小”或“不变”)。
(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=__ 。
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___ 。
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因___ 。
(1)氨水呈碱性的原因为(用离子方程式表示)
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式
(3)若向氨水中加入少量硫酸铵固体,此时溶液中

(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因
您最近一年使用:0次



