名校
1 . 25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
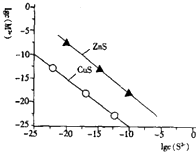

| A.向Cu2+浓度为10-5mol•L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| B.25℃时K甲(CuS)约为1×10-35 |
| C.向100mLZn2+、Cu2+浓度均为10-5mol•L-1的混合溶液中逐滴加入10-4 mol•L-1的Na2S溶液,Cu2+先沉淀 |
| D.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)═2c(Na+) |
您最近一年使用:0次
2 . 对四支分别盛有无色溶液的试管,进行如下操作,结论正确的是
| 操作 | 现象 | 结论 | |
| A | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| B | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向10mL 0.2mol/LNaOH溶液中先滴入2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先有白色沉淀生成,加入FeCl3溶液后,又有红褐色沉淀生成 | 在相同的温度下的Ksp: Mg(OH)2>Fe(OH)3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中一定无NH4+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-14更新
|
533次组卷
|
3卷引用:2017届江西省新余市第一中学高三下学期第七次模拟考试理综化学试卷
名校
3 . 下列说法正确的是
| A.KAl(SO4)2溶液中 c(K+)= 2c(SO42-) |
| B.向NaHCO3溶液中加入少量 Ba(OH)2固体,c(CO32-)增大 |
| C.含有AgCl和AgBr固体的悬浊液中,C(Ag+)>c(Cl-) =c(Br-) |
| D.常温下,向含0.1molCH3COOH的溶液中加入amolNaOH固体,反应后溶液中c(CH3COOH) =c(CH3COO-),则溶液显碱性。(已知醋酸Ka =1.75×10-5 ) |
您最近一年使用:0次
2017-03-09更新
|
369次组卷
|
3卷引用:江西省新余市第四中学2018届高三上学期第三次段考化学试题
4 . 软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。
已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是_________________ (任写一种)。①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______________________ 。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_________ 。
(3)步骤③中MnO2的其作用是__________________ ,另外一种物质X可以是__________ 。
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式__________ 。
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为__________________ 。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______ 。[已知:Ksp(MnS)=1.4×10―15]

已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是
(3)步骤③中MnO2的其作用是
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为
您最近一年使用:0次
2017-02-26更新
|
306次组卷
|
2卷引用:2017届江西省新余市第四中学、宜春中学高三下学期开学联考理科综合化学试卷
5 . 某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是
| A.NaOH | B.ZnO | C.Na2CO3 | D.Fe2O3 |
您最近一年使用:0次
2016-12-09更新
|
573次组卷
|
6卷引用:2013-2014学年江西省新余市高二上学期期末考试化学试卷
(已下线)2013-2014学年江西省新余市高二上学期期末考试化学试卷(已下线)2010年吉林省长春十一中高二上学期期中考试化学试卷2018学年上海市控江中学高二第一学期第一次月考化学考试内蒙古自治区巴彦淖尔市临河区第三中学2019-2020学年高二上学期期末考试化学试题宁夏银川市唐徕中学2022-2023学年高二下学期3月月考化学试题第2课时 沉淀溶解平衡的应用
6 . 镁橄榄石主要成分是Mg2SiO4,电解法促进镁橄榄石固定CO2的工艺流程如下图所示:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
固碳时主要反应的方程式为NaOH(aq)+CO2(g)=NaHCO3(aq)。
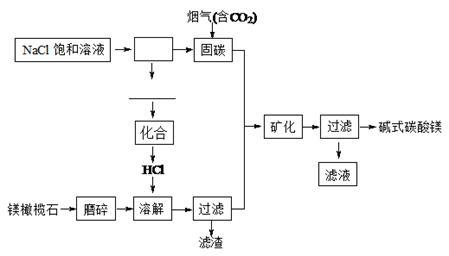
(1)上图方框里的操作名称是________ ,横线上的物质有(填化学式)________ 。
(2)下列物质中也可用作“固碳”的是(填字母序号)________ 。
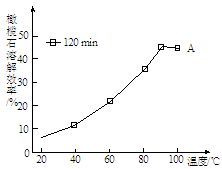
(3)由下图可知,90 ℃后曲线A溶解效率下降,分析其原因______________________ 。
(4)经分析,所得碱式碳酸镁沉淀中含有少量NaCl。为提纯,可采取的方法是_________ 。本流程中可循环利用的物质是(填化学式)_________ 。
(5)另一种橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为__________ 。
已知:Mg2SiO4(s)+4HCl(aq)
 2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1固碳时主要反应的方程式为NaOH(aq)+CO2(g)=NaHCO3(aq)。

(1)上图方框里的操作名称是
(2)下列物质中也可用作“固碳”的是(填字母序号)
| A.CaCl2 | B.NH3·H2O |
| C.Na2CO3 | D.H2O |
(3)由下图可知,90 ℃后曲线A溶解效率下降,分析其原因

(4)经分析,所得碱式碳酸镁沉淀中含有少量NaCl。为提纯,可采取的方法是
(5)另一种橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为
您最近一年使用:0次
2015-05-11更新
|
523次组卷
|
2卷引用:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷



