名校
解题方法
1 . 氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。
回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有___________ 因素。
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
(3)常温时,几种金属离子沉淀的pH如图所示,加 时发生反应的离子方程式为
时发生反应的离子方程式为___________ ;“调pH(Ⅰ)”时,调节溶液 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为___________ (填化学式)。___________ 。
 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: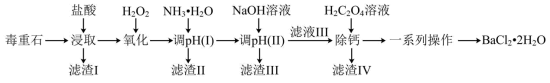
 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.31 | 69.60 | 68.42 | 59.21 | 74.31 | 74.15 | 55.32 | 59.84 | 65.12 | 74.31 | 74.35 |
(3)常温时,几种金属离子沉淀的pH如图所示,加
 时发生反应的离子方程式为
时发生反应的离子方程式为 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案合理,且能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 将乙醇与浓硫酸的混合物加热至170℃,并将产生的气体干燥后通入少量溴的四氯化碳溶液中,观察溴的四氯化碳溶液颜色的变化 | 验证乙醇发生了消去反应 |
| B | 将混有HCl杂质气体的 通入饱和食盐水中 通入饱和食盐水中 | 除去杂质HCl气体 |
| C | 分别测定相同浓度的 溶液和 溶液和 溶液的pH 溶液的pH | 比较 溶液和 溶液和 的酸性 的酸性 |
| D | 向2mL0.1mol/L 溶液中滴入几滴0.1mol/LKCl溶液,生成白色沉淀,再滴加几滴0.1mol/LKI溶液,观察沉淀颜色的变化 溶液中滴入几滴0.1mol/LKCl溶液,生成白色沉淀,再滴加几滴0.1mol/LKI溶液,观察沉淀颜色的变化 | 证明Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-19更新
|
682次组卷
|
6卷引用:江西省南昌市2024届高三第一次模拟测试化学试卷
江西省南昌市2024届高三第一次模拟测试化学试卷江西省南昌市2024届高三下学期第一次模拟测试化学试题2024届河南省焦作市博爱县第一中学高三下学期二模化学试题江西省宜春市宜丰中学2023-2024学年高三下学期3月月考化学试题(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题09?微型化学实验设计与评价(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
3 . 下列实验能达到实验目的是
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸测定浓度为 溶液和 溶液和 溶液的pH 溶液的pH | 比较 和 和 的酸性强弱 的酸性强弱 |
| B | 等体积、pH均为2的HA和HB两种酸分别与足量Zn反应,HA放出的 多 多 | 证明HA是弱酸 |
| C | 室温下,向 溶液中加入几滴 溶液中加入几滴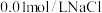 溶液出现白色沉淀,再滴加几滴 溶液出现白色沉淀,再滴加几滴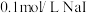 溶液,出现黄色沉淀. 溶液,出现黄色沉淀. | 证明相同温度下: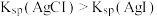 |
| D | 酸式滴定管中硫酸液面在20.00mL,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列用于解释事实的方程式书写不正确的是
A.用明矾作净水剂: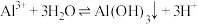 |
B.将水加热至90℃,水的pH变小: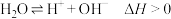 |
C.向氢氧化镁悬浊液中滴入酚酞溶液,溶液变红: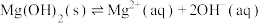 |
D.用碳酸钠溶液处理水垢中的硫酸钙: |
您最近一年使用:0次
名校
解题方法
5 . 利用含钴废料(主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图: 的反应原理:
的反应原理: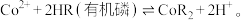 下列说法错误的是
下列说法错误的是
 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图: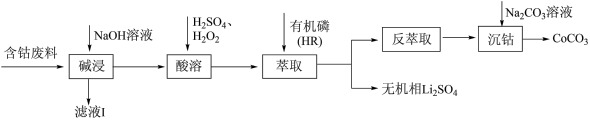
 的反应原理:
的反应原理: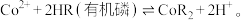 下列说法错误的是
下列说法错误的是A.“滤液Ⅰ”中溶质的主要成分是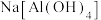 |
B.“反萃取”中可加入 分离出 分离出 |
C.“酸溶”反应中 可以换成 可以换成 |
D.为提高产品的纯度,“沉钴”时 溶液滴加速率不宜过快 溶液滴加速率不宜过快 |
您最近一年使用:0次
2024-01-08更新
|
391次组卷
|
3卷引用:江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷
江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 福建省泉州市第七中学2023-2024学年高三上学期期中考试化学试题 (已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
6 . 常温下,向10.0mL浓度均为0.1mol/L的 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.

已知:①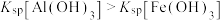 ;
;
②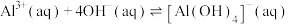 ,298K,
,298K, 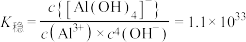 。
。
下列叙述正确的是
 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
已知:①
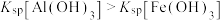 ;
;②
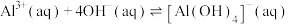 ,298K,
,298K, 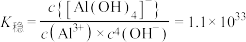 。
。下列叙述正确的是
A.曲线Ⅱ代表 |
B.常温下,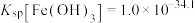 |
C.c点铁铝元素主要存在形式为 和 和 |
D.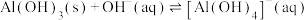 的平衡常数K为 的平衡常数K为 数量级 数量级 |
您最近一年使用:0次
名校
7 . 已知CuS是一种不溶于非氧化性酸的沉淀。下列说法正确并能用勒 夏特列原理解释的是
夏特列原理解释的是
 夏特列原理解释的是
夏特列原理解释的是| A.工业合成SO3采用高压条件以增大平衡转化率 |
B.向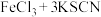  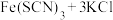 的平衡体系中加入少量KCl固体,溶液颜色变浅 的平衡体系中加入少量KCl固体,溶液颜色变浅 |
C.向氯水中加碳酸钠,可提高溶液中 的浓度 的浓度 |
| D.向饱和H2S溶液中加入少量硫酸铜溶液,溶液酸性增强 |
您最近一年使用:0次
名校
8 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 乙烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的有机物具有酸性 |
| B | 46 g乙醇与足量Na反应生成1 g H2 | 乙醇分子中氢氧键比碳氢键更易断裂 |
| C | 酰胺在酸或碱存在并加热时可水解 | 氨基酸有两性,能发生反应生成肽键 |
| D | FeS去除工业废水中的Hg2+、Cu2+ | FeS具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
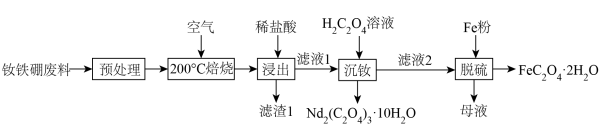
9 . 钕铁硼废料是一种具有较高经济价值的废弃物,主要成分为稀土元素钕(Nd)、Fe、B.一种采用分步沉淀从钕铁硼油泥中回收Nd2(C2O4)3·10H2O和FeC2O4·2H2O的工艺流程如图:
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择___________ (填化学式)溶液。
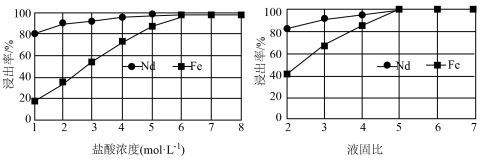
(2)“滤渣1”的主要成分是___________ (填名称)。“浸出”时,盐酸浓度和液固比对钕、铁的浸出率影响如图所示,则浸出过程的最佳条件是___________ 。___________ 。
(4)“沉铁”时,加入铁粉的作用是___________ 。
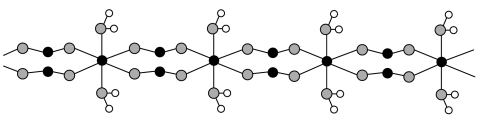
(5)FeC2O4·2H2O晶体结构片段如图所示。___________ ;碳原子采用___________ 杂化。现测定草酸亚铁晶体纯度。准确称取Wg样品于锥形瓶,加入适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液bmL。滴定反应: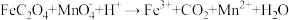 (未配平)。该样品纯度为
(未配平)。该样品纯度为___________ %。
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择
(2)“滤渣1”的主要成分是
(4)“沉铁”时,加入铁粉的作用是
(5)FeC2O4·2H2O晶体结构片段如图所示。
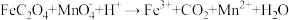 (未配平)。该样品纯度为
(未配平)。该样品纯度为
您最近一年使用:0次
2023-11-01更新
|
1021次组卷
|
5卷引用:2024届江西省南昌市第十九中学高三下学期模拟预测化学试题
名校
解题方法
10 . 废旧铅蓄电池会导致铅污染,回收铅的流程如图所示。
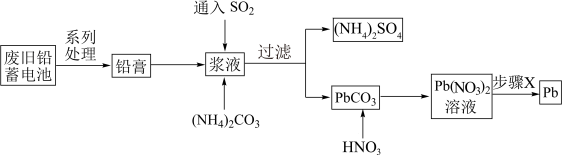
| A.SO2的作用是将PbO2还原成PbSO4 |
B.加入(NH4)2CO3后发生的反应为:PbSO4(s)+CO (aq) (aq) PbCO3(s)+SO PbCO3(s)+SO (aq) (aq) |
| C.步骤X可以是蒸干灼烧 |
| D.若步骤X为电解,则整个流程中,HNO3可循环使用 |
您最近一年使用:0次
2023-09-17更新
|
592次组卷
|
5卷引用:2024届南昌市第十九中学高三下学期模拟预测化学试题



