名校
解题方法
1 . 废旧铅蓄电池会导致铅污染,回收铅的流程如图所示。
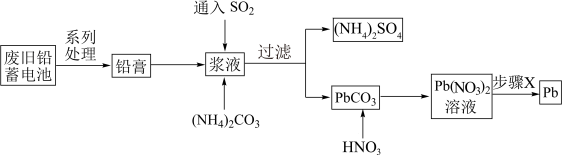
| A.SO2的作用是将PbO2还原成PbSO4 |
B.加入(NH4)2CO3后发生的反应为:PbSO4(s)+CO (aq) (aq) PbCO3(s)+SO PbCO3(s)+SO (aq) (aq) |
| C.步骤X可以是蒸干灼烧 |
| D.若步骤X为电解,则整个流程中,HNO3可循环使用 |
您最近一年使用:0次
2023-09-17更新
|
606次组卷
|
5卷引用:2024届南昌市第十九中学高三下学期模拟预测化学试题
2 . 下图为 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(
关系图( ;
; 可认为
可认为 离子沉淀完全)。下列叙述正确的是
离子沉淀完全)。下列叙述正确的是
 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(
关系图( ;
; 可认为
可认为 离子沉淀完全)。下列叙述正确的是
离子沉淀完全)。下列叙述正确的是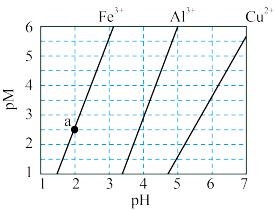
A.由 点可求得 点可求得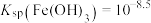 |
B. 时 时 的溶解度为 的溶解度为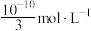 |
C.浓度均为 的 的 和 和 可通过分步沉淀进行分离 可通过分步沉淀进行分离 |
D.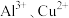 混合溶液中 混合溶液中 时二者不会同时沉淀 时二者不会同时沉淀 |
您最近一年使用:0次
2023-06-09更新
|
16936次组卷
|
33卷引用:江西省南昌市第十九中学2023-2024学年高三上学期11月期中考试化学试卷
江西省南昌市第十九中学2023-2024学年高三上学期11月期中考试化学试卷 2023年高考全国甲卷化学真题(已下线)T13-溶液中的离子平衡(已下线)T13-溶液中的离子平衡(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题16 水溶液中的离子平衡(已下线)2023年高考山东卷化学真题变式题(不定项选择题)(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)第15练 水溶液中的离子平衡图像分析 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)湖南省长沙市长郡中学2022-2023学年高二下学期期末考试化学试题(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)海南省海南中学2023-2024学年高三上学期第0次月考化学试题河南省南阳市第一中学校2023-2024学年高三上学期开学考试化学试题四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)第32讲难溶电解质的溶解平衡(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第6讲 沉淀溶解平衡图像分析福建泉州培元中学2023-2024学年上学期高三10月月考化学试题(已下线)选择题11-16福建省福州第四中学2023-2024学年高三上学期期中考试化学试题(已下线)题型03 电解质溶液图像分析-2024年高考化学答题技巧与模板构建(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)安徽省淮北市2023-2024学年高三上学期1月调研化学试题(已下线)选择题11-15河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)天津市耀华中学2023-2024学年高二上学期1月期末化学试题天津市耀华中学2023-2024学年高二上学期期末学情调研化学试卷山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题
3 . 下列实验过程能达到探究目的的是
| 选项 | 实验过程 | 探究目的 |
| A | 检验Na2SO3中是否混有Na2CO3 | 取少量固体,滴加稀盐酸,观察是否有气体生成 |
| B | 向20%蔗糖溶液中加入少量稀硫酸,加热;再加入银氨溶液,无明显现象 | 蔗糖未发生水解反应 |
| C | 苯和液溴的混合液中加入铁粉,将产生的气体通入硝酸酸化的AgNO3溶液中,产生淡黄色沉淀 | 证明苯与液溴在Fe催化下发生取代反应 |
| D | 向饱和FeSO4溶液中加入CuS固体,测得溶液中c(Fe2+)不变 | Ksp(CuS)<Ksp(FeS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列方案设计、现象和结论正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究1-溴丁烷的消去反应 | 向圆底烧瓶中加入2.0gNaOH和15mL乙醇,搅拌,微热。将产生的气体通入酸性KMnO4溶液中 | 酸性KMnO4溶液褪色,说明1-溴丁烷发生消去反应生成1-丁烯 |
| B | 证明Ksp(CuS)<Ksp(ZnS) | 在2mL0.01mol/L的Na2S溶液中先滴入几滴0.01mol/LZnSO4溶液,再滴入0.01mol/LCuSO4溶液 | 先有白色沉淀生成,又出现黑色沉淀,说明Ksp(CuS)<Ksp(ZnS) |
| C | 探究Fe2+、Br-的还原性强弱 | 向FeBr2溶液中加入过量氯水,再加CCl4萃取 | 若CCl4层无色,则Fe2+的还原性强于Br- |
| D | 证明溴乙烷中还有溴元素 | 取少量溴乙烷与NaOH溶液共热,一段时间后,向反应液中加入足量硝酸,再滴入几滴AgNO3溶液 | 产生淡黄色沉淀,证明溴乙烷中含有溴元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 室温下,通过下列实验探究0.1 NaHS溶液的性质。
NaHS溶液的性质。
下列有关说法正确的是
 NaHS溶液的性质。
NaHS溶液的性质。| 实验 | 实验操作和现象 |
| ① | 滴加几滴酚酞溶液,溶液变红 |
| ② | 加入等体积0.1 NaOH溶液充分混合,无明显现象 NaOH溶液充分混合,无明显现象 |
| ③ | 加入少量 溶液,产生黑色沉淀 溶液,产生黑色沉淀 |
| ④ | 加入适量NaClO溶液,有淡黄色沉淀产生 |
A.实验①溶液中: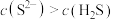 |
B.实验②所得溶液中: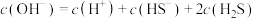 |
C.实验③反应后静置一段时间,上层清液中存在: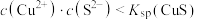 |
D.实验④中反应的离子方程式: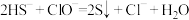 |
您最近一年使用:0次
2023-05-12更新
|
558次组卷
|
3卷引用:江西师范大学附属中学2023-2024学年高三上学期期中考试化学试题
江西师范大学附属中学2023-2024学年高三上学期期中考试化学试题天津市南开区2023届高三下学期质量监测 ( 二 ) 化学试题(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)
名校
解题方法
6 . 含硫化合物的反应具有多样性。下列有关反应的离子方程式书写不正确的是
A.用 溶液吸收 溶液吸收 废气: 废气: |
B.海水提溴工艺中用 还原 还原 : :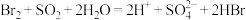 |
C.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 : :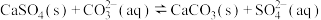 |
D.将S与 溶液混合加热制备 溶液混合加热制备 : :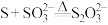 |
您最近一年使用:0次
2023-02-19更新
|
1628次组卷
|
5卷引用:江西省南昌市第十九中学2023-2024学年高三上学期11月期中考试化学试卷
江西省南昌市第十九中学2023-2024学年高三上学期11月期中考试化学试卷 广东省深圳市2022-2023学年高三第一次调研考试化学试题(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)(已下线)专题04 离子反应山西省名校2023-2024学年高三上学期10月联考化学试题
名校
7 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向3mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
B | 向浓度均为0.05mol·L−1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)> Ksp(AgCl) |
C | 某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的 、
、 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的 、
、 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是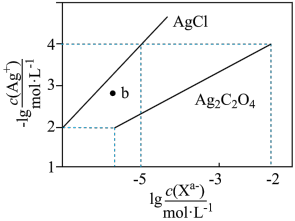
A.b点表示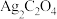 的饱和溶液 的饱和溶液 |
B.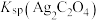 数量级为 数量级为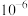 |
C.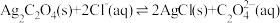 的平衡常数为 的平衡常数为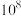 |
D.向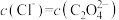 的混合液中滴入 的混合液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
您最近一年使用:0次
2023-01-17更新
|
349次组卷
|
3卷引用:江西省南昌十九中2022-2023学年高二上学期期末考试化学试卷
名校
解题方法
9 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.1mol·Lˉ1 Na2S2O3溶液和5mL 0.1mol·Lˉ1 Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol·Lˉ1H2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),向其中通入氩气,反应速率不变 2NH3(g),向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 探究生成物浓度对化学平衡的影响 | 向2mL 0.1mol·L-1 FeCl3溶液加入1滴KSCN溶液,再加入少量KCl溶液 | 若溶液先变血红色,加入KCl溶液后血红色变浅,说明增大生成物浓度,平衡逆向移动 |
| D | 探究溶度积常数的大小关系 | 向盛有2mL 0.1mol/L NaOH溶液的试管中滴加4~5滴0.1mol/L MgSO4溶液,再向其中滴加0.1mol/L CuSO4溶液 | 先生成白色沉淀,后生成蓝色沉淀,说明Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
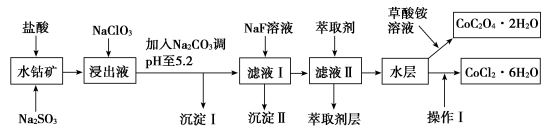
已知:①NaClO3不能氧化CoCl2
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3目的是_______ 。
(2)加入Na2CO3调pH至5.2,目的是_______ ;萃取剂层含锰元素,则沉淀Ⅱ的主要成分为_______ 。
(3)操作Ⅰ包括:将水层加入浓盐酸调整pH为2~3,_______ 、_______ 、过滤、洗涤、减压烘干等过程。
(4)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为_______ 。[已知:CoC2O4·2H2O的摩尔质量为183g·mol−1]

已知:①NaClO3不能氧化CoCl2
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)加入Na2CO3调pH至5.2,目的是
(3)操作Ⅰ包括:将水层加入浓盐酸调整pH为2~3,
(4)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
您最近一年使用:0次



