名校
解题方法
1 . 从废旧磷酸铁锂电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
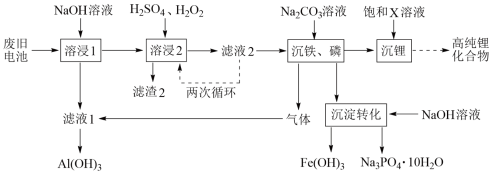
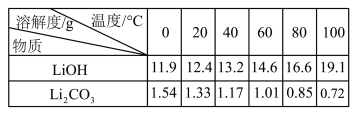
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为___________________________ 。
(2)完成“溶浸2”反应的离子方程式___________________________ :
 LiFePO4+
LiFePO4+ H2O2+
H2O2+ =
= Li++
Li++ +
+ H2PO4-+
H2PO4-+ H2O
H2O
(3)“滤渣2”的主要成分是_______________ 。
(4)“滤液2”循环两次的目的是___________________________ 。
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为_______________________ 。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是___________________________ 。
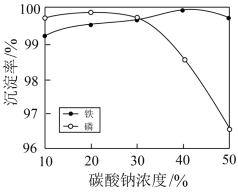
(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是___ (填标号)。
A.NaOH20-40℃B.NaOH80-100℃
C.Na2CO320-40℃D.Na2CO360-80℃


回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为
(2)完成“溶浸2”反应的离子方程式
 LiFePO4+
LiFePO4+ H2O2+
H2O2+ =
= Li++
Li++ +
+ H2PO4-+
H2PO4-+ H2O
H2O(3)“滤渣2”的主要成分是
(4)“滤液2”循环两次的目的是
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为

(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是
A.NaOH20-40℃B.NaOH80-100℃
C.Na2CO320-40℃D.Na2CO360-80℃
您最近一年使用:0次
名校
2 . 下列实验能达到相应的实验目的的是
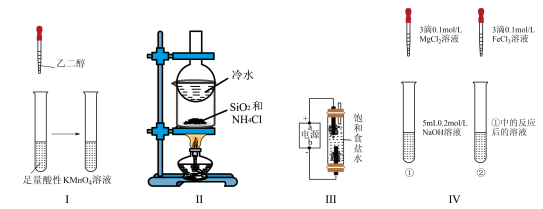

| A.I将乙二醇转化为乙二酸 |
| B.II分离SiO2和NH4Cl |
| C.III制备少量含NaClO的消毒液 |
| D.IV证明该温度下溶度积常数:Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
您最近一年使用:0次
2020-11-09更新
|
307次组卷
|
3卷引用:江西省南昌市第二中学2021届高三上学期第四次考试理综化学试题
2010·湖南·一模
名校
解题方法
3 . 已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13,则下列说法不正确 的是( )
| A.所得溶液中的c(H+)=1.0×10-13mol·L-1 |
| B.所得溶液中由水电离产生的c(OH-)=1.0×10-13 mol·L-1 |
| C.所加的烧碱溶液pH=13 |
| D.所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1 |
您最近一年使用:0次
2020-10-17更新
|
421次组卷
|
16卷引用:2015-2016学年江西省南昌二中高二上第三次考试化学试卷
2015-2016学年江西省南昌二中高二上第三次考试化学试卷【全国百强校】江西省南昌市第二中学2018-2019学年高二上学期第三次月考化学试题(已下线)2011届嘉禾一中高三第一次摸底考试化学卷2015届甘肃省高三第一次诊断考试理综化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷12015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年黑龙江省大兴安岭实验中学高二上学期期末化学试卷广东省中山市第一中学2017-2018学年高二上学期第三次统测化学试题【全国百强校】广西桂林市第十八中学2017-2018学年高二下学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——与pH相关的计算综合(提升练习)2020届高三化学化学二轮复习——常考题型:浓度积及浓度积常数【精编24题】海南省琼山中学2019-2020学年高二上学期期末考试化学试题(已下线)3.4.1 沉淀溶解平衡原理(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)广西玉林师院附中、玉林十一中等五校2020-2021学年高二上学期教学质量评价理综化学试题山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记
名校
4 . 亚硝酰氯(ClNO)是有机物合成中的重要试剂,红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度:
(1)实验室可用下图装置制备亚硝酰氯(ClNO);
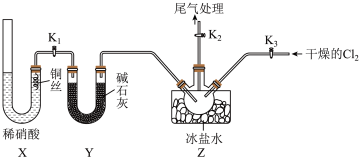
①X装置的优点为_________________________ 。
②检验装置气密性并装入药品,打开k2,然后再打开________ (填“k1”“k2”或“k3”),
通入一段时间气体,(其目的为________________________________________ ),然后进行其它操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为__________________ 。
(2)亚硝酰氯(ClNO)的纯度测定:取Z中所得液体m g溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12),则亚硝酰氯(ClNO)的质量分数为_________ (用代数式表示)。
(1)实验室可用下图装置制备亚硝酰氯(ClNO);

①X装置的优点为
②检验装置气密性并装入药品,打开k2,然后再打开
通入一段时间气体,(其目的为
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为
(2)亚硝酰氯(ClNO)的纯度测定:取Z中所得液体m g溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用c mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12),则亚硝酰氯(ClNO)的质量分数为
您最近一年使用:0次
2020-10-10更新
|
221次组卷
|
3卷引用:江西省南昌市第二中学2021届高三上学期第三次考试化学试题
名校
解题方法
5 . V2O5是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是V2O3,其中含铝、硅、铜、锰等氧化物及油脂等杂质,一种以该下脚料为原料提取V2O5的工艺流程如下:
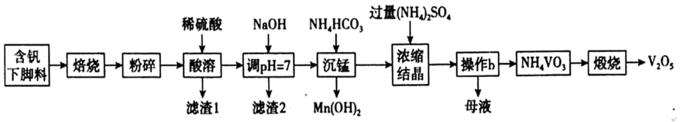
已知:i.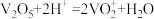 ;
;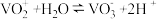 。
。
ii.常温时,有关氢氧化物的溶度积常数如下表:

回答下列问题:
(1)“焙烧”可以除去油脂,还有一个作用是_______________________________________ 。
(2)将焙烧冷却后的固体残留物进行“粉碎”,其目的是______________________________ 。
(3)“滤渣1”的主要成分是____________ (写化学式),“调pH=7”,析出沉淀后,滤液中c(Cu2+):c(Al3+)=____________ 。
(4)“沉锰”操作需微热,微热的目的是______________________________ ,该反应的离子方程式是________________________________________ 。
(5)“浓缩结晶”时,需要加入过量(NH4)2SO4,其原因是_______________ 。
(6)利用制得的V2O5可通过电解的方法制备金属钒,电解装置如图:石墨电极Y接直流电池___________ (填“正极”或“负极”),阴极反应式是_________________________ 。
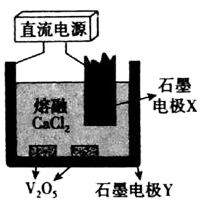

已知:i.
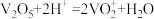 ;
;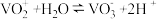 。
。ii.常温时,有关氢氧化物的溶度积常数如下表:

回答下列问题:
(1)“焙烧”可以除去油脂,还有一个作用是
(2)将焙烧冷却后的固体残留物进行“粉碎”,其目的是
(3)“滤渣1”的主要成分是
(4)“沉锰”操作需微热,微热的目的是
(5)“浓缩结晶”时,需要加入过量(NH4)2SO4,其原因是
(6)利用制得的V2O5可通过电解的方法制备金属钒,电解装置如图:石墨电极Y接直流电池

您最近一年使用:0次
2020-10-10更新
|
364次组卷
|
4卷引用:江西省南昌市第二中学2021届高三上学期第三次考试化学试题
江西省南昌市第二中学2021届高三上学期第三次考试化学试题(已下线)【南昌新东方】2. 南昌二中 左佳鑫百校联盟2021届高三高考9月份联考化学试题江西省靖安中学2021届高三上学期第四次月考化学试题
6 . 一定温度下,三种碳酸盐 (M:
(M: 、
、 、
、 )的沉淀溶解平衡曲线如图所示。下列说法错误的是
)的沉淀溶解平衡曲线如图所示。下列说法错误的是
 (M:
(M: 、
、 、
、 )的沉淀溶解平衡曲线如图所示。下列说法错误的是
)的沉淀溶解平衡曲线如图所示。下列说法错误的是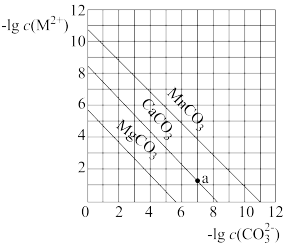
A.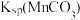 的数量级为 的数量级为 |
B.向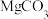 的悬浊液中加入少量水,充分振荡后 的悬浊液中加入少量水,充分振荡后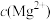 不变 不变 |
C.a点表示的溶液中,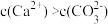 |
D.向浓度均为 的 的 、 、 、 、 的混合溶液中逐滴加入 的混合溶液中逐滴加入 溶液,最先生成 溶液,最先生成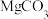 沉淀 沉淀 |
您最近一年使用:0次
2020-09-19更新
|
641次组卷
|
18卷引用:江西省南昌市第十中学2020-2021学年高二上学期期末考试化学试题
江西省南昌市第十中学2020-2021学年高二上学期期末考试化学试题福建省龙海市第二中学2019届高三下学期期初考试化学试题【市级联考】广东省广州市2019届高三上学期期末调研测试理科综合化学试题【全国百强校】四川省成都市成都外国语学校2018-2019学年高二下学期3月月考化学试题广东省广州市113中学2019-2020学年高三11月月考化学试题2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)3.4 难溶电解质的溶解平衡(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)河南省郑州市第四高级中学2021-2022学年高二下学期第一次调研考试化学试题江苏省常州市金坛区2021-2022学年高二下学期期中质量调研化学试题(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)天津市第八中学2021-2022学年高二上学期12月月考化学试题 北京市首都师范大学附属中学2023-2024学年高三上学期1月阶段化学练习北京市第四中学顺义分校2023-2024学年高三下学期3月开学考试化学试题
名校
7 . 室温下,已知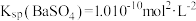 ,
,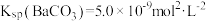 。下列说法中正确的是
。下列说法中正确的是
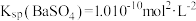 ,
,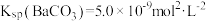 。下列说法中正确的是
。下列说法中正确的是A.在含有 固体的溶液中,一定有 固体的溶液中,一定有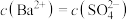 |
B.向只含有 的悬浊液中加入少量水,溶液中 的悬浊液中加入少量水,溶液中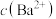 增大 增大 |
C.向只含有 的悬浊液中逐渐加入 的悬浊液中逐渐加入 固体至 固体至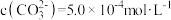 时, 时, 开始向 开始向 沉淀转化 沉淀转化 |
D.向 和 和 的混合溶液中加入 的混合溶液中加入 溶液,当生成 溶液,当生成 沉淀时, 沉淀时,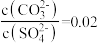 |
您最近一年使用:0次
2020-09-13更新
|
183次组卷
|
8卷引用:江西省南昌市第十中学2019-2020学年高二上学期期末考试化学试题
江西省南昌市第十中学2019-2020学年高二上学期期末考试化学试题(已下线)【南昌新东方】2019 南昌市三校(一中、十中、铁一中)高二上 期末江西省南昌市八一中学、洪都中学等七校2020-2021学年高二上学期期末联考化学试题湖北省黄冈市2017-2018学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节综合训练高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节综合训练(已下线)四川省棠湖中学2018-2019学年高二上学期期末模拟理综-化学试题江西省宜春市万载中学2021-2022学年高二上学期第三次月考化学试题
8 . 常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如下图所示(不考虑C2O42-的水解)。下列叙述正确的是
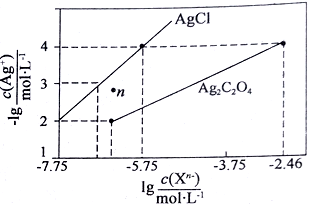

| A.Ksp(Ag2C2O4)的数量级等于10-7 |
| B.n点表示AgCl的不饱和溶液 |
| C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
| D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为109.04 |
您最近一年使用:0次
2020-05-27更新
|
509次组卷
|
9卷引用:【南昌新东方】2019 南昌二中 高二上 期末
9 . 某温度下,向50 mL饱和CuCl溶液中缓慢加入NaI固体并搅拌,溶液中c(I-)与c(Cu+)的变化曲线如图所示,已知:Ksp(CuI)=1.0×10-12,下列说法正确的是


| A.Ksp(CuCl)=1.0×10-9 |
| B.图示中的x为10-6 |
| C.向CuI饱和溶液中加入淀粉会出现蓝色 |
| D.曲线bc段内,c(Cl-):c(I-)=106 |
您最近一年使用:0次
2020-05-18更新
|
210次组卷
|
2卷引用:江西省南昌市第二中学2020届高三5月模拟理综化学试题
18-19高三上·江西南昌·阶段练习
解题方法
10 . 下列实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有漂白粉溶液的试管中加浓硫酸 | 产生黄绿色气体 | 浓硫酸具有氧化性 |
| B | 向SO2水溶液中滴入几滴BaCl2溶液,振荡 | 出现白色沉淀 | 此沉淀是BaSO4 |
| C | 使装有NO2气体的密闭容器减小体积 | 气体颜色先变深、而后变浅 | 气体颜色变浅原因是:2NO2⇋N2O4 |
| D | 先向2mL 0.1mol/L Na2S溶液中滴入几滴0.1mol/L ZnSO4溶液,再加入几滴0.1mol/L CuSO4溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



