已知CuS是一种不溶于非氧化性酸的沉淀。下列说法正确并能用勒 夏特列原理解释的是
夏特列原理解释的是
 夏特列原理解释的是
夏特列原理解释的是| A.工业合成SO3采用高压条件以增大平衡转化率 |
B.向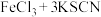  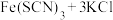 的平衡体系中加入少量KCl固体,溶液颜色变浅 的平衡体系中加入少量KCl固体,溶液颜色变浅 |
C.向氯水中加碳酸钠,可提高溶液中 的浓度 的浓度 |
| D.向饱和H2S溶液中加入少量硫酸铜溶液,溶液酸性增强 |
更新时间:2023-12-14 09:19:08
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
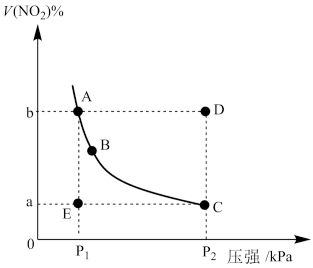
【推荐1】反应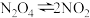 在温度一定时,平衡体系中NO2的体积分数
在温度一定时,平衡体系中NO2的体积分数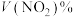 随压强的变化情况如图所示。下列说法正确的是
随压强的变化情况如图所示。下列说法正确的是
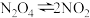 在温度一定时,平衡体系中NO2的体积分数
在温度一定时,平衡体系中NO2的体积分数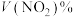 随压强的变化情况如图所示。下列说法正确的是
随压强的变化情况如图所示。下列说法正确的是
| A.A、C两点的正反应速率的关系A>C |
| B.A、B、C、D、E各状态,v(正)<v(逆)的是状态E |
| C.E→A所需时间为x,D→C所需时间为y,则x<y |
| D.根据C点对应的坐标值可以计算出该反应的平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验事实能用平衡移动原理解释的是
| A.工业上用SO2和O2制备SO3时,选择常压而不用高压 |
| B.使用铁触媒能加快合成氨的反应速率 |
C.平衡4CO(g)+2NO2(g) N2(g)+4CO2(g),加压气体颜色变深 N2(g)+4CO2(g),加压气体颜色变深 |
| D.将氯化铝溶液低温蒸干,最终得到氢氧化铝固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关合成氨工业的叙述,可用勒·夏特列原理来解释的是
| A.使用铁触媒,使N2和H2混合气体有利于合成氨 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.500℃左右比室温更有利于合成氨的反应 |
| D.合成氨时采用循环操作,可提高原料的利用率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是
A.对2HI(g) H2(g)+I2(g),平衡体系增大压强可使颜色变深;能用勒夏特列原理解释 H2(g)+I2(g),平衡体系增大压强可使颜色变深;能用勒夏特列原理解释 |
B.在密闭容中发生下列反应aA(g) cC(s)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时D的浓度为原平衡的1.8倍,平衡向正反应方向移动 cC(s)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时D的浓度为原平衡的1.8倍,平衡向正反应方向移动 |
C.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2HBr(g)∆H<0;平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b,则a<b 2HBr(g)∆H<0;平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b,则a<b |
D.对平衡CO2(g) CO2(aq) ∆H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是降温增压 CO2(aq) ∆H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是降温增压 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现进行下列实验:
(1)将
 溶液和
溶液和
 溶液等体积混合,得到悬浊液a;将悬浊液a过滤,得到滤液b和白色沉淀c。
溶液等体积混合,得到悬浊液a;将悬浊液a过滤,得到滤液b和白色沉淀c。
(2)向滤液b中滴加
 溶液,滤液出现浑浊。
溶液,滤液出现浑浊。
(3)向沉淀c中滴加
 溶液,沉淀变为黄色。
溶液,沉淀变为黄色。
下列关于上述实验的分析错误的是
(1)将

 溶液和
溶液和
 溶液等体积混合,得到悬浊液a;将悬浊液a过滤,得到滤液b和白色沉淀c。
溶液等体积混合,得到悬浊液a;将悬浊液a过滤,得到滤液b和白色沉淀c。(2)向滤液b中滴加

 溶液,滤液出现浑浊。
溶液,滤液出现浑浊。(3)向沉淀c中滴加

 溶液,沉淀变为黄色。
溶液,沉淀变为黄色。下列关于上述实验的分析错误的是
A.悬浊液a中存在沉淀溶解平衡: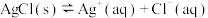 |
B.滤液b中含有 |
C.实验(3)表明 转化为 转化为 |
D.实验可以证明 的 的 比 比 的小 的小 |
您最近一年使用:0次
【推荐2】常温下,AgCl和AgI在水中的溶解平衡曲线如图所示,下列说法错误的是
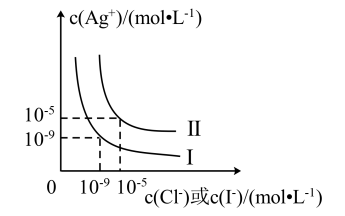

| A.曲线Ⅰ表示AgI的溶解平衡 |
| B.常温下,Ksp(AgCl)=1×10-10 |
C.常温下,饱和AgCl溶液与饱和AgI溶液两种溶液中 |
| D.常温下,向饱和AgCl溶液中加入更多的AgCl固体,则c(Ag+)不变 |
您最近一年使用:0次



