解题方法
1 . 七水合硫酸镁(MgSO4•7H2O)在印染、造纸等领域应用广泛。以化工废弃物盐泥(主要成分为MgCO3•CaCO3,含少量NaCl与含铁化合物)为原料可制取七水合硫酸镁,回答下列问题:
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为________ ;配制3.0mol•L-1H2SO4溶液时,用到的实验仪器除烧杯、玻璃棒、量筒外,还必须使用的仪器有________ (填标号)。
A. B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是________ 、________ ,继续加热煮沸的目的是________ 。
(3)要证明铁元素已除尽,实验操作及现象是:________ 。
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是________ ,将滤渣完全溶于3.0mol•L-1H2SO4溶液,经如下实验操作:加热蒸发、________ 、过滤、洗涤、干燥,得到七水合硫酸镁。
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为________ %,将产品加热至77℃,测得固体失重率为43.9%,该温度下固体的化学式为________ 。
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为
A.
 B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是
(3)要证明铁元素已除尽,实验操作及现象是:
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为
您最近一年使用:0次
解题方法
2 . 难溶电解质存在沉淀溶解平衡,已知: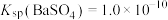 ,
,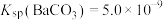 ,下列叙述中正确的是
,下列叙述中正确的是
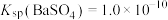 ,
,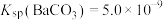 ,下列叙述中正确的是
,下列叙述中正确的是A.在含有 固体的悬浊液中加入少量 固体的悬浊液中加入少量 固体, 固体,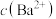 不变 不变 |
B. 悬浊液液中逐渐加入 悬浊液液中逐渐加入 溶液,一定不发生 溶液,一定不发生 |
C.将几滴 溶液滴入 溶液滴入 溶液,得到白色沉淀,再滴加 溶液,得到白色沉淀,再滴加 溶液,出现红褐色沉淀,证明 溶液,出现红褐色沉淀,证明 |
D.另取少量C中白色沉淀,滴入 浓溶液使其溶解,可能是 浓溶液使其溶解,可能是 导致沉淀溶解 导致沉淀溶解 |
您最近一年使用:0次
2022-07-07更新
|
435次组卷
|
3卷引用:四川省成都市2021-2022学年高二下学期摸底考试化学试题
四川省成都市2021-2022学年高二下学期摸底考试化学试题四川省成都经济技术开发区实验中学校2022-2023学年高二下学期5月月考化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
3 . 严谨的实验设计能有效规避实验风险,能重复实验并得到相同的结果。由粗盐制备试剂级的NaCl的相关实验步骤和装置如下:
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO 已经除净的实验方法是
已经除净的实验方法是___________ 。
(2)第II步加入Na2CO3可以除去的离子为___________ 。
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、___________ ;已知:Ksp(BaCO3)=5.0×10-9、Ksp(BaSO4)=1.1×10-10;如果省略第I步“倾析法分离”,所得氯化钠溶液的纯度将___________ (填“升高”、“降低”或“不受影响”)。
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。
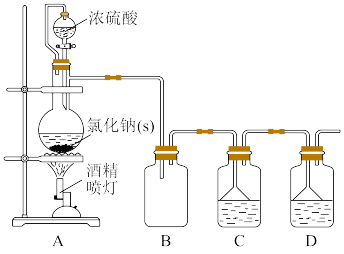
(4)装置A中发生的化学反应方程式为___________ ,控制该反应速率可采取的措施___________ (任答一点即可)。
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是___________ ,装置C的溶液中能观察到的实验现象是___________ 。装置D中盛放的试剂为___________ (填“NaOH溶液”、“NaHSO3溶液”或“浓H2SO4”)。
【粗盐的提纯】
第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。
第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3,过滤,再用3.0mol/L HCl调节pH至1~2。
第III步,加热浓缩至溶液刚刚出现微晶膜。
(1)第I步加入BaCl2时,证明SO
 已经除净的实验方法是
已经除净的实验方法是(2)第II步加入Na2CO3可以除去的离子为
(3)第III步加热浓缩时所用到的硅酸盐材质的仪器有酒精灯、
【试剂级的NaCl的制备】
第IV步,将第III步浓缩溶液转移至下图装置C中继续实验。

(4)装置A中发生的化学反应方程式为
(5)装置B中的广口瓶和装置C、D中的漏斗,其共同作用是
您最近一年使用:0次
2022-03-25更新
|
506次组卷
|
5卷引用:四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
名校
解题方法
4 . 用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是( )
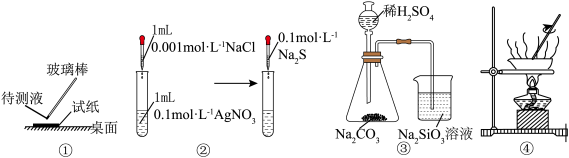

| A.①用pH试纸测某溶液的酸碱性 |
| B.实验室用图②所示装置若先出现白色沉淀后又变黑,则能比较Ksp(AgCl)﹥Ksp(Ag2S) |
| C.实验室用图③所示装置证明酸性:H2SO4>H2CO3>H2SiO3 |
| D.图④可由AlCl3饱和溶液制备AlCl3晶体 |
您最近一年使用:0次
2019-12-21更新
|
177次组卷
|
4卷引用:四川省广元市川师大万达中学2019-2020学年高二上学期11月月考化学试题
解题方法
5 . 以某含镍废料(主要成分为NiO,还含有少量FeO、Fe2O3、CoO、SiO2)为原料制备NixOy和碳酸钴的工艺流程如下:
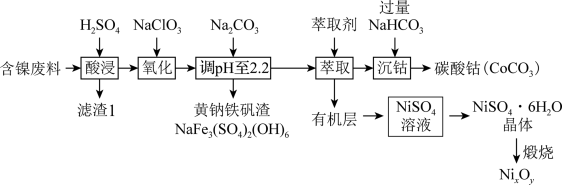
(1)“酸溶”时需将含镍废料粉碎,目的是_________________________________ ;“滤渣Ⅰ”主要成分为____________________ (填化学式)。
(2)“氧化”中添加NaClO3的作用是_______________________ ,为证明添加NaClO3已足量,可用_______________ (写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,其离子方程式为__________________ 。
(4)“沉钴”过程的离子方程式________________________ 。若“沉钴”开始时c(Co2+)=0.10 mol/L,则控制pH≤_____________ 时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15,lg2=0.3)
(5)从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,______________ ,过滤,洗涤,干燥。“煅烧”时剩余固体质量与温度变化曲线如图,该曲线中B段所表示氧化物的化学式为__________________ 。
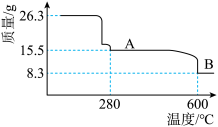

(1)“酸溶”时需将含镍废料粉碎,目的是
(2)“氧化”中添加NaClO3的作用是
(3)“调pH”过程中生成黄钠铁钒沉淀,其离子方程式为
(4)“沉钴”过程的离子方程式
(5)从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,

您最近一年使用:0次
2019-12-28更新
|
1038次组卷
|
4卷引用:四川省成都市2020届高三第一次诊断性检测理综化学试题
四川省成都市2020届高三第一次诊断性检测理综化学试题2019年四川省成都市高三第一次诊断考试化学试题2020届高三《新题速递·化学》1月第02期(考点11-13)(已下线)03 无机化工流程题(3) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
6 . 某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
【查阅资料】25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
【实验探究】向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
A、白色沉淀转化为红褐色沉淀 B、白色沉淀不发生改变
C、红褐色沉淀转化为白色沉淀 D、白色沉淀溶解,得无色溶液
(2)测得试管Ⅰ中所得混合液pH=6,则溶液中c(Fe3+)=______________ 。
(3)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1: 结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________ 。
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是__________ (填 “1”或“2”)。
【查阅资料】25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
【实验探究】向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
| 试管编号 | 加入试剂 | 实验现象 |
| Ⅰ | 2滴0.1mol/LFeCl3溶液 | ① |
| Ⅱ | 4mL2mol/LNH4Cl溶液 | ② |
C、红褐色沉淀转化为白色沉淀 D、白色沉淀溶解,得无色溶液
(2)测得试管Ⅰ中所得混合液pH=6,则溶液中c(Fe3+)=
(3)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:
 结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。猜想2:
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是
您最近一年使用:0次
2018-06-25更新
|
520次组卷
|
9卷引用:【全国百强校】四川省绵阳市南山中学2017-2018学年高二下学期期末模拟考试(6月)化学试题
【全国百强校】四川省绵阳市南山中学2017-2018学年高二下学期期末模拟考试(6月)化学试题【全国百强校】四川省绵阳市南山中学2017-2018学年高二下学期期末模拟考试(6月)化学试题四川省棠湖中学2019-2020学年高二下学期期中考试化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第三单元 水溶液中的离子平衡单元测试A卷安徽省太和第一中学2020-2021学年高二上学期期中考试化学(普通班)试题安徽省怀宁中学2020-2021学年高二上学期第二次质量检测(普通班)化学试题河南省中原名校2021-2022学年高二上学期期末联考化学试题作业(二十一) 沉淀溶解平衡的应用河南省南阳市第八中学校2022-2023学年高二上学期线上期末考试化学试题
名校
7 . 下列实验设计的步骤及现象均正确的是
| 选项 | 实验目的 | 实验步骤及现象 |
| A | 证明氯水有酸性 | 试样 溶液变红色,且长时间不变 溶液变红色,且长时间不变 |
| B | 检验某红棕色气体是否为溴蒸气 | 试样 观察溶液是否变蓝 观察溶液是否变蓝 |
| C | 证明酸性条件下H2O2氧化性比 I2强 | NaI   溶液变蓝色 溶液变蓝色 |
| D | 比较: Ksp(AgCl)>Ksp(AgI) | AgNO3 溶液 产生白色沉淀 产生白色沉淀 有黄色沉淀生成 有黄色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol·L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2 =3V1,下列说法正确的是
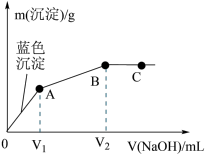

| A.原溶液中MgCl2和CuCl2的物质的量浓度相等 |
| B.该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 |
| C.水的电离程度:A>B>C |
| D.若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
您最近一年使用:0次
2018-01-01更新
|
494次组卷
|
8卷引用:四川省遂宁市2019-2020学年高二下学期期末考试化学试题
名校
解题方法
9 . 金属镁性质活泼,能与许多物质反应。
I.某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2燃烧,可能产物为MgO、N2和Mg3N2。通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO2气体能被NaOH吸收,Mg3N2极易与水反应。
(1)实验中,装置依次连按的顺序为A_____ (填字母序号);装置B的作用是______ ;
(2)用来检验N2的实验装置为____ (填字母序号);
(3)设计实验证明:产物中存在Mg3N2、____ ;
Ⅱ.工业上以菱镁矿为原料(主要成分为MgCO3,还有SiO2、FeCO3等杂质)制备纳米氧化镁。
(4)根据反应流程要求,先除去FeCO3,采用先酸浸再氧化的方法,其中加入H2O2时,发生反应的离子方程式为_____ 。
(5)已知:在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,流程后期,当除杂完成后,再加入CO(NH2)2开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或离子反应方程式表示)_______ ;_______ 。
I.某校课外活动小组根据镁能在二氧化碳中燃烧,推测Mg也能在NO2燃烧,可能产物为MgO、N2和Mg3N2。通过如图所示实验装置来验证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO2气体能被NaOH吸收,Mg3N2极易与水反应。
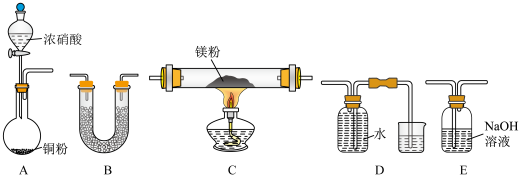
(1)实验中,装置依次连按的顺序为A
(2)用来检验N2的实验装置为
(3)设计实验证明:产物中存在Mg3N2、
Ⅱ.工业上以菱镁矿为原料(主要成分为MgCO3,还有SiO2、FeCO3等杂质)制备纳米氧化镁。
(4)根据反应流程要求,先除去FeCO3,采用先酸浸再氧化的方法,其中加入H2O2时,发生反应的离子方程式为
(5)已知:在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,流程后期,当除杂完成后,再加入CO(NH2)2开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或离子反应方程式表示)
您最近一年使用:0次
2017-05-05更新
|
302次组卷
|
3卷引用:【全国百强校】四川省棠湖中学2019届高三下学期4月月考理科综合化学试题
名校
10 . 下列说法中正确的是
| A.钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO3而排出 |
B.珊瑚虫从海水中获取Ca2+和HCO ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 |
C.泡沫灭火器原理3CO +2Al3++3H2O=2Al(OH)3 +3CO2 +2Al3++3H2O=2Al(OH)3 +3CO2 |
| D.使用含氟牙膏预防龋齿利用了盐类水解的原理 |
您最近一年使用:0次



