1 . 25℃,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,先出现黄色沉淀,最终生成黑色沉淀。已知有关物质的颜色和溶度积如下:
下列叙述不正确的是
| 物质 | AgCl | AgI | Ag2S |
| 颜色 | 白 | 黄 | 黑 |
| Ksp(25℃) | 1.8×10-10 | 1.5×10-16 | 1.8×10-50 |
| A.溶度积小的沉淀可以转化为溶度积更小的沉淀 |
| B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生 |
| C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同 |
| D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 |
您最近一年使用:0次
2021-11-22更新
|
489次组卷
|
11卷引用:辽宁省葫芦岛市第八高级中学2020届高三上学期期中考试化学(实验班)试题
辽宁省葫芦岛市第八高级中学2020届高三上学期期中考试化学(实验班)试题(已下线)2010-2011学年宁夏银川一中高二下学期期中考试化学试卷(已下线)2012届高考化学一轮复习《溶液中的离子反应》专题综合测试(苏教版)(已下线)2014高考化学名师选择题专练 电解质溶液练习卷河北省安平中学2020-2021学年高二上学期第三次月考化学试题湖北省石首市第一中学2020-2021学年高二上学期12月月考化学试题第22届(2008年)全国高中学生化学竞赛(河南省赛区)预赛试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期期中考试化学(理)试题黑龙江省哈尔滨市第六中学2022-2023学年高三8月月考化学试题第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用【精品卷】3.4.2 沉淀溶解平衡的应用-人教版2023-2024学年选择性必修1
2 . 下列实验操作中,根据实验现象得出的结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 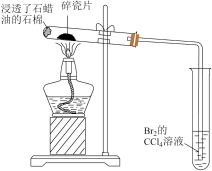 | Br2的CCl4溶液褪色 | 石蜡油分解产生乙烯气体 |
| B | 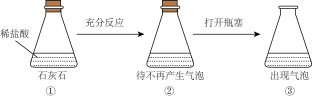 | ③中出现气泡 | 可以用平衡移动原理解释 |
| C |  | ①中出现白色沉淀 ②中出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
| D | 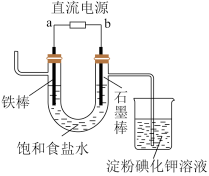 | 淀粉碘化钾溶液变蓝 | b为直流电源负极 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-14更新
|
159次组卷
|
3卷引用:辽宁省葫芦岛协作校2020届高三4月质量检测(一模) 化学 试题
名校
3 . 下列反应中,第一步反应生成的沉淀经第二步反应后质量增加的是
| A.将少量CO2(g)通入饱和Ca(OH)2溶液中,再通入过量Cl2 |
| B.将少量AgNO3溶液滴加到NaCl溶液中,再滴加Na2S溶液 |
| C.将少量FeCl2溶液加入到NaOH溶液中,再滴加H2O2溶液 |
| D.将少量Ba(OH)2溶液滴加到Al2(SO4)3溶液中,再加入过量NaOH溶液 |
您最近一年使用:0次
2020-05-10更新
|
544次组卷
|
5卷引用:辽宁省实验中学东戴河分校2020届高三10月月考化学试题
4 . 已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确 的是( )

注:加热为微热,忽略体积变化。

注:加热为微热,忽略体积变化。
| A.实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3 |
| B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响 |
C.实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O  [FeCl4(H2O)2]- [FeCl4(H2O)2]- |
| D.实验④,可证明升高温度,Fe3+水解平衡正向移动 |
您最近一年使用:0次
解题方法
5 . 下列离子方程式中,不能正确表达反应颜色变化的是
| A.向氯水中通入SO2气体,溶液浅黄绿色消失:Cl2 + SO2 + 2 H2O = 4H+ + 2Cl- + SO42- |
| B.向AgNO3溶液中加入一定量HCl溶液,后加入Na2S溶液,白色沉淀变黑色:2AgCl + S2- = Ag2S + 2Cl- |
| C.向氢氧化铁胶体中加入HI酸溶液,首先出现红褐色沉淀,后沉淀消失,溶液变为黄色:2Fe(OH)3 + 6H+ + 2I- = 2Fe2+ + I2 + 6H2O |
D.向CrO42-中加入H2SO4溶液,颜色由黄色变为橙色:2CrO42-+2H+ Cr2O72-+H2O Cr2O72-+H2O |
您最近一年使用:0次
6 . 根据下列图示所得出的结论正确的是( )


| A.图甲表示pH相同的NaOH溶液与氨水稀释过程pH的变化,曲线a对应氨水 |
| B.图乙表示某放热反应分别在有、无催化剂的情况下,反应过程中的能量变化 |
C.图丙表示CO(g)+Cl2(g) COCl2(g)的反应速率随时间的变化,在t1时改变的条件是加入催化剂 COCl2(g)的反应速率随时间的变化,在t1时改变的条件是加入催化剂 |
| D.图丁表示用0.0100mol·L-1的硝酸银标准溶液滴定浓度均为0.1000mol·L-1 Cl-、Br-及I-的混合溶液时,先沉淀的是Cl- |
您最近一年使用:0次
2019-05-24更新
|
342次组卷
|
2卷引用:辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题
名校
7 . 下列实验方案能达到实验目的的是
实验目的 | 实验方案 | |
| A | 证明Mg(OH)2 沉淀可以转化为Fe(OH)3 | 向2mL1mol/LNaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/LFeCl3 |
| B | 比较氯和碳的非金属性强弱 | 将盐酸滴入碳酸氢钠溶液中 |
| C | 配制100mL1.0mol/LCuSO4溶液 | 将25gCuSO4·5H2O溶于100mL蒸馏水中 |
| D | 验证氧化性:Fe3+>I2 | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,观察下层液体是否变成紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-01-18更新
|
296次组卷
|
8卷引用:辽宁省葫芦岛市第六中学2019届高三上学期开学考试(8月)化学试题



