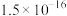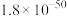名校
解题方法
1 . 下列有关实验操作、现象和结论都正确的是
| 实验操作和现象 | 结论 | |
| A | 将二氧化碳通入氯化钡溶液中,产生沉淀 | 盐酸的酸性强于碳酸 |
| B | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 室温时,将等体积、等物质的量浓度的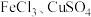 溶液分别加入等体积的 溶液分别加入等体积的 的 的 溶液中 溶液中 | 探究 的催化效果的优劣 的催化效果的优劣 |
| D | 向相同物质的量浓度的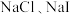 混合溶液中滴加少量稀 混合溶液中滴加少量稀 溶液,先有黄色沉淀生成 溶液,先有黄色沉淀生成 | 相同温度时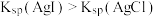 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 25℃时有关物质的颜色和溶度积( )如下表:
)如下表:
下列叙述不正确的是
 )如下表:
)如下表:物质 | AgCl | AgBr | AgI |
|
颜色 | 白 | 淡黄 | 黄 | 黑 |
|
|
|
|
|
A.向AgCl的白色悬浊液中加入0.1 KI溶液,有黄色沉淀产生 KI溶液,有黄色沉淀产生 |
B.25℃时,AgCl、AgBr、AgI、 饱和水溶液中 饱和水溶液中 的浓度相同 的浓度相同 |
C.25℃,AgCl固体在等物质的量浓度NaCl、 溶液中的溶度积相同 溶液中的溶度积相同 |
D.在5mL 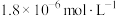 NaCl溶液中,加入1滴(20滴约为1mL) NaCl溶液中,加入1滴(20滴约为1mL)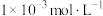  液,不能产生白色沉淀 液,不能产生白色沉淀 |
您最近一年使用:0次
2023-06-01更新
|
167次组卷
|
2卷引用:云南省昆明市第一中学2022-2023学年高二下学期期中考试化学试题
3 . 已知: ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线如图所示。已知:
溶液的滴定曲线如图所示。已知: 。下列说法正确的是
。下列说法正确的是

 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线如图所示。已知:
溶液的滴定曲线如图所示。已知: 。下列说法正确的是
。下列说法正确的是
A. 、 、 、 、 三点的 三点的 从大到小的顺序为 从大到小的顺序为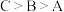 |
B.在 点的溶液中存在 点的溶液中存在 |
C.常温下,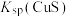 为 为 |
D.其他条件相同,若将 溶液换为同浓度、同体积的 溶液换为同浓度、同体积的 溶液,B点会平行向右移动 溶液,B点会平行向右移动 |
您最近一年使用:0次
2022-12-23更新
|
491次组卷
|
8卷引用:云南省曲靖市第一中学2023-2024学年高二上学期11月期中考试化学试题
云南省曲靖市第一中学2023-2024学年高二上学期11月期中考试化学试题河南省洛阳市2022-2023学年高三上学期期末测试化学试题河南省洛阳市2022-2023学年高三上学期普高联考测评(三)化学试题新疆昌吉回族自治州奇台县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题安徽省淮北市第一中学2022-2023学年高二下学期第二次月考化学试题(已下线)选择题11-16
4 . 已知 25℃时,几种难溶电解质的溶度积常数 Ksp 如表所示:
下列叙述正确的是
| 难容电解质 | AgCl | AgBr | AgI | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10 -17 | 1.4×10-5 | 1.12×10-12 |
| A.由溶度积常数可以判断相应物质的溶解性大小 |
| B.将等体积的 4×10-3 mol/L的 AgNO3溶液和 4×10-3 mol/L K2CrO4溶液混合,有 Ag2CrO4沉淀产生 |
| C.向 AgCl 的悬浊液中滴加饱和 NaBr 溶液不能得到浅黄色 AgBr |
| D.将0.02mol/L的AgNO3 溶液滴入浓度均为0.02 mol/L的K2CrO4和NaCl的混合溶液中,Ag2CrO4沉淀先析出 |
您最近一年使用:0次
2021-05-11更新
|
185次组卷
|
2卷引用:云南省玉溪市一中2020-2021学年高二下学期期中考试化学试题
5 . 以菱镁矿(主要成分为MgCO3,含少量SiO2,Fe2O3和A12O3)为原料制备高纯镁砂的工艺流程如下:
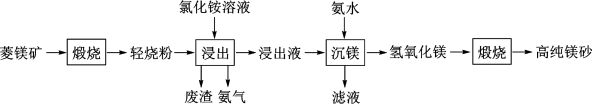
A.浸出镁的反应为 |
| B.浸出和沉镁的操作均应在较高温度下进行 |
| C.流程中可循环使用的物质有NH3、NH4Cl |
| D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物Ksp的不同 |
您最近一年使用:0次
2020-07-11更新
|
10499次组卷
|
75卷引用:云南省大理州实验中学2021-2022学年高二上学期化学期中考试题
云南省大理州实验中学2021-2022学年高二上学期化学期中考试题河南省南阳市2021届高三期中质量评估化学试题广东省汕头市金山中学2021届高三上学期期中考试化学试题重庆市第七中学2021届高三上学期期中化学试题河南省南阳市2021届高三上期期中考试化学试题(已下线)【苏州新东方】2021.04江苏省苏州市十中三中期中联考.江苏省淮安市高中校协作体2021-2022学年高三上学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高三上学期期中考试化学试题福建省三明第一中学2022-2023学年高三上学期期中考试化学试题2020年山东省高考化学试卷(新高考)(已下线)专题15 工艺流程题-2020年高考真题和模拟题化学分项汇编(已下线)第七单元 水溶液中的离子平衡测试题-2021年高考化学一轮复习名师精讲练黑龙江省大庆实验中学2021届高三8月开学考试化学试题广东省仲元中学、中山一中等七校联合体2021届高三上学期第一次联考化学试题(已下线)小题必刷16 金属元素为载体的化工流程选择题——2021年高考化学一轮复习小题必刷(通用版)山东省枣庄市第三中学2021届高三上学期9月阶段性检测化学试题(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)福建省福州市第四中学2021届高三10月月考化学试题山东省临沂市莒南第二中学2021届高三10月月考化学试题广东省珠海市第二中学2021届高三10月月考化学试题广东省云浮市郁南县蔡朝焜纪念中学2021届高三10月月考化学试题吉林松原市油田第十一中学2021届高三第二次阶段考试化学试题湖南省邵东县第一中学2021届高三上学期第三次月考化学试题湖北省随州市第一中学2021届高三11月月考化学试题(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)热点5 常见元素及其化合物的性质与应用-2021年高考化学专练【热点·重点·难点】(已下线)热点5 常见元素及其化合物的性质与相互转化-2021年高考化学专练【热点·重点·难点】(新高考)(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)考向07 铁及其重要化合物-备战2022年高考化学一轮复习考点微专题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)北京市十一学校2022 届高三上学期开学考试(暑期学习检测)化学试题安徽省合肥市第九中学2022届高三第一次阶段测验化学试卷(已下线)专题12 工艺流程选择题-备战2022年高考化学真题及地市好题专项集训【山东专用】山东省聊城市高唐县第一中学2021-2022学年高三上学期开学考试化学试题(已下线)第3周 周测卷-备战2022年高考化学周测与晚练(新高考专用)江西省宜春市丰城市第九中学2021-2022学年高三上学期第三次月考化学试题河南省温县第一高级中学2021-2022学年高三上学期10月月考化学试题辽宁省沈阳市重点高中联合体2021-2022学年高三12月考试化学试题河北省石家庄市新华中学2020-2021学年高三上学期10月月考化学试题(已下线)第十单元 化学实验基础(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)河南省信阳市罗山县2021-2022学年高三上学期高中毕业班第二次调研考试化学试题(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)河南省驻马店市2021-2022学年高二上学期期末考试化学试题福建省龙岩第一中学2021-2022学年高三上学期第三次月考化学试题陕西省西北农林科技大学附属中学2021-2022学年高二上学期期末考试化学试题(已下线)押新高考卷03题 元素化合物的性质-备战2022年高考化学临考题号押题(新高考通版)山西省长治市沁源县第一中学等名校2021-2022学年高二下学期5月联考化学试题(已下线)2020年山东卷化学高考真题变式题1-10(已下线)考点50 物质的分离、提纯和检验-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第08练 金属材料-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第21练 自然资源的开发利用-2023年高考化学一轮复习小题多维练(全国通用)重庆市第七中学校2021-2022学年高二上学期第二次月考化学试题(已下线)第08讲 金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)第三章 综合拔高练(已下线)专题讲座(八) 无机化工流程题的解题策略(练)-2023年高考化学一轮复习讲练测(全国通用)湖南省常德市汉寿县第一中学2022-2023学年高三上学期第一次月考化学试题山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题09 常见金属元素的性质及应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第三章 金属及其化合物 第15讲 金属材料 金属冶炼进阶训练5(已下线)题型26 碱土金属元素及其化合物北京市一零一中学2022-2023学年高三下学期3月统练二化学试题(已下线)专题10 物质的反应及转化(已下线)第5讲 铝、镁及其重要化合物安徽六校教育研究会2024届高三上学期入学素质测试化学试题江苏省苏南八校2023-2024学年高二上学期12月联考化学(创新班)试卷福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题湖南省长沙市一中2024届高三高考适应性演练(二)化学试题
6 . 某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是
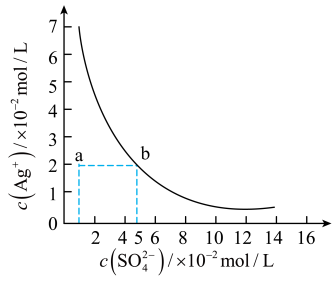

| A.含有大量SO42-的溶液中肯定不存在Ag+ |
| B.Ag2SO4的溶度积常数(Ksp)为1×10-3 |
| C.0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀 |
| D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
您最近一年使用:0次
2018-12-05更新
|
936次组卷
|
17卷引用:云南省通海县一中2020-2021学年高二下学期期中考试化学试题
云南省通海县一中2020-2021学年高二下学期期中考试化学试题【全国百强校】河北省石家庄市第一中学2018-2019学年高二上学期期中考试化学试题云南省文山马关实验高级中学2019-2020学年高二期末考试化学试题安徽省肥东县高级中学2020-2021学年高二上学期期中考试化学试题(已下线)2010年广东省汕头市潮阳一中理综化学考前押题卷2014-2015辽宁省沈阳二中高二上学期12月月考化学试卷2016-2017学年黑龙江省哈尔滨市第六中学高二3月月考化学试卷辽宁省辽阳2017-2018学年高二化学上学期期末考试题河南省安阳县第一高级中学2017-2018学年高二上学期第三次月考化学试卷广东省惠来县葵潭中学2019-2020学年高二上学期第二次月考化学试题安徽省合肥市六校2019-2020学年高二上学期期末考试化学试题(已下线)山东省邹城市2018-2019学年高二上学期12月月考化学试卷(已下线)第03章 水溶液中的离子反应与平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)吉林省榆树市实验高级中学2020-2021学年高二下学期第二次月考化学试题吉林省大安市第一中学校2021-2022学年高二上学期第三次月考化学试题(已下线)题型27 沉淀溶解平衡常数及其应用图象作业(二十一) 沉淀溶解平衡与溶度积
14-15高二上·辽宁沈阳·期末
7 . 下列关于化学平衡常数(K),电离平衡常数(Ka或Kb),水解平衡常数(Kh),沉淀溶解平衡常数(Ksp),水的离子积常数(Kw)的叙述中错误的是( )
| A.K、Ka或Kb、Kh、Ksp、Kw都与温度有关,温度越高,常数值越大 |
| B.比较Ksp与离子积Qc的相对大小,可判断难溶解电解质在给定条件下沉淀能否生成或溶解 |
| C.K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完全了 |
| D.弱酸HA的Ka与NaA的Kh、水的离子积常数Kw三者间的关系可表示为:Kw=Ka·Kh |
您最近一年使用:0次
2017-12-25更新
|
326次组卷
|
5卷引用:云南省玉溪市玉溪一中2017-2018学年高二上学期第二次月考化学试题
云南省玉溪市玉溪一中2017-2018学年高二上学期第二次月考化学试题(已下线)2013-2014学年辽宁省沈阳市高二上教学质量监测化学试卷(已下线)2014届辽宁省沈阳市高二上教学质量监测化学试卷 江西省南昌市新建县第一中学2019-2020学年高二上学期期末考试化学试题安徽省安庆市怀宁县第二中学2021届高三上学期第一次月考化学试题