名校
解题方法
1 . 2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。______ 极,发生______ (填“氧化”或“还原”)反应。
②Cu棒,上发生的电极反应是______ 。
③溶液中H+向______ (填“Zn”或“Cu”)电极定向移动。
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是______ (填“Zn”或“Cu”),正极的电极反应是______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=______ mol。
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。
该原电池电解质是KOH溶液,写出正极的电极反应______ 。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。

②Cu棒,上发生的电极反应是
③溶液中H+向
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH。
该原电池电解质是KOH溶液,写出正极的电极反应
您最近一年使用:0次
2024-01-11更新
|
505次组卷
|
2卷引用:陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
2 . 盐酸羟胺(NH2OH·HCl)用途广泛,可利用如图装置来制备。以盐酸为离子导体,向两电极分别通入NO和H2.下列说法正确的是
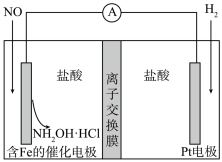
| A.Pt电极为原电池的正极 |
| B.Cl-通过离子交换膜到左极室 |
| C.一段时间后,含Fe的催化电极所在极室的pH增大 |
| D.每生成1mol盐酸羟胺电路中转移4mole- |
您最近一年使用:0次
2024-01-04更新
|
204次组卷
|
6卷引用:陕西省西安市2023-2024学年高二上学期期末化学测试卷B
名校
解题方法
3 . 利用CH4燃料电池作电源电解法制备Ca(H2PO4)2,装置如图所示。下列说法不正确的是

| A.a极反应:CH4-8e-+4O2- = CO2+2H2O |
| B.A膜为阳离子交换膜,B膜和C膜为阴离子交换膜 |
| C.该装置工作时还可得到产物NaOH、H2、Cl2 |
| D.a极通入2.24 L(标准状况)甲烷,阳极室Ca2+减少0.4mol |
您最近一年使用:0次
解题方法
4 . 将铜片和银片用导线连接插入硝酸银溶液中,当线路中有0.2mol的电子发生转移时,负极质量的变化是
| A.增加6.4g | B.增加2.16g | C.减轻6.4g | D.减轻2.16g |
您最近一年使用:0次
名校
解题方法
5 . 含磷有机物应用广泛。电解法可实现由白磷直接制备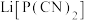 ,过程如图所示。下列说法正确的是
,过程如图所示。下列说法正确的是
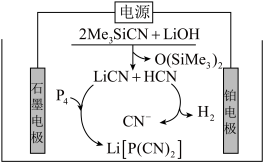
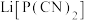 ,过程如图所示。下列说法正确的是
,过程如图所示。下列说法正确的是
A.生成1mol 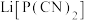 ,理论上外电路需要转移2mol电子 ,理论上外电路需要转移2mol电子 |
B.阳极上的电极反应为: |
C.在电解过程中 向铂电极移动 向铂电极移动 |
D.电解产生的 中的氢元素来自于LiOH 中的氢元素来自于LiOH |
您最近一年使用:0次
名校
解题方法
6 . 原电池和电解池在日常生活中有着广泛的应用。根据所学知识完成下列题目。
I.电化学装置如图所示
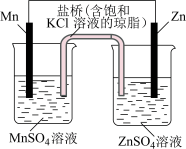
(1)已知金属活泼性:Mn>Zn。若装置中负极金属的消耗速率为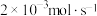 ,则盐桥中
,则盐桥中 流向
流向___________ (填“ ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为___________  。
。
Ⅱ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为: ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。

(2)装置甲中A电极为___________ 极,B电极的电极反应式为:___________ 。
(3)装置乙中D电极产生的气体是_______ (写化学式),体积为_________ mL(标准状况)。
(4)其他条件不变时,若将装置丙中的NaCl溶液改换成 和
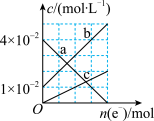
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中曲线b代表的离子为
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中曲线b代表的离子为___________ 。
I.电化学装置如图所示

(1)已知金属活泼性:Mn>Zn。若装置中负极金属的消耗速率为
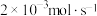 ,则盐桥中
,则盐桥中 流向
流向 ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为 。
。Ⅱ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为:
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
(2)装置甲中A电极为
(3)装置乙中D电极产生的气体是
(4)其他条件不变时,若将装置丙中的NaCl溶液改换成
 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中曲线b代表的离子为
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中曲线b代表的离子为
您最近一年使用:0次
7 . 电解原理在化学工业中有广泛应用。
(1)用固态碳燃料电池电解饱和食盐水(M极室为食盐水,N极室为稀NaOH溶液)的装置如下图所示。
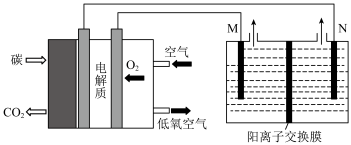
①电极M是___________ 极,N极区的产物为:___________ (用化学式表示);
②已知电解前M极区溶液的浓度为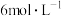 ,体积为200mL。当消耗标准状况下1.12L
,体积为200mL。当消耗标准状况下1.12L 时,M极区溶液的浓度变为
时,M极区溶液的浓度变为___________  。(电解前后溶液体积变化忽略不计)。
。(电解前后溶液体积变化忽略不计)。
(2)电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题:
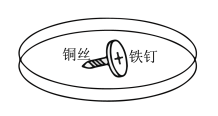
①下图为探究金属Fe是否腐蚀的示意图,在培养皿中加入一定量的琼脂与饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ (填“左”或“右”端),结合化学用语解释变红的原因:___________ 。
②支撑海港码头基础的钢管桩常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。该保护方法叫作___________ (填“牺牲阳极法”或“外加电流法”)。下列有关表述正确的是___________ (填字母)。
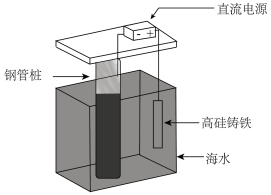
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(1)用固态碳燃料电池电解饱和食盐水(M极室为食盐水,N极室为稀NaOH溶液)的装置如下图所示。

①电极M是
②已知电解前M极区溶液的浓度为
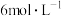 ,体积为200mL。当消耗标准状况下1.12L
,体积为200mL。当消耗标准状况下1.12L 时,M极区溶液的浓度变为
时,M极区溶液的浓度变为 。(电解前后溶液体积变化忽略不计)。
。(电解前后溶液体积变化忽略不计)。(2)电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题:
①下图为探究金属Fe是否腐蚀的示意图,在培养皿中加入一定量的琼脂与饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为

②支撑海港码头基础的钢管桩常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。该保护方法叫作

a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
您最近一年使用:0次
名校
解题方法
8 . 某有色金属工业的高盐废水中主要含有H+、Cu2+、Zn2+、 、F-和Cl-,利用如图电解装置可回收ZnSO4、CuSO4并尽可能除去F-和Cl-,其中双极膜(BP)中间层的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移,M膜、N膜为相同的一价离子交换膜。下列说法错误的是
、F-和Cl-,利用如图电解装置可回收ZnSO4、CuSO4并尽可能除去F-和Cl-,其中双极膜(BP)中间层的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移,M膜、N膜为相同的一价离子交换膜。下列说法错误的是

 、F-和Cl-,利用如图电解装置可回收ZnSO4、CuSO4并尽可能除去F-和Cl-,其中双极膜(BP)中间层的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移,M膜、N膜为相同的一价离子交换膜。下列说法错误的是
、F-和Cl-,利用如图电解装置可回收ZnSO4、CuSO4并尽可能除去F-和Cl-,其中双极膜(BP)中间层的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移,M膜、N膜为相同的一价离子交换膜。下列说法错误的是
A.BP膜中 均向左侧溶液移动,M膜为一价阳离子交换膜 均向左侧溶液移动,M膜为一价阳离子交换膜 |
| B.当阴极产生22.4L气体(标准状况)时,M膜和N膜各有2mol离子通过 |
| C.溶液a的主要溶质为ZnSO4和CuSO4 |
| D.电解过程中,高盐废水pH不宜过高 |
您最近一年使用:0次
名校
解题方法
9 . 氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正确 的是
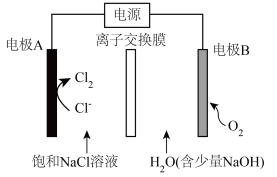

| A.电极A接电源正极,发生氧化反应 |
| B.用该装置制得的产品和传统氯碱工业的产品完全一样 |
| C.当生成1mol氯气时,电极B消耗11.2L(标况下)氧气 |
| D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗 |
您最近一年使用:0次
名校
解题方法
10 . 铅蓄电池是常见的二次电池,已知充电时电池总反应为 ,其内部简易结构如图所示。下列说法正确的是
,其内部简易结构如图所示。下列说法正确的是
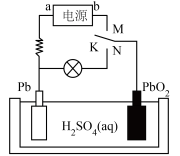
 ,其内部简易结构如图所示。下列说法正确的是
,其内部简易结构如图所示。下列说法正确的是
| A.a是电源正极,b是电源负极 |
B.K连接M时,两个电极都有 生成 生成 |
C.放电时,每转移0.5mol  ,消耗0.5 mol ,消耗0.5 mol  |
D.放电时, 电极的电极反应式为 电极的电极反应式为 |
您最近一年使用:0次



