名校
1 . 我国向国际社会承诺2030年前“碳达峰”。CO2的转化、回收及综合利用受到广泛关注,回答下列问题:
(1)用CO2和H2制取甲醇,反应的能量变化如图所示。

根据上图计算CO2(g)+3H2(g)=CH3OH(l)+H2O(l) ΔH=___________ 。
(2)萨巴帝尔(Sabatier)反应可以将二氧化碳转化为甲烷和水,配合水 电解可以实现氧气的再生。该方法可同时解决二氧化碳的清除问题,因此成为一种非常重要的载人航天器中氧气再生方法。
电解可以实现氧气的再生。该方法可同时解决二氧化碳的清除问题,因此成为一种非常重要的载人航天器中氧气再生方法。
①萨巴帝尔(Sabatier)反应是放热反应,控制反应器内的温度非常重要,反应温度过低则会造成___________ 。
②萨巴帝尔(Sabatier)反应在载人航天器实现回收CO2再生O2,其过程如图所示,这种方法再生O2的最大缺点是需要不断补充_______ (填化学式)。

(3)铅蓄电池作为电源可将CO2转化为乙烯(C2H4),其原理如图所示,所用电极材料均为惰性电极。已知铅蓄电池总反应式为: PbO2+Pb+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O

①铅蓄电池充电时Pb电极应与外加电源的___ 极相连。
②生成乙烯的电极反应式是___________ 。
③若电解过程中生成标准状况下4.48 L O2,电路中转移的电子至少为___________ mol。
(1)用CO2和H2制取甲醇,反应的能量变化如图所示。

根据上图计算CO2(g)+3H2(g)=CH3OH(l)+H2O(l) ΔH=
(2)萨巴帝尔(Sabatier)反应可以将二氧化碳转化为甲烷和水,配合水
 电解可以实现氧气的再生。该方法可同时解决二氧化碳的清除问题,因此成为一种非常重要的载人航天器中氧气再生方法。
电解可以实现氧气的再生。该方法可同时解决二氧化碳的清除问题,因此成为一种非常重要的载人航天器中氧气再生方法。①萨巴帝尔(Sabatier)反应是放热反应,控制反应器内的温度非常重要,反应温度过低则会造成
②萨巴帝尔(Sabatier)反应在载人航天器实现回收CO2再生O2,其过程如图所示,这种方法再生O2的最大缺点是需要不断补充

(3)铅蓄电池作为电源可将CO2转化为乙烯(C2H4),其原理如图所示,所用电极材料均为惰性电极。已知铅蓄电池总反应式为: PbO2+Pb+2H2SO4
 2PbSO4+2H2O
2PbSO4+2H2O
①铅蓄电池充电时Pb电极应与外加电源的
②生成乙烯的电极反应式是
③若电解过程中生成标准状况下4.48 L O2,电路中转移的电子至少为
您最近一年使用:0次
名校
解题方法
2 . 电化学给人类的生活和工业生产带来极大的方便。回答下列问题:
(1)一种利用垃圾渗滤液中 发电的原理如图所示。
发电的原理如图所示。

①X为该装置的_______ 极。
②该装置工作时,Y电极周围溶液的
_______ (填“升高”或“降低”)。
③写出该装置工作时的电池反应式:_______ 。
(2)若将(1)中电极X、Y分别与如图的a、f相连,一段时间后,测得 溶液浓度变为
溶液浓度变为 。
。

①电极b上生成的气体的体积(标准状况下)约为_______ L,该电极上发生的电极反应为_______ 。
②电极c的质量增加_______ g。
③一段时间后, 溶液中
溶液中 全部析出,此时电解还能继续进行,其原因是
全部析出,此时电解还能继续进行,其原因是_______ 。
(1)一种利用垃圾渗滤液中
 发电的原理如图所示。
发电的原理如图所示。
①X为该装置的
②该装置工作时,Y电极周围溶液的

③写出该装置工作时的电池反应式:
(2)若将(1)中电极X、Y分别与如图的a、f相连,一段时间后,测得
 溶液浓度变为
溶液浓度变为 。
。
①电极b上生成的气体的体积(标准状况下)约为
②电极c的质量增加
③一段时间后,
 溶液中
溶液中 全部析出,此时电解还能继续进行,其原因是
全部析出,此时电解还能继续进行,其原因是
您最近一年使用:0次
2022-04-04更新
|
192次组卷
|
3卷引用:陕西省铜川市第一中学2021-2022学年高二上学期期末考试化学试题
解题方法
3 . 科学家采用碳基电极材料设计了一种新的电解氯化氢回收氯气的工艺方案,原理如图所示。下列说法错误的是


| A.a是电源的正极 |
| B.阴极的电极反应式为:Fe2+-e-=Fe3+ |
| C.电路中每转移1mole-理论上可以回收氯气11.2L(标准状况) |
D.该工艺涉及的总反应为4HCl+O2 2Cl2+2H2O 2Cl2+2H2O |
您最近一年使用:0次
2022-03-15更新
|
566次组卷
|
7卷引用:陕西省西安市蓝田县乡镇高中联考2023-2024学年高二上学期11月期中化学试题
陕西省西安市蓝田县乡镇高中联考2023-2024学年高二上学期11月期中化学试题四川省成都市武侯高级中学2021-2022学年高二下学期期中考试化学试题河南省开封市2022届高三第二次模拟考试理综化学试题(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-2022年高考真题+模拟题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)(已下线)选择题11-15
名校
4 . 生活中,形式多样化的电池,满足不同的市场需求。图中是几种不同类型的原电池装置。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。
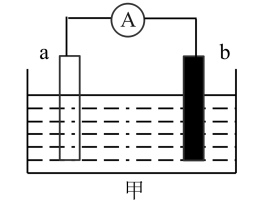
①若容器中盛有 溶液,a极为
溶液,a极为_______ (填“正极”或“负极”);b极附近观察到的现象是_______ 。
②若容器中盛有浓硫酸,b极的电极反应式是_______ ,导线中电子的流动方向是_______ (填“a→b”或“b→a”)。
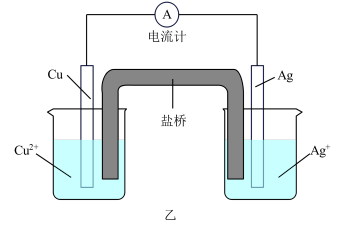
(2)铜-银原电池装置如图乙所示,下列有关叙述正确的是_______(填标号)。
(3)乙烯是水果的催熟剂,又可用作燃料,由 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。
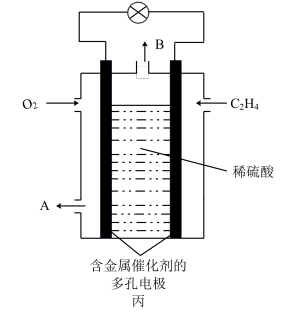
①乙烯燃料电池的正极反应式是_______ 。
②当消耗2.8g乙烯时,生成物质B的体积为_______ L(标准状况下)。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。

①若容器中盛有
 溶液,a极为
溶液,a极为②若容器中盛有浓硫酸,b极的电极反应式是
(2)铜-银原电池装置如图乙所示,下列有关叙述正确的是_______(填标号)。

| A.银电极上发生还原反应 |
| B.电池工作一段时间后,铜极的质量增加 |
| C.取出盐桥后,电流计依旧发生偏转 |
| D.电池工作时,每转移0.1mol电子,两电极的质量差会增加14g |
 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。
①乙烯燃料电池的正极反应式是
②当消耗2.8g乙烯时,生成物质B的体积为
您最近一年使用:0次
2022-03-08更新
|
379次组卷
|
2卷引用:陕西省西安中学2021-2022学年高二上学期期末考试化学试题
解题方法
5 . 如图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
请回答:
(1)溶液B中含有的阳离子有____ (填离子符号)。
(2)下列物质中最适宜做氧化剂X的是____ (填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,要调整pH范围是____ ,则试剂①可以选择____ (填化学式)。
(4)已知溶液中c(Cu2+)与pH的关系为lgc(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1 mol/L,此时溶液中的Fe3+能否沉淀完全:_____ (填“能”或“否”)。
(5)用下列装置对E中溶液进行电化学过程的示意图,其中A、B均为Pt电极。请填空:

①甲池中,B作____ 极(填电极名称),电极反应式为____ 。
②乙池中,Fe作____ 极(填电极名称),乙池中总反应的离子方程式为____ 。
③在此过程中若完全反应,乙池中Fe极的质量增加64 g,此时E溶液呈淡蓝色,则甲池中理论上消耗标准状况下O2____ L。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀 | 2.7 | 7.5 | 4.4 |
| 完全沉淀 | 3.7 | 9.7 | 6.7 |
请回答:
(1)溶液B中含有的阳离子有
(2)下列物质中最适宜做氧化剂X的是
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,要调整pH范围是
(4)已知溶液中c(Cu2+)与pH的关系为lgc(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1 mol/L,此时溶液中的Fe3+能否沉淀完全:
(5)用下列装置对E中溶液进行电化学过程的示意图,其中A、B均为Pt电极。请填空:

①甲池中,B作
②乙池中,Fe作
③在此过程中若完全反应,乙池中Fe极的质量增加64 g,此时E溶液呈淡蓝色,则甲池中理论上消耗标准状况下O2
您最近一年使用:0次
名校
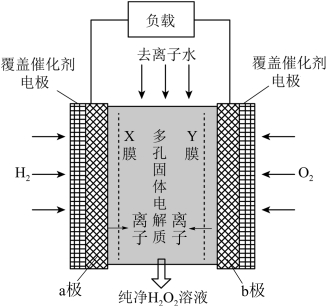
6 . 2019年11月《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示(已知:H2O2 H++
H++ ,Ka=2.4×10﹣12)。下列说法错误的是
,Ka=2.4×10﹣12)。下列说法错误的是
 H++
H++ ,Ka=2.4×10﹣12)。下列说法错误的是
,Ka=2.4×10﹣12)。下列说法错误的是
| A.X膜为阳离子交换膜 |
| B.每生成1molH2O2,外电路通过4mole- |
| C.催化剂可加快单位时间内反应中电子的转移数目 |
D.b极上的电极反应为:O2+H2O+2e- ═ +OH− +OH− |
您最近一年使用:0次
2022-02-28更新
|
399次组卷
|
15卷引用:陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题
陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题江苏省宿迁市沭阳县2019-2020学年高二下学期期中调研测试化学试题江苏省泰州中学2019-2020学年高二下学期第二次月考化学试题浙江省丽水市高中发展共同体2020-2021学年高二下学期期中联合测试化学试题安徽省合肥市六校2020-2021学年高二下学期期末联考化学试题山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题2019年江苏省南京、盐城高三第一次模拟考试化学试题山东省济宁市2020届高三下学期线上自我检测化学试题重庆市第一中学2020届高三3月月考理科综合化学试题江苏省连云港市老六所四星高中(海州高中 、赣榆高中 、海头中学 、东海高中 新海高中 、灌云高中)2020届高三模拟考试化学试题宁夏中卫市2020届高三第二次模拟考试理综化学试题天津市河西区2020芦台一中高三模拟测试江苏省常熟市2021-2022学年高三上学期阶段性抽测一化学试题山东省烟台第二中学2021-2022学年高一3月月月考化学试题
名校
解题方法
7 . 游泳池水普遍存在尿素超标现象,一种电化学除游泳池中尿素的实验装置如下图所示,其中钌钛用作析氯电极,不参与电解。除尿素的反应为: 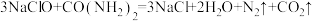 ,下列说法正确的是
,下列说法正确的是

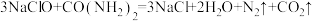 ,下列说法正确的是
,下列说法正确的是
| A.电解过程中不锈钢电极会缓慢发生腐蚀 |
B.电解过程中钌钛电极上发生反应为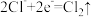 |
C.电解过程中不锈钢电极附近 增大 增大 |
D.电解过程中每逸出 ,电路中至少通过 ,电路中至少通过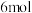 电子 电子 |
您最近一年使用:0次
2022-01-27更新
|
261次组卷
|
2卷引用:陕西省西安市铁一中学2022-2023学年高二上学期期末考试化学试题
8 . 已知:向FeCl2溶液中滴加稀硝酸,溶液颜色由浅绿色变为棕黄色。某同学用此反应设计了如图所示原电池。

(1)写出FeCl2与稀硝酸反应的离子方程式_______ 。
(2)图中电子流动方向为_______ 极到________ 极(填“a”或“b”)。
(3)在乙烧杯中会观察到的现象为______ ,写出乙烧杯中的电极反应方程式_______ 。
(4)H+流向______ 烧杯(填“甲”或“乙”),若一段时间内流向该烧杯的H+有0.05mol,则消耗Fe2+______ g。
(5)该装置存在的缺点是______ (写一点)。

(1)写出FeCl2与稀硝酸反应的离子方程式
(2)图中电子流动方向为
(3)在乙烧杯中会观察到的现象为
(4)H+流向
(5)该装置存在的缺点是
您最近一年使用:0次
解题方法
9 . 如图所示,若电解5min时铜电极质量增加2.16g,回答:
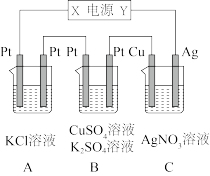
(1)电源电极X名称为___________ 。
(2)pH变化:A池___________ ,B池___________ ,C池___________ 。
(3)若A中KCl溶液的体积是200mL,电解后溶液的pH=___________ 。

(1)电源电极X名称为
(2)pH变化:A池
(3)若A中KCl溶液的体积是200mL,电解后溶液的pH=
您最近一年使用:0次
10 . Ⅰ.我国是世界氯碱工业大国,氯碱工业即采用电解饱和食盐水的方法来制备工业原料 、
、 、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
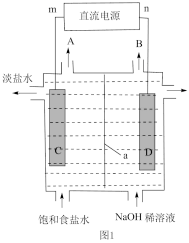
(1)n为直流电源的___________ (填“正”或“负”)极,电极D附近的pH___________ (填“增大”、“减小”或“不变”);离子交换膜a为___________ (填“阴”或“阳”)离子交换膜。
(2)写出该电解装置的总反应方程式:___________ 。
Ⅱ.一次化学实验课上,某兴趣小组组装了电化学装置(如图2),其中A、B、C、D、E、F均为石墨电极,U形管中为滴有几滴酚酞的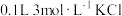 溶液,甲、乙烧杯中溶质电离出的离子均是
溶液,甲、乙烧杯中溶质电离出的离子均是 、
、 、
、 、
、 中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
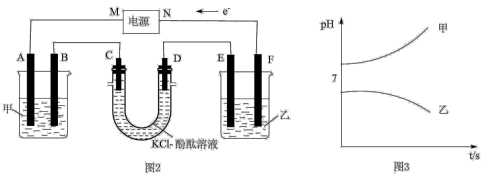
(3)甲、乙两烧杯中溶液的溶质分别为___________ 、___________ 。(填化学式)
(4)F极上的电极反应式为___________ 。
(5)①U形管中溶液先变红的一极为___________ (填“C”或“D”)极。
②若要将U形管中的溶液恢复到电解前的状态,应加入___________ mol的___________ (填物质名称)。
 、
、 、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
(1)n为直流电源的
(2)写出该电解装置的总反应方程式:
Ⅱ.一次化学实验课上,某兴趣小组组装了电化学装置(如图2),其中A、B、C、D、E、F均为石墨电极,U形管中为滴有几滴酚酞的
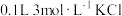 溶液,甲、乙烧杯中溶质电离出的离子均是
溶液,甲、乙烧杯中溶质电离出的离子均是 、
、 、
、 、
、 中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
(3)甲、乙两烧杯中溶液的溶质分别为
(4)F极上的电极反应式为
(5)①U形管中溶液先变红的一极为
②若要将U形管中的溶液恢复到电解前的状态,应加入
您最近一年使用:0次
2022-01-08更新
|
176次组卷
|
4卷引用:陕西省安康市2021-2022学年高二上学期期末考试化学试题



