名校
1 . 通过如图装置进行能量转化。下列分析不正确的是
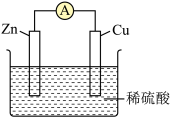

| A.该装置能将化学能转化为电能 |
| B.电子从锌片流向铜片,电流表指针偏转 |
C.Cu片;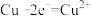 ;Zn片: ;Zn片: |
| D.氧化反应和还原反应可在两个不同的区域进行 |
您最近半年使用:0次
2023-07-13更新
|
187次组卷
|
4卷引用:北京朝阳区2022-2023学年高一下学期7月期末考试化学试题
名校
2 . 以软锰矿(主要成分为 )为原料制备粗二氧化锰颗粒的过程如下:
)为原料制备粗二氧化锰颗粒的过程如下:
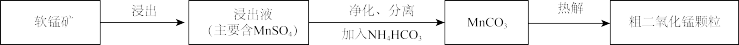
(1)浸出
①通入 浸出锰元素,该反应的化学方程式为
浸出锰元素,该反应的化学方程式为_______ 。
②研究表明, 可催化浸出效果,其催化过程如下:
可催化浸出效果,其催化过程如下:
过程Ⅰ: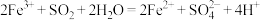 过程Ⅱ:……
过程Ⅱ:……
过程Ⅱ的离子方程式是_______ 。
③浸出液中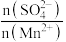 比值明显大于1,可能的原因是
比值明显大于1,可能的原因是_______ 。
(2)净化、分离
软锰矿浸出液中的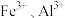 可通过加碱转化为沉淀去除,分离出清液的方法是
可通过加碱转化为沉淀去除,分离出清液的方法是_______ 。
(3)热解
在一定空气流速下,相同时间内 热解产物中不同价态
热解产物中不同价态 (Ⅱ、Ⅲ等代表锰元素的化合价)的占比随热解温度的变化如图。
(Ⅱ、Ⅲ等代表锰元素的化合价)的占比随热解温度的变化如图。 热解过程中涉及如下化学反应:
热解过程中涉及如下化学反应:
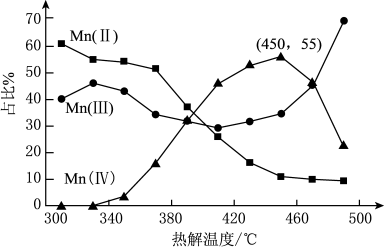
注:图中Mn(Ⅱ)等表示化合物中锰元素的价态
ⅰ.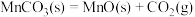
ⅱ.
ⅲ.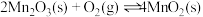
①为了增大产物中 的占比,可以采用的措施是
的占比,可以采用的措施是_______ (答出两条)。
②温度升高,产物中 的占比均降低,可能的原因是
的占比均降低,可能的原因是_______ 。
(4)碱性锌锰电池的总反应为: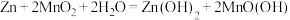 。
。
①电池的负极为_______ 。
②正极的电极反应为_______ 。
 )为原料制备粗二氧化锰颗粒的过程如下:
)为原料制备粗二氧化锰颗粒的过程如下: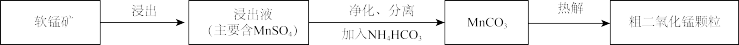
(1)浸出
①通入
 浸出锰元素,该反应的化学方程式为
浸出锰元素,该反应的化学方程式为②研究表明,
 可催化浸出效果,其催化过程如下:
可催化浸出效果,其催化过程如下:过程Ⅰ:
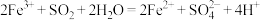 过程Ⅱ:……
过程Ⅱ:……过程Ⅱ的离子方程式是
③浸出液中
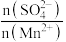 比值明显大于1,可能的原因是
比值明显大于1,可能的原因是(2)净化、分离
软锰矿浸出液中的
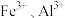 可通过加碱转化为沉淀去除,分离出清液的方法是
可通过加碱转化为沉淀去除,分离出清液的方法是(3)热解
在一定空气流速下,相同时间内
 热解产物中不同价态
热解产物中不同价态 (Ⅱ、Ⅲ等代表锰元素的化合价)的占比随热解温度的变化如图。
(Ⅱ、Ⅲ等代表锰元素的化合价)的占比随热解温度的变化如图。 热解过程中涉及如下化学反应:
热解过程中涉及如下化学反应:
注:图中Mn(Ⅱ)等表示化合物中锰元素的价态
ⅰ.
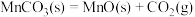
ⅱ.

ⅲ.
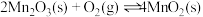
①为了增大产物中
 的占比,可以采用的措施是
的占比,可以采用的措施是②温度升高,产物中
 的占比均降低,可能的原因是
的占比均降低,可能的原因是(4)碱性锌锰电池的总反应为:
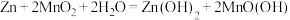 。
。①电池的负极为
②正极的电极反应为
您最近半年使用:0次
名校
解题方法
3 . 某学习小组探究某浓度浓硝酸和稀硝酸与铁的反应。
(1)Ⅰ中液面上方气体由无色变为红棕色的化学方程式为_______ 。
(2)取少量Ⅰ中溶液,加入KSCN溶液,_______ (填现象),说明产生了Fe3+。
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有_______ 性。
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
①用方程式解释现象ⅳ:_______ 。
②推测现象ⅰ中被还原的是_______ 。
③解释现象ii中指针左右偏转,往复多次的原因_______ 。
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是_______ 。
| 实验 | 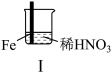 | 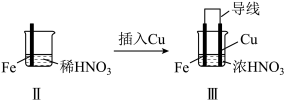 | |
| 现象 | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 | Ⅱ中:Fe表面产生红棕色气泡,过一会儿停止 | Ⅲ中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;随即又产生红棕色气泡,而后停止,……如此往复多次。Cu表面始终产生红棕色气泡 |
(2)取少量Ⅰ中溶液,加入KSCN溶液,
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
| 实验 | 现象 |
 | ⅰ.K闭合时,指针向左偏转(Cu做负极),Fe表面无明显现象 ⅱ.过一会儿指针向右偏,Fe表面产生红棕色气体;后又迅速向左偏,Fe表面停止产生气泡,……如此往复多次 ⅲ.一段时间后,指针一直处于右端,Fe表面持续产生红棕色气体 ⅳ.Cu表面始终产生红棕色气泡 |
②推测现象ⅰ中被还原的是
③解释现象ii中指针左右偏转,往复多次的原因
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是
您最近半年使用:0次
2021-04-05更新
|
826次组卷
|
5卷引用:北京市朝阳区2021届高三一模化学试题
北京市朝阳区2021届高三一模化学试题(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)2021年北京高考化学试题变式题11-19辽宁省葫芦岛市普通高中2021-2022学年高三上学期期末学业质量监测化学试题北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
4 . 下列关于Cu-Zn原电池装置(如右图所示)的叙述中,不正确 的是( )
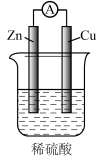

| A.铜片上有无色气体生成 |
| B.锌片做负极,电极反应式是Zn-2e-=Zn2+ |
| C.工作一段时间后,溶液中c(H+)减小 |
| D.电子从铜片经导线流向锌片 |
您最近半年使用:0次
2020-07-17更新
|
265次组卷
|
3卷引用:北京市第八十中学2021-2022学年高一下学期期中考试化学试题
名校
解题方法
5 . 我国科学家研发了一种水系可逆Zn-CO2电池,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充电、放电时,复合膜层间的H2O解离成H+和OH-,工作原理如图所示。下列说法错误的是( )


| A.a膜是阳离子膜,b膜是阴离子膜 |
| B.放电时负极的电极反应式为Zn+4OH--2e-=Zn(OH)42- |
| C.充电时CO2在多孔Pd纳米片表面转化为甲酸 |
| D.外电路中每通过1mol电子,复合膜层间有1mol H2O解离 |
您最近半年使用:0次
2020-06-08更新
|
1859次组卷
|
12卷引用:北京市朝阳区第八十中学2020届高三模拟化学试题
北京市朝阳区第八十中学2020届高三模拟化学试题广东省广州市2020届高三综合测试(二)理科综合化学试题广东省广州大学附属中学等三校2021届高三上学期返校联考化学试题宁夏银川一中2021届高三第五次月考化学试题天津市滨海七校2021届高三上学期期末联考化学试题浙江省杭州第二中学2021届高三上学期期中考试化学试题第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题北京一零一中学2021-2022学年高三下学期入学考试化学试题辽宁省六校2023届高三上学期开学考试化学试题山东师范大学附属中学2023届高三下学期6月模拟考试化学试题山东省齐鲁名师联盟2023-2024学年高三上学期第一次诊断考试化学试题广东省汕头市潮阳实验学校2021届高三下学期第二次月考化学试题
名校
解题方法
6 . 电能是现代社会应用最广泛的能源之一。
(1)某原电池装置如图所示。其中,Zn 电极为原电池的______ 极(填“正” 或“负”),电极反应式是______ 。Cu 电极上发生的反应属于______ (填“氧化”或“还原”) 反应。
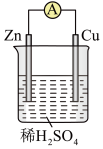
(2)能证明产生电能的实验现象是______ 。
(3)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如图。下列说法正确的是______ (填序号)。
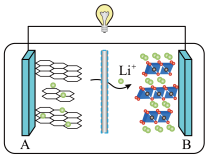
① A 为电池的正极
② 该装置实现了化学能转化为电能
③ 电池工作时,电池内部的锂离子定向移动
(1)某原电池装置如图所示。其中,Zn 电极为原电池的

(2)能证明产生电能的实验现象是
(3)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如图。下列说法正确的是

① A 为电池的正极
② 该装置实现了化学能转化为电能
③ 电池工作时,电池内部的锂离子定向移动
您最近半年使用:0次
名校
解题方法
7 . 下图为氢氧燃料电池构造示意图,按照此图的提示,下列叙述不正确的是
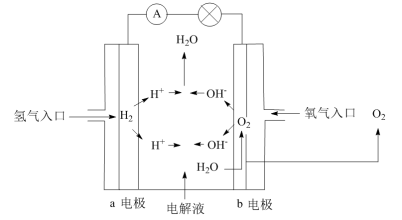

| A.a 电极是负极 |
| B.电子由b 通过灯泡流向 a |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
您最近半年使用:0次
2020-05-02更新
|
303次组卷
|
3卷引用:北京市第八十中学2019-2020学年高一下学期期中考试化学试题
名校
8 . 某同学设计如下原电池,其工作原理如图所示。下列说法不正确 的是
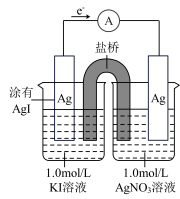

| A.该装置将化学能转化为电能 |
| B.负极的电极反应是:Ag +I--e-=AgI |
| C.电池的总反应是Ag+ +I-=AgI |
| D.盐桥(含KNO3的琼脂)中NO3-从左向右移动 |
您最近半年使用:0次
2019-07-30更新
|
1360次组卷
|
9卷引用:北京市朝阳区2018-2019学年高二第二学期期末统一考试化学试题
北京市朝阳区2018-2019学年高二第二学期期末统一考试化学试题(已下线)1.2.1 原电池的工作原理(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 化学能转化为电能——电池 课时2 化学电源高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 第一节综合训练(已下线)第2章 化学反应与能量(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)选择性必修1专题1第二单元 综合训练福建省石狮市第一中学2022-2023学年高二上学期第一次月考化学试题(已下线)第六章 化学反应与能量 第35练 原电池 化学电源湖北省襄阳市第一中学2022-2023学年高一下学期4月月考化学试题
9 . 我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。下列说法不正确 的是
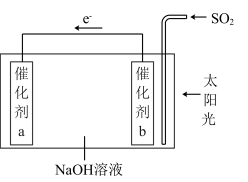

| A.该装置可将太阳能转化为化学能 |
| B.催化剂a表面发生还原反应,产生H2 |
| C.催化剂b附近的溶液pH增大 |
| D.吸收1 mol SO2,理论上能产生1 mol H2 |
您最近半年使用:0次
2019-04-04更新
|
1268次组卷
|
7卷引用:【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题
名校
10 . 微生物燃料电池在净化废水的同时能获得能源或得到有价值的化学产品,图1为其工作原理,图2为废水中Cr2O72-离子浓度与去除率的关系。下列说法不正确的是
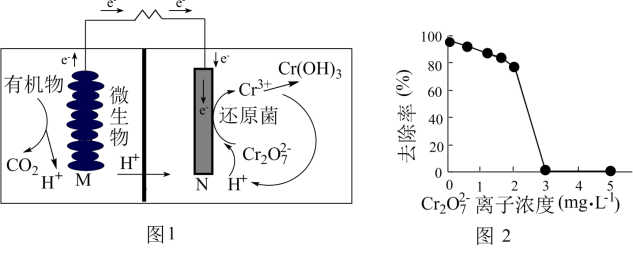

| A.M为电源负极,有机物被氧化 |
| B.处理1 mol Cr2O72-时有6 mol H+从交换膜左侧向右侧迁移 |
| C.电池工作时,N极附近溶液pH增大 |
| D.Cr2O72-离子浓度较大时,可能会造成还原菌失活 |
您最近半年使用:0次
2018-12-26更新
|
379次组卷
|
8卷引用:北京市朝阳区2017~2018学年度第一学期高三年级期末质量检测化学试题



