名校
解题方法
1 . 根据化学能转化为电能的相关知识,回答下列问题:
I.理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是____ (填化学式),电解质溶液是____ (填化学式)溶液。
(2)正极上发生的电极反应为____ 。
(3)若导线上转移的电子为1mol,则消耗的金属铜的质量为____ 。
II.甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。
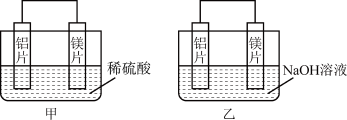
(4)甲池中出现气泡的电极材料为____ 。
(5)乙中作负极的是____ ,写出负极上的电极反应式:____ 。
(6)如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是____ (填标号)。
I.理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上发生的电极反应为
(3)若导线上转移的电子为1mol,则消耗的金属铜的质量为
II.甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。

(4)甲池中出现气泡的电极材料为
(5)乙中作负极的是
(6)如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是
| A.镁的金属性不一定比铝的金属性强 |
| B.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析 |
您最近一年使用:0次
名校
解题方法
2 . 新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温。该体温枪所用的电池为一种银锌电池(如图所示),该电池的总反应式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag。下列关于该电池的说法正确的是
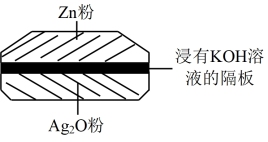

| A.Ag2O电极作正极,发生氧化反应 |
| B.该电池放电时溶液中的K+向Zn电极移动 |
| C.电池工作时,电子从Ag2O电极经过隔板流向Zn电极 |
| D.该电池的负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
您最近一年使用:0次
2022-04-27更新
|
335次组卷
|
9卷引用:甘肃省天水市第一中学2021-2022学年高一下学期第一阶段考试化学试题
甘肃省天水市第一中学2021-2022学年高一下学期第一阶段考试化学试题(已下线)第12讲 化学电池(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市嘉定区第一中学2021-2022学年高一下学期期期末考试化学试题福建省福州第三中学2021-2022学年高一下学期期末考试化学试题陕西省渭南市大荔县2020-2021学年高二下学期期末考试化学试题(已下线)社会热点之新冠肺炎背景下的相关研究(已下线)选择性必修1 综合检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)广东省江门市第二中学2021-2022学年高二上学期第一次月考化学试题广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第一次月考化学试题
名校
3 . 如图装置的说法正确的是
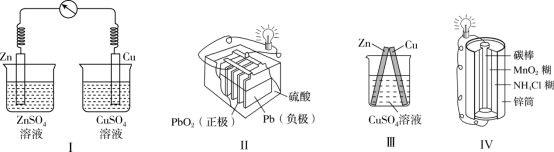

| A.图Ⅰ所示装置能将化学能转化为电能 |
| B.图Ⅱ所示装置属于一次电池 |
| C.图Ⅲ所示装置中铜棒上发生还原反应 |
| D.图Ⅳ工作时,电子由碳棒通过导线流向锌筒 |
您最近一年使用:0次
2022-04-15更新
|
380次组卷
|
3卷引用:甘肃省民乐县第一中学2021-2022学年高一下学期期中考试化学试题
名校
4 . 人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)碱性水溶液条件下纽扣式银锌电池的总反应为:Zn+Ag2O=2Ag+ZnO,则其正极电极反应式为:___________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为___________ ,电解质溶液为___________ ,反应中Cl-移向___________ (填“负极”或“正极”),FeCl3溶液发生___________ 反应(填“氧化”或“还原”)。当线路中转移0.2mol电子时,参与反应的铜的质量为___________ g.
(3)燃料电池是一种高效、环境友好的供电装置,如图为乙烷燃料电池原理示意图。
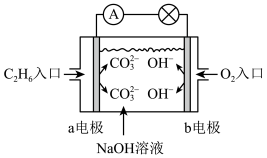
①乙烷通入的一极为电源的___________ 极,该电极反应式:___________ 。
②有0.05molC2H6参与反应时,消耗的氧气体积在标准状况下为___________ L。
(1)碱性水溶液条件下纽扣式银锌电池的总反应为:Zn+Ag2O=2Ag+ZnO,则其正极电极反应式为:
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(3)燃料电池是一种高效、环境友好的供电装置,如图为乙烷燃料电池原理示意图。

①乙烷通入的一极为电源的
②有0.05molC2H6参与反应时,消耗的氧气体积在标准状况下为
您最近一年使用:0次
名校
5 . 如图所示,电流计G发生偏转,同时A极逐渐变细,B极逐渐变粗,C为电解质溶液,则A、B、C应是下列各组中的
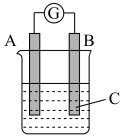

| A.A是Zn、B是Cu、C为稀硫酸 |
| B.A是Cu、B是Al、C为CuSO4溶液 |
| C.A是Zn、B是石墨、C为AgNO3溶液 |
| D.A是石墨、B是Fe、C为FeCl3溶液 |
您最近一年使用:0次
2021-12-01更新
|
1187次组卷
|
9卷引用:甘肃省兰州第一中学2020-2021学年高一上学期期中考试化学试题
甘肃省兰州第一中学2020-2021学年高一上学期期中考试化学试题(已下线)综合测试卷-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)山东省临沂市2021-2022学年高一下学期期中考试化学试题河南省平顶山第一中学2022-2023学年高一下学期校内质量检测(一)化学试题吉林省长春市新解放学校2022-2023学年高一下学期4月月考化学试题四川省江油中学2022-2023学年高一下学期期中考试化学试题山东省泰安第二中学2022-2023学年高一下学期4月月考化学试题河南省南阳市邓州市第一高级中学校2023-2024学年高一下学期第一次月考化学试题B卷福建师范大学附属中学2021-2022学年高一下学期期末考试化学试题
解题方法
6 . 写出下列原电池的电极反应和总反应(属于离子反应的,用离子方程式表示)。
(1)负极:___________ ;正极:___________ ;总反应式:___________ 。
(2)负极:___________ ;正极:___________ ;总反应式:___________ 。
| 负极 | 正极 | 电解质溶液 | |
| (1) | 铁 | 铜 | 稀硫酸 |
| (2) | 铜 | 银 | AgNO3溶液 |
(1)负极:
(2)负极:
您最近一年使用:0次
7 . 现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀H2SO4溶液中,电子流动方向为A→导线→C。
根据上述情况,回答下列问题:
(1)在①中,金属片___________ 发生氧化反应,金属片___________ 作正极;
(2)在②中,金属片___________ 作负极;___________ 金属更活泼。
(3)如果把B、D用导线连接后同时浸入稀H2SO4溶液,则金属片___________ 上有气泡产生;
(4)上述四种金属的活动性由强到弱的顺序是___________ 。
①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;
③把A、C用导线连接后同时浸入稀H2SO4溶液中,电子流动方向为A→导线→C。
根据上述情况,回答下列问题:
(1)在①中,金属片
(2)在②中,金属片
(3)如果把B、D用导线连接后同时浸入稀H2SO4溶液,则金属片
(4)上述四种金属的活动性由强到弱的顺序是
您最近一年使用:0次
名校
解题方法
8 . 有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B为正极。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活泼性由强到弱的顺序是
| A.D>A>B>C | B.B>A>D>C | C.D>B>A>C | D.D>A>C>B |
您最近一年使用:0次
2021-10-09更新
|
561次组卷
|
12卷引用:甘肃省兰州市第一中学2020-2021学年高一下学期期中考试化学(文)试题
甘肃省兰州市第一中学2020-2021学年高一下学期期中考试化学(文)试题湖南省常德市第一中学2020-2021学年高一下学期第一次月考化学试题浙江省宁波市北仑中学2020-2021学年高一下学期期中考试化学试题浙江省宁波市北仑中学2020-2021学年高一下学期期中考试化学(1班选考)试题黑龙江省哈尔滨宾县第一中学2020-2021学年高一下学期第一次月考化学试题黑龙江省牡丹江市三校联谊2020-2021学年高一下学期期中考试化学试题新疆阜康市第一中学2020-2021学年高一下学期期中考试化学试题云南省昆明市第八中学2020-2021学年高一下学期期中考试理科化学试题福建省莆田市第一中学2021-2022学年高一下学期期末考试化学试题浙江省平湖市平湖杭州湾实验学校2021-2022学年高一下学期第一次月考化学试题广西桂林市临桂区五通中学2021-2022学年高一下学期期中考试化学试题四川省广元市树人中学2021-2022学年高三上学期第二次段考化学试题
9-10高一下·陕西西安·期中
名校
解题方法
9 . 有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:
| A.A>B>C>D | B.B>D>C>A | C.A>C>D>B | D.C>A>B>D |
您最近一年使用:0次
2021-10-09更新
|
924次组卷
|
124卷引用:2011-2012学年甘肃省张掖二中高一下学期期中考试化学试卷
(已下线)2011-2012学年甘肃省张掖二中高一下学期期中考试化学试卷 2015-2016学年甘肃省天水一中高一下期中理科化学试卷【全国百强校】甘肃省天水市一中2018-2019学年高一(文)下学期第二学段考试化学试题甘肃省东乡族自治县第二中学2017-2018学年高一下学期期中考试化学试题甘肃省庆阳市宁县第二中学2019-2020学年高一下学期期中考试化学试题(已下线)甘肃省宁县二中2018-2019高一下学期期中考试化学试卷甘肃省酒泉市青海油田第一中学2020-2021学年高一下学期期中考试化学试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)2010年陕西省西安铁一中高一第二学期期中考试化学试题(已下线)2010年黑龙江省哈六中高一下学期期中考试化学试题(已下线)09-10年深圳高中高一下学期期末测试化学卷(已下线)2010年山东省阳信一中高一第二学期期末考试化学试题(已下线)2010-2011学年江西省鄱阳县油墩街中学高一下学期期中考试化学试卷(已下线)2010-2011学年黑龙江省牡丹江一中高一下学期期中考试化学试卷(已下线)2010-2011学年广东省潮州金中高一下学期期中考试化学(理科班)化学卷(已下线)2010—2011学年广东惠阳高级中学高一第二学期期末考试化学试卷(已下线)2011-2012学年江西省横峰中学高一下学期期中考试化学试卷(已下线)2011-2012学年四川省资阳中学高一下半期考试化学试卷(已下线)2011-2012学年浙江省温州四中高一下学期期中考试化学试卷(已下线)2012-2013学年陕西省长安一中高一下学期期中考试化学试卷(已下线)2012-2013学年江苏省南京学大教育专修学校高一4月月考化学试卷(已下线)2014年高一化学人教版必修二 2-2-1化学能转化为电能练习卷(已下线)2013-2014河北省邢台一中高一下学期第三次月考化学试卷(已下线)2013届江西省高安中学高一下学期期中考试试题化学试卷(已下线)2014年7月山东省泰安市高一年级考试化学试卷(已下线)2013-2014江西省上高二中高一下学期期末考试化学试卷2014-2015浙江省杭州地区七校高一下学期期中联考化学试卷2015-2016学年山西省祁县中学高一上学期升学化学试卷2015-2016学年四川省成都石室中学高一4月月考化学试卷2015-2016学年河北省邢台一中高一下期中化学试卷2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷2015-2016学年陕西省西安交大二中南校高一下学期期中考试化学试卷2015-2016学年河北省邯郸市鸡泽一中高一5月月考化学试卷2015-2016学年北大附中河南分校高一下期末化学试卷2015-2016学年吉林东北师大附属实验高一下期末化学试卷2015-2016学年山东济南一中高一下期末化学试卷新疆生产建设兵团第二中学2016-2017学年高一下学期第二次月考化学试题吉林省汪清县第六中学2016-2017学年高一下学期期中考试化学试题江西省宜春市奉新县第一中学2016-2017学年高一下学期期末考试化学试题山东省平邑县曾子学校2016-2017学年高一下学期期末考试化学试题四川省威远中学2017-2018学年高一下学期期中考试化学试题【全国百强校】江西省高安中学2017-2018学年高一下学期期末考试化学试题【全国百强校】广东省深圳市南山区深圳实验学校高中部2017-2018学年高一下学期第一次阶段考试化学试题【全国百强校】辽宁省实验中学2016-2017学年高一下学期期中考试文科反向理科综合化学试题(已下线)2019年3月19日 《每日一题》必修2 原电池工作原理的应用【全国百强校】山东省师范大学附属中学2018-2019学年高一下学期期中考试化学试题【全国百强校】河北省张家口市第一中学2018-2019学年高一下学期期中考试化学试题2【全国百强校】天津市静海区第一中学2018-2019学年高一(等级班)下学期5月月考化学试题【全国百强校】天津市静海区第一中学2018-2019学年高一(合格班)下学期5月月考化学试题吉林省白山市第十九中学2018-2019学年高一下学期期中考试化学试题吉林省白城市通榆县第一中学2018-2019学年高一6月月考化学试题黑龙江省青冈县一中2018-2019学年高一下学期期末考试(B班)化学试题辽宁省凌源市联合校2019-2020学年高一上学期期中考试化学试题安徽省合肥市第二中学2018-2019学年高一下学期期中考试化学试题陕西省渭南市三贤中学2020年高一下学期期中考试化学试题山西省运城市临猗县临晋中学2019-2020学年高一下学期开学复课摸底考试化学试题湖南省长沙市长沙县2019-2020学年高一下学期6月联考化学试题青海省西宁市大通回族土族自治县第一完全中学2019-2020学年高一下学期期中考试化学试题山西省朔州市怀仁市第一中学云东校区2019-2020学年高一期末考试化学试题北京市首都师范大学附属中学2019-2020学年高一下学期结业考试(期末)化学试题湖北省荆门市2019-2020学年高一下学期期末考试化学试题高一必修第二册(人教2019版)第六章 第一节 化学反应与能量变化 课时2 化学能转化为电能江苏省泗阳桃州中学2019-2020学年高一下学期期末考试化学试题人教版2019必修第二册 第六章 第一节 第2课时 化学反应与电能江苏省盐城市伍佑中学2020-2021学年高一下学期第一次阶段考试化学试题浙江省温州市越秀学校2020-2021学年高一下学期3月月考化学试题山西省长治市第二中学校2020-2021学年高一下学期期中考试化学试题江苏省徐州市邳州市运河中学2020-2021学年高一下学期期中考试(实验班)化学试题北京市第六十六中学2020-2021学年高一下学期期中考试化学试题天津市实验中学滨海学校2020-2021学年高一下学期期中化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 第三单元 化学能与电能的转化 课时1 化学能转化为电能浙江省余姚市第七中学2020-2021学年高一下学期第一次阶段性考试化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期中考试化学(理)试题(已下线)第08讲 化学反应与电能(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)云南省瑞丽市第一民族中学2021-2022学年高一上学期期末考试 化学试题北京市第四十三中学2021-2022学年高一下学期期中考试化学试题四川省泸县第一中学2021-2022学年高一下学期期中考试化学试题四川省遂宁市射洪中学校2021-2022学年高一下学期第二次月考化学试题新疆乌苏市第一中学2021-2022学年高一下学期期中考试化学试题(加强班)辽宁省鞍山市第三中学、华育高级中学2021-2022学年高一下学期期中考试化学试题四川省凉山州宁南中学2021-2022学年高一下学期第一次月考化学试题浙江省杭州市源清中学2021-2022学年高一下学期期中考试化学试题(已下线)浙江省杭州市2021-2022学年杭州第九中学高一下学期期中考试化学试题云南红河县第一中学2021-2022学年高一下学期期末考试化学试题吉林省延边朝鲜族自治州汪清县汪清第四中学2020-2021学年高一下学期期末考试化学试题广东省江门市第一中学2021-2022学年高一下学期第一次月考化学试题重庆市江津第五中学校2020-2021学年高一下学期半期考试化学试题(已下线)6.1.2 化学反应与电能——同步学习必备知识浙江省宁波市姜山中学2022-2023学年高一下学期3月月考化学试题湖南省益阳市安化县第二中学2022-2023学年高一下学期4月月考化学试题广东省汕头市潮阳区河溪中学2022-2023学年高一下学期期中考试化学试题(已下线)6.1.2化学反应与电能-随堂练习(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷(已下线)2011-2012学年吉林省松原市宁江区实验中学高二上学期12月份月考化学试卷(已下线)2012年苏教版高中化学选修6 5.1原电池练习卷(已下线)2013-2014学年江苏省无锡江阴市高二下学期期中考试化学试卷(已下线)2014-2015学年福建省宁德市五校高二上学期期中化学试卷2014-2015学年湖北省枣阳市高级中学高二下学期期末化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2015-2016学年吉林省长春外国语学校高二上学期期末化学试卷2016-2017学年吉林省毓文中学高二上期中化学卷宁夏吴忠中学2017-2018学年高二下学期开学考试化学试题内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题安徽省天长市天长二中2018-2019学年高二第一学期12月月考化学试题福建省永安市第三中学2019-2020学年高二10月月考化学试题安徽省合肥市肥东县第二中学2019-2020学年高二上学期第二次月考化学试题(普通班)吉林省松原市前郭尔罗斯蒙古族中学2020-2021学年高二上学期期中考试化学试题福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题河北省秦皇岛市第一中学2020-2021学年高二上学期12月月考化学试题河北省任丘市第一中学2020-2021学年高二上学期第二次阶段考试化学试题吉林省长春市农安县2020-2021学年高二上学期期末考试化学试题黑龙江省鸡东二中2020-2021学年高二上学期期末考试化学试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2020-2021年度高二上学期期中考试化学试题青海省西宁市海湖中学2021-2022学年高二上学期开学考试化学试题四川省江油中学2020-2021学年高二下学期4月月考化学试题黑龙江省实验中学2021-2022学年高二上学期第一次月考化学试题吉林省榆树市第一高级中学校2021-2022学年高二上学期10月月考化学试题云南省玉溪市民族中学2021-2022学年高二上学期期末考试化学试题云南省瑞丽市第一民族中学2021-2022学年高二上学期期末考试化学试题云南省文山州第一中学2021-2022学年高二下学期3月份考试化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期开学考试化学试题 天津市静海区第一中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 现有反应①Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑②Fe+H2SO4=FeSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是___________ (填序号,下同),能设计成原电池的是___________ 。
(2)铁铜原电池的装置如图所示。
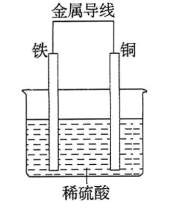
①铁作___________ (填“正极”或“负极”),溶液中的H+向___________ (填“铁”或“铜”)电极方向移动。
②正极的现象是___________ 。负极的电极方程式为___________ 。
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为___________ L。
(1)两反应中属于吸热反应的是
(2)铁铜原电池的装置如图所示。

①铁作
②正极的现象是
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
2021-10-08更新
|
762次组卷
|
7卷引用:甘肃省永昌县第一高级中学2021-2022学年高一下学期期中合格性考试化学试题
甘肃省永昌县第一高级中学2021-2022学年高一下学期期中合格性考试化学试题河北省保定市2016-2017学年高一下学期期中考试化学试题(已下线)6.1.2 化学反应与电能(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)河南省开封市五县联考2020-2021学年高一下学期期中考试化学试题吉林省长春市2020-2021学年高一下学期期末联考化学试题广东省清远市2021-2022学年高一下学期期中调研考试化学试题(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)



